Clear Sky Science · ar
يحمي فيسكيون-8-O-β-D-مونوجلوكوزيد خلايا الكبد من الاستماتة المحفزة بواسطة TNF-α عبر قمع مسار الإشارات PI3K/AKT/NF-κB
لماذا هذا مهم لصحة الكبد
أمراض الكبد تمثل مشكلة عالمية متزايدة، وتبدأ العديد من الحالات بضرر مفاجئ وشديد لخلايا الكبد يُعرف بإصابة الكبد الحادة. هذا النوع من الضرر يمكن أن يقود بسرعة إلى فشل كبدي إذا لم يُتحكم فيه، ومع ذلك العلاجات الحالية محدودة. تستقصي الدراسة وراء هذا المقال مركبًا طبيعيًا مشتقًا من عشب صيني تقليدي قد يساعد في حماية خلايا الكبد من أحد أقوى الإشارات الالتهابية الضارة في الجسم.
مركب نباتي بنكهة حديثة
المركب المحوري في هذا العمل يدعى فيسكيون-8-O-β-D-مونوجلوكوزيد (PMG)، يوجد في Radix et Rhizoma Rhei، وهو جذر يشبه الزنجبيل يستخدم في الطب الصيني التقليدي لمشاكل الكبد. أبحاث سابقة أشارت إلى أن مستخلصات خام ومركبات ذات صلة قد تحمي الكبد، لكنها كانت تمتص بشكل سيء وكانت آلياتها الدقيقة غير واضحة. PMG هو شكل أكثر قابلية للامتصاص، يصل إلى مستويات أعلى في مجرى الدم بعد الجرعات الفموية. لاحظ المؤلفون سابقًا أن PMG يمكن أن يخفف الضرر الكبدي الناجم عن السموم في الفئران، وفي هذه الدراسة سعوا لكشف كيف يعمل بالضبط على المستوى الخلوي والجزيئي.
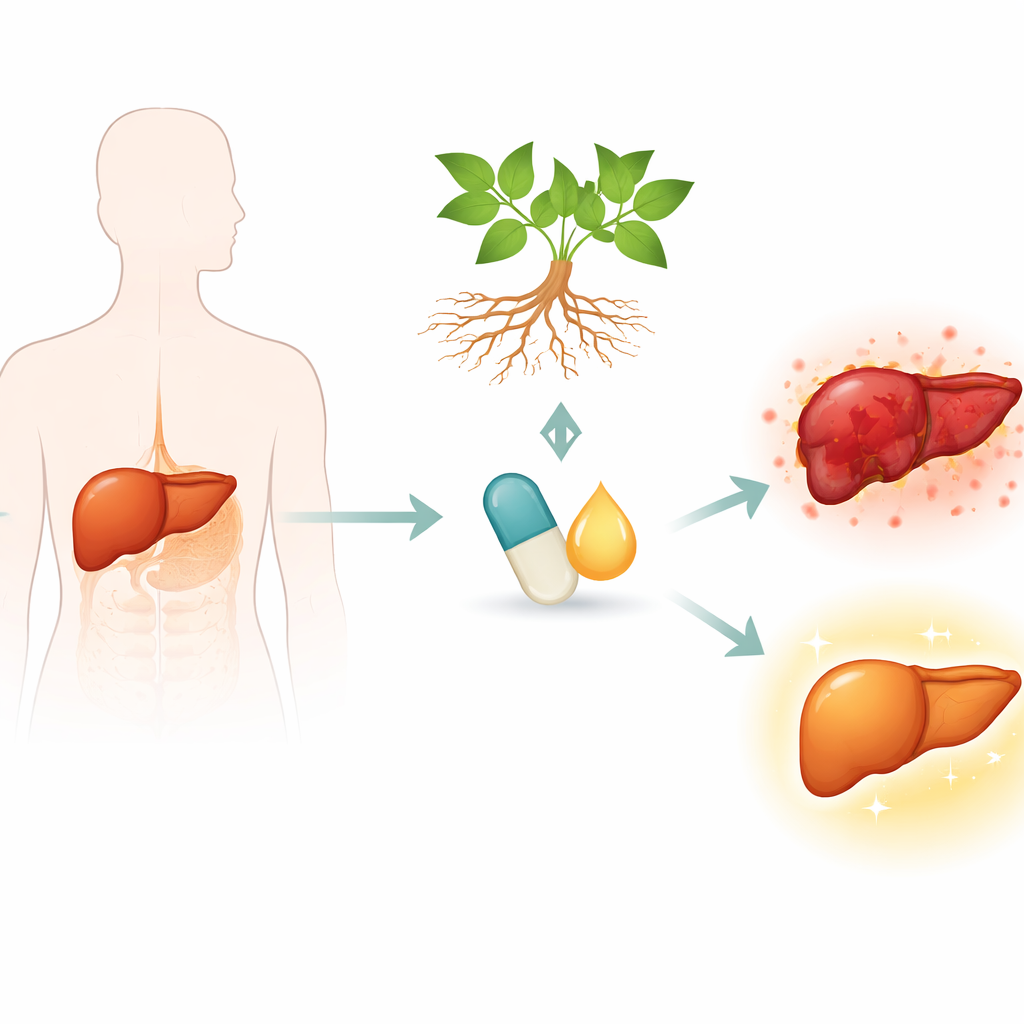
خفض إشارة إنذار خطيرة
لاعب رئيسي في إصابة الكبد الحادة هو عامل نخر الورم-ألفا (TNF-α)، إشارة إنذار قوية يفرزها جهاز المناعة. يرتبط TNF-α بمستقبل على خلايا الكبد يسمى TNFR1 ويمكن أن يدفع تلك الخلايا نحو الموت المبرمج والالتهاب. باستخدام خلايا كبد فأرية مزروعة وفي فئران تعرضت لمادة كيميائية مدمرة للكبد (رباعي كلوريد الكربون)، أظهر الباحثون أن PMG يساعد هذه الخلايا على البقاء في مواجهة إجهاد محفز بواسطة TNF-α. في الأطباق الخلوية، لم يسبب PMG ضررًا للخلايا السليمة بمفرده، لكن عندما أُضيف TNF-α ودواء حساس، أعاد PMG بقاء الخلايا، وحسّن شكل الخلايا، وخفض تسرب إنزيمات الكبد — وهي مؤشرات على تلف الخلايا — إلى وسط الزرع.
دليل من أمخاخ فئران مصابة
في الفئران الحية، تسبب رباعي كلوريد الكربون بعلامات كلاسيكية لإصابة كبد حادة: اضطراب في بنية النسيج، وموت واسع للخلايا، وارتفاع حاد في مستويات إنزيمات الكبد (AST وALT) في الدم. الحيوانات المعالجة مسبقًا بـPMG أظهرت أنسجة كبدية أكثر صحة بشكل واضح، ومستويات إنزيمات أقل، وخلايا ميتة أقل عند فحوص صبغية مجهرية متعددة. كما خفض PMG إنتاج الكبد نفسه لـTNF-α ولامتدٍ التهابي آخر، الإنترلوكين-6. عندما أجبر الفريق الكبد على إنتاج كمية إضافية من TNF-α باستخدام فيروس ناقل للجين، اختفت فوائد PMG إلى حد كبير. هذا الانعكاس يشير بقوة إلى أن التأثيرات الوقائية لـPMG تعتمد على إبقاء TNF-α وتبعاته قيد الكبح.
حجب تفاعل سلسلة ضار داخل الخلايا
لفهم كيف يهديء PMG إشارة TNF-α، نظر الباحثون إلى سلسلة أحداث جزيئية معروفة داخل الخلايا، وهي مسار PI3K/AKT/NF-κB. عند فرط تنشيطه، يعزز هذا المسار نشاط الجينات الالتهابية ويشجع موت الخلايا. استخدم الفريق محاكاة ربط جزيئي بالحاسوب لتوضيح أن PMG يمكنه الارتباط مباشرة بمستقبل TNFR1، مما يدعم الفكرة أنه يتداخل في أول خطوة من الإشارة. في أكباد الفئران المتضررة برابع كلوريد الكربون، كانت مستويات PI3K وAKT النشطة وNF-κB النووي مرتفعة، وكذلك بروتين المنفذ المنشق كاسبيز-3، وهو علامة مميزة لخلايا تخضع للموت المبرمج. قلل علاج PMG من كل هذه الإشارات وخفض تفعيل كاسبيز-3. ومع ذلك، عندما تم إفراط إنتاج TNF-α صناعيًا، فقدت هذه التغيرات الوقائية واندلع المسار الإشارِي من جديد.
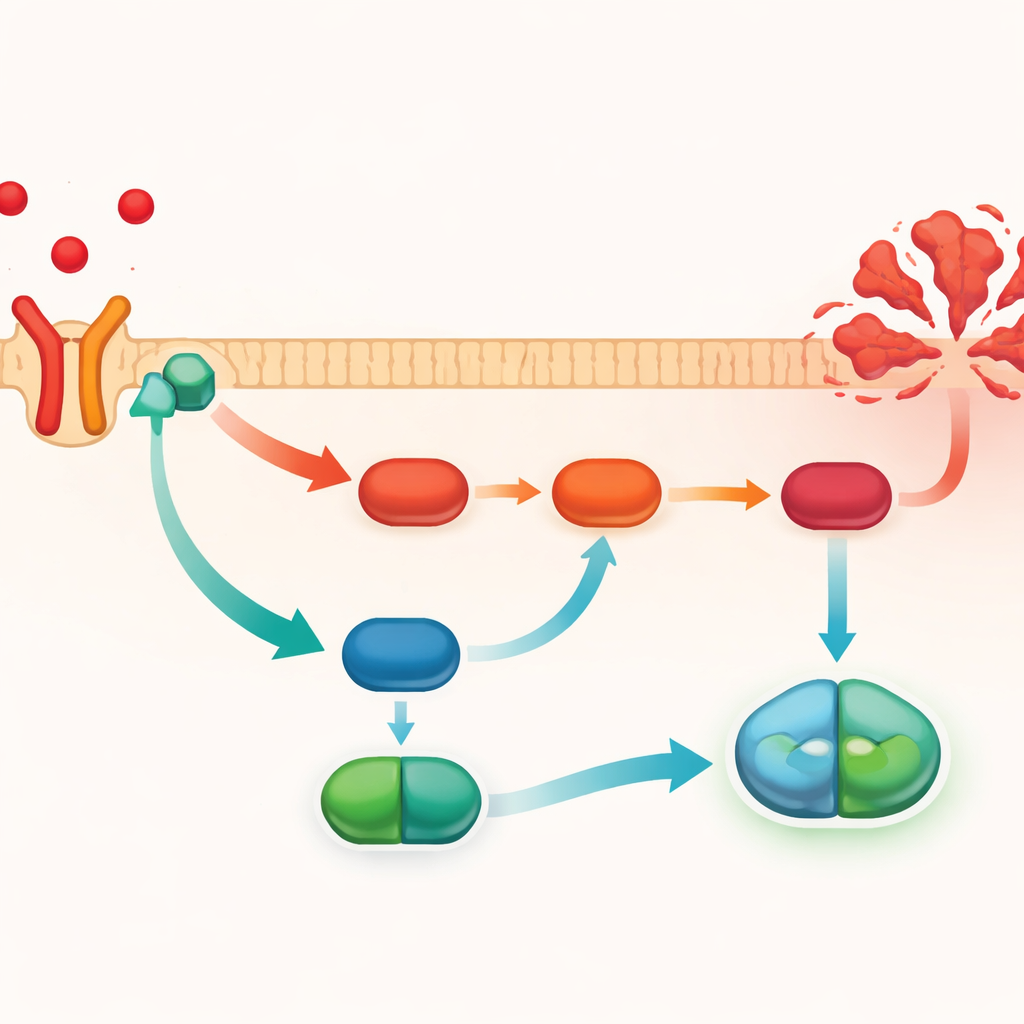
ما الذي قد يعنيه هذا للعلاجات المستقبلية
تجتمع النتائج لتصوغ صورة واضحة: يبدو أن PMG يحمي خلايا الكبد من الإصابة الالتهابية الحادة عن طريق حجب إشارة TNF-α عند مستقبلها وتهدئة مسار PI3K/AKT/NF-κB الذي كان سيدفع بدلاً من ذلك الالتهاب وموت الخلايا. رغم أن هذا العمل أُجري في فئران وخلايا مزروعة، فإنه يوفر أساسًا آليًا لمركب نباتي كمُرشح دوائي محتمَل لإصابة الكبد الحادة. هناك حاجة لدراسات إضافية لاختبار السلامة والجرعات وما إذا كانت فوائد مماثلة ستحدث لدى البشر، لكن الدراسة تبرز كيف يمكن للعلاجات التقليدية أن تلهم تدخلات حديثة مستهدفة لحماية أحد أهم أعضاء الجسم.
الاستشهاد: Hu, R., Chen, Z., Chen, T. et al. Physcion-8-O-β-D-monoglucoside protects hepatocytes from TNF-α-mediated apoptosis by suppressing the PI3K/AKT/NF-κB signaling pathway. Sci Rep 16, 12716 (2026). https://doi.org/10.1038/s41598-026-38701-6
الكلمات المفتاحية: إصابة الكبد الحادة, الالتهاب, عامل نخر الورم, الطب الصيني التقليدي, حماية الكبد