Clear Sky Science · zh
肿瘤全基因组测序在实体瘤临床中的现实价值
这对癌症患者为何重要
对于许多晚期癌症患者来说,治疗中最难的部分往往是判断某种药物是否真正可能带来益处。本研究考察了一种强大的检测方法——全基因组测序,它能够一次性读取肿瘤中几乎所有的DNA变异。研究者提出了一个简单但关键的问题:当这种检测在日常医院护理中使用时,是否真的会改变患者的治疗路径或结局?
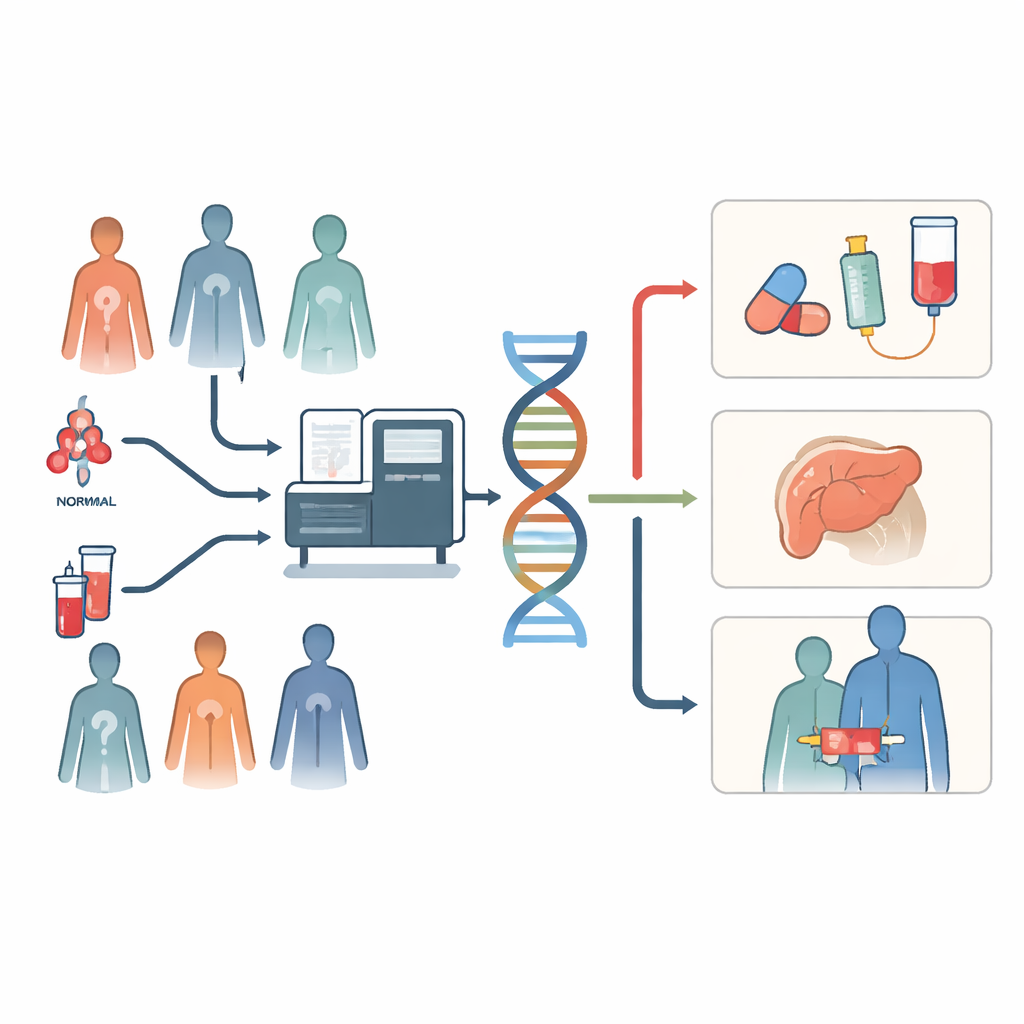
一次检测替代多次检测
传统的癌症检测常常像一场缓慢的接力赛。医生先下单做一项DNA检测,等结果出来后再做下一项,每项检测寻找可能对应特定药物的不同标志物。这种逐步进行的方法会消耗宝贵的肿瘤组织和时间。全基因组测序采取了不同策略:通过新鲜冷冻的肿瘤样本和一份血样,在一次运行中捕获几乎所有的DNA变异。这包括常见的药物靶点、复杂的重排、提示可能对免疫疗法敏感的特征以及可能影响家属的遗传风险变异。在荷兰,一家癌症中心将这种广泛的检测纳入了难治实体瘤患者的常规护理,并追踪后续的临床处理。
该检测在真实世界中的表现如何
研究团队回顾了2021年初至2022年底期间对全基因组测序的1,052份请求。在排除了肿瘤细胞或DNA含量不足的样本后,他们为723名患者的793份肿瘤样本获得了成功报告。大多数样本来自肺癌、原发灶不明的癌症和软组织肉瘤。周转时间足以支持临床决策:从样本到达测序实验室到医院收到报告,通常为六个工作日。基于DNA读数,专科医师记录了哪些肿瘤具有可指向现有或实验性治疗的特征,并在分子肿瘤委员会中登记了这些决策。
比常规模块检测发现更多治疗选项
在所有患者中,73%至少有一个可“行动”的DNA信号,可用于指导选择或避免某些治疗。约四分之一的患者携带与已作为标准护理报销的药物相关的标志物,而近三分之二的患者则有可能符合临床试验或早期使用计划的条件。当研究者通过数字模拟比较较小的靶向基因面板时,他们发现即使是一个较大的523基因面板,也会在大约十分之一的患者中错过重要线索,尤其是复杂的基因融合和一种称为同源重组缺陷的模式,该模式提示对某些药物敏感。全基因组测序还在约6.5%的患者中发现了临床相关的遗传性变异,其中一半此前未被既往的遗传检测发现。
为原发灶不明癌症破题并指导治疗
对原发灶不明的癌症患者而言,一个显著的好处出现了:医生能看到转移病灶却无法找到癌症原发部位。在这类病例中,63% 的情况下,基因组检测帮助确定了可能的起源组织或细化了诊断,常常使医生能够从含糊的“原发灶不明”方案转为更有针对性的、基于肿瘤类型的治疗。总体而言,41% 的受检患者因全基因组报告而产生了具体的临床后果:开始基于生物标志物的药物治疗、进入临床试验、获得修订或明确的诊断,或被转诊至遗传咨询。对于一些已有明确诊断的患者,检测甚至导致了癌症的重新分类或更精细的亚型划分,并带来了直接的治疗改变。
对生存期的影响
由于这不是一项随机对照试验,研究者无法断言因果关系,但可以进行组间比较。在肿瘤携带至少一个可行动标志物的患者中,那些在全基因组测序后实际接受基于标志物治疗的患者,从报告日起的中位生存期为405天,而未接受此类治疗的类似患者为309天——约增加了31%。当在任何系统性治疗开始之前就进行基因组检测时,这种获益最为明显:在该组中,接受指导性治疗的患者在四年时中位生存期尚未达到,明显长于未经基因组指导治疗或根本未接受系统性治疗的患者。相比之下,当测序被推迟到在一线或多线治疗之后进行时,这一生存优势在很大程度上消失了。
对未来的意义
对患者和临床医生而言,本研究表明在常规护理中读取整个肿瘤基因组不仅在技术上可行;它频繁改变诊断、开启个体化治疗的途径,并在早期使用时与更长的生存期相关。全基因组测序还构建了丰富的数据资源,可用于改进未来患者的癌症护理。作者认为,随着成本下降和数据系统的改进,这种广泛的DNA检测应成为精准肿瘤学的基石,而不是最后的选择。
引用: van Putten, J., Snaebjornsson, P., Bosch, L.J.W. et al. Real-world clinical utility of tumor whole-genome sequencing in solid cancers. Nat Med 32, 1286–1295 (2026). https://doi.org/10.1038/s41591-026-04280-2
关键词: 全基因组测序, 精准肿瘤学, 可作用生物标志物, 原发灶不明的癌症, 基于生物标志物的治疗