Clear Sky Science · pt
Utilidade clínica no mundo real do sequenciamento do genoma inteiro de tumores em cânceres sólidos
Por que isso importa para pessoas com câncer
Para muitas pessoas com câncer avançado, a parte mais difícil do tratamento é saber se um determinado medicamento tem realmente probabilidade de ajudar. Este estudo analisa um teste potente chamado sequenciamento do genoma inteiro, que lê quase todas as alterações no DNA do tumor de uma pessoa em uma única execução. Os pesquisadores fizeram uma pergunta simples, mas crucial: quando esse teste é usado no atendimento hospitalar cotidiano, ele realmente altera o curso dos pacientes?
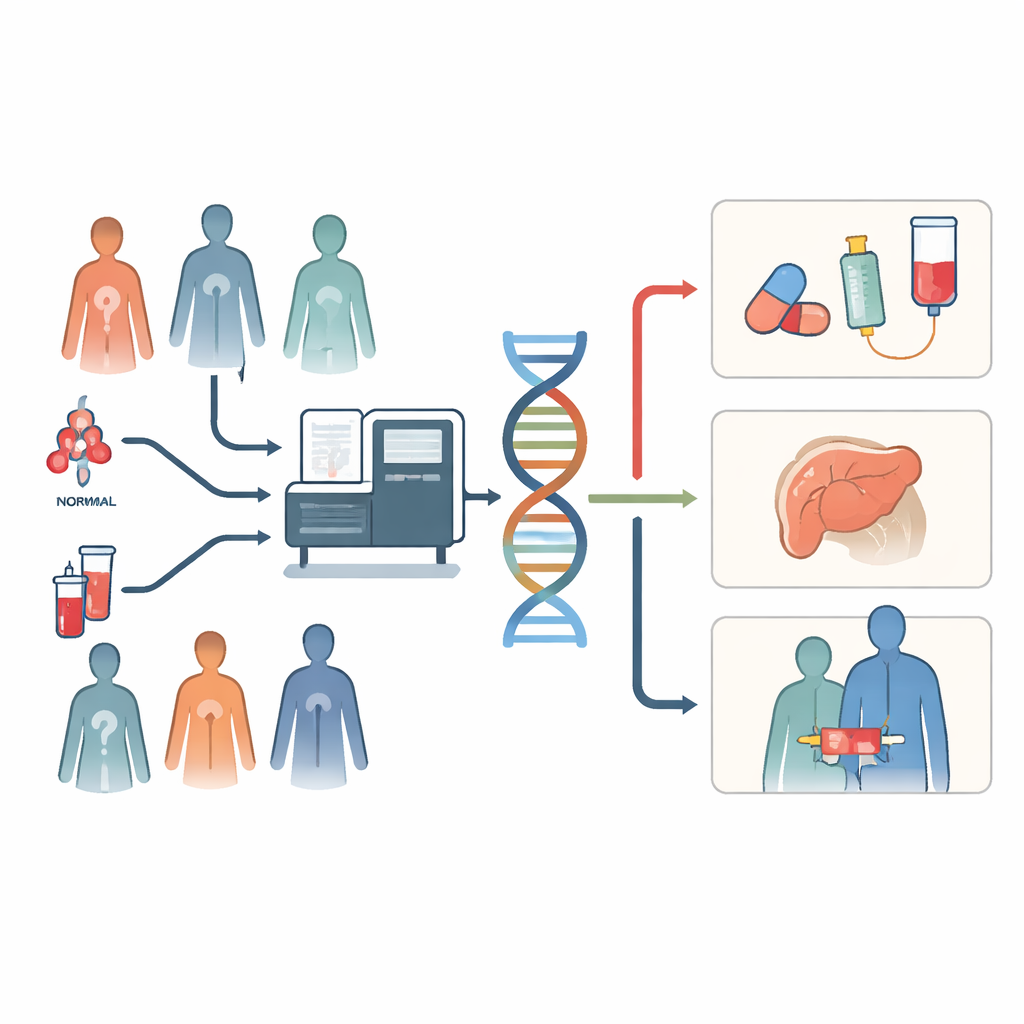
Um único teste em vez de muitos
Os testes tradicionais para câncer frequentemente funcionam como uma corrida de revezamento lenta. Os médicos solicitam um teste de DNA, aguardam o resultado e depois pedem outro, cada um procurando um marcador diferente que possa corresponder a um medicamento específico. Essa abordagem em etapas pode consumir tecido tumoral e tempo preciosos. O sequenciamento do genoma inteiro adota uma estratégia diferente: a partir de uma amostra de tumor fresca congelada e de uma amostra de sangue, ele captura quase todas as alterações do DNA em uma única rodada. Isso inclui alvos comuns de medicamentos, rearranjos complexos, sinais de que um tumor pode responder à imunoterapia e variantes de risco hereditário que podem ser relevantes para parentes. Nos Países Baixos, um centro de câncer incorporou esse teste amplo ao cuidado de rotina de pacientes com tumores sólidos de difícil tratamento e acompanhou o que aconteceu a seguir.
Como o teste funcionou na prática
A equipe revisou 1.052 solicitações de sequenciamento do genoma inteiro entre o início de 2021 e o final de 2022. Após excluir amostras sem células tumorais ou DNA suficientes, eles obtiveram relatórios bem-sucedidos para 793 amostras tumorais de 723 pacientes. A maioria das amostras veio de cânceres de pulmão, cânceres de primário desconhecido e sarcomas de tecidos moles. O tempo de resposta foi rápido o suficiente para decisões clínicas: tipicamente seis dias úteis desde a chegada da amostra ao laboratório de sequenciamento até o retorno do relatório ao hospital. Usando a leitura do DNA, especialistas catalogaram quais tumores apresentavam características que poderiam indicar tratamentos existentes ou experimentais e registraram essas decisões em um comitê molecular de tumor.
Encontrando mais opções do que painéis padrão
Em todos os pacientes, 73% apresentaram ao menos um sinal de DNA “acionável” que poderia orientar a seleção ou a evitação de terapias. Cerca de um quarto tinha marcadores vinculados a medicamentos já reembolsados como cuidado padrão, enquanto quase dois terços tinham marcadores que os tornavam elegíveis para ensaios clínicos ou programas de acesso precoce. Quando os pesquisadores simularam digitalmente o que teria sido detectado com painéis de genes menores e direcionados, descobriram que mesmo um grande painel de 523 genes teria perdido oportunidades importantes em aproximadamente um em cada dez pacientes, particularmente fusões gênicas complexas e um padrão chamado deficiência na recombinação homóloga, que aponta sensibilidade a certos medicamentos. O sequenciamento do genoma inteiro também revelou variantes hereditárias clinicamente relevantes em cerca de 6,5% dos pacientes, metade das quais não havia sido detectada por testes genéticos anteriores.
Resolvendo cânceres misteriosos e orientando o tratamento
Um benefício marcante surgiu para pessoas com cânceres de primário desconhecido, em que os médicos veem metástases, mas não conseguem localizar onde o câncer começou. Em 63% desses casos, o teste genômico ajudou a identificar um provável tecido de origem ou a refinar o diagnóstico, frequentemente permitindo que os médicos mudassem de esquemas vagos de “primário desconhecido” para tratamentos mais específicos por tipo tumoral. No total, 41% de todos os pacientes testados experimentaram uma consequência clínica concreta do relatório do genoma inteiro: iniciar um medicamento guiado por biomarcador, ingressar em um ensaio, receber um diagnóstico revisado ou clarificado, ou ser encaminhado para aconselhamento genético. Para alguns pacientes com diagnósticos estabelecidos, o teste levou até à reclassificação ou a um subtipo mais detalhado do câncer, com mudanças de tratamento diretas.
O que isso significou para a sobrevida
Como este não foi um ensaio randomizado, os pesquisadores não puderam provar causalidade, mas puderam comparar grupos. Entre pacientes cujos tumores apresentavam pelo menos um marcador acionável, aqueles que realmente receberam terapia informada pelo biomarcador após o sequenciamento do genoma inteiro viveram mediana de 405 dias após o relatório, contra 309 dias para pacientes semelhantes que não receberam esse tratamento—cerca de 31% a mais. O benefício foi mais pronunciado quando o teste genômico foi feito antes de qualquer terapia sistêmica: nesse grupo, a sobrevida dos pacientes que receberam tratamento guiado ainda não havia atingido a mediana aos quatro anos, claramente mais longa do que para aqueles tratados sem orientação genômica ou que não receberam tratamento sistêmico. Em contraste, quando o sequenciamento foi adiado até depois de uma ou mais linhas de tratamento, a vantagem em sobrevida praticamente desapareceu.
O que isso significa daqui para frente
Para pacientes e clínicos, este estudo mostra que ler todo o genoma tumoral no atendimento de rotina não é apenas tecnicamente viável; frequentemente altera diagnósticos, abre portas para tratamentos personalizados e está associado a maior sobrevida quando usado cedo. O sequenciamento do genoma inteiro também cria um rico recurso de dados que pode ajudar a aperfeiçoar o cuidado do câncer para pacientes futuros. Os autores argumentam que, à medida que os custos caem e os sistemas de dados melhoram, esse teste amplo de DNA deve se tornar uma pedra angular da oncologia de precisão, em vez de uma opção de último recurso.
Citação: van Putten, J., Snaebjornsson, P., Bosch, L.J.W. et al. Real-world clinical utility of tumor whole-genome sequencing in solid cancers. Nat Med 32, 1286–1295 (2026). https://doi.org/10.1038/s41591-026-04280-2
Palavras-chave: sequenciamento do genoma inteiro, oncologia de precisão, biomarcadores acionáveis, câncer de primário desconhecido, terapia guiada por biomarcador