Clear Sky Science · nl
Klinische bruikbaarheid in de praktijk van tumor-whole-genome sequencing bij solide tumoren
Waarom dit belangrijk is voor mensen met kanker
Voor veel mensen met vergevorderde kanker is het moeilijkste onderdeel van de behandeling te weten of een bepaald geneesmiddel daadwerkelijk waarschijnlijk zal helpen. Deze studie onderzoekt een krachtig onderzoek: whole-genome sequencing, dat bijna alle DNA-veranderingen in de tumor van een persoon in één keer uitleest. De onderzoekers stelden een eenvoudige maar cruciale vraag: verandert dit onderzoek, wanneer het in de dagelijkse ziekenhuispraktijk wordt gebruikt, daadwerkelijk wat er met patiënten gebeurt?
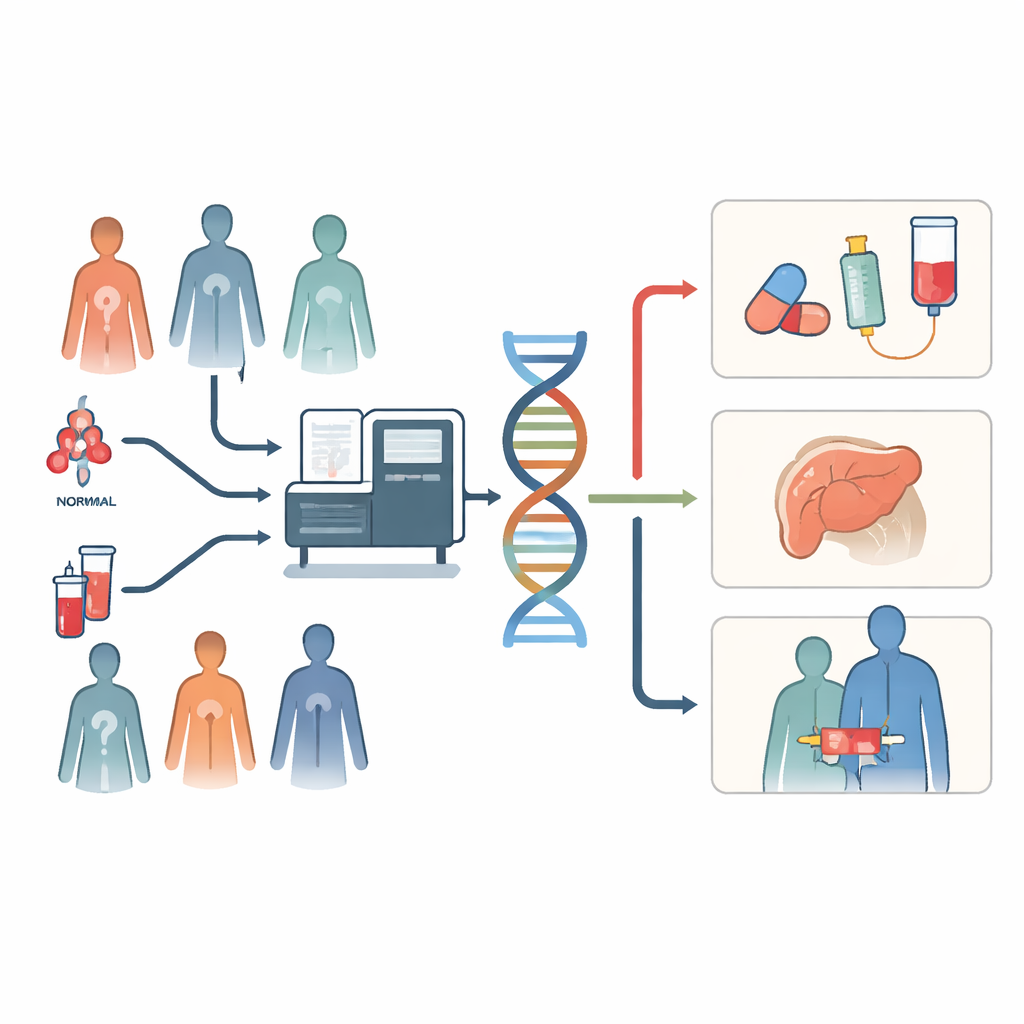
Één test in plaats van veel
Traditionele kankertests werken vaak als een trage estafette. Artsen vragen één DNA-test aan, wachten op het resultaat en vragen vervolgens een andere aan, waarbij elk onderzoek naar een andere marker zoekt die mogelijk past bij een specifiek geneesmiddel. Deze stapsgewijze aanpak kan kostbaar tumorweefsel en tijd verbruiken. Whole-genome sequencing pakt het anders aan: uit een vers ingevroren tumormonster en een bloedmonster legt het vrijwel alle DNA-veranderingen vast in één keer. Dat omvat veelvoorkomende doeltargets, complexe herschikkingen, aanwijzingen dat een tumor mogelijk op immunotherapie reageert, en erfelijke risicovarianten die relevant kunnen zijn voor familieleden. In Nederland maakte één kankercentrum deze brede test onderdeel van de routinematige zorg voor patiënten met moeilijk behandelbare solide tumoren en volgde wat er vervolgens gebeurde.
Hoe goed de test in de praktijk werkte
Het team beoordeelde 1.052 aanvragen voor whole-genome sequencing tussen begin 2021 en eind 2022. Na uitsluiting van monsters zonder voldoende tumorcellen of DNA verkregen ze succesvolle rapporten voor 793 tumormonsters van 723 patiënten. De meeste monsters kwamen uit longkankers, kankers van onbekende primaire oorsprong en weke delen sarcomen. De doorlooptijd was snel genoeg voor klinische beslissingen: doorgaans zes werkdagen vanaf aankomst van het monster in het sequencinglab tot een rapport terug in het ziekenhuis. Op basis van de DNA-uitslag noteerden specialisten welke tumoren kenmerken hadden die konden wijzen op bestaande of experimentele behandelingen en legden die beslissingen vast in een moleculair tumorboard.
Meer opties dan standaardpanelen
Over alle patiënten had 73% minstens één “actieerbaar” DNA-signaal dat de therapiekeuze of -vermijding kon sturen. Ongeveer een kwart had markers die gekoppeld zijn aan geneesmiddelen die al als standaardzorg worden vergoed, terwijl bijna twee derde markers had die hen in aanmerking zouden kunnen brengen voor klinische onderzoeken of vroege-toegangsprogramma’s. Toen de onderzoekers digitaal nabootsten wat met kleinere gerichte genpanelen gezien zou zijn, ontdekten ze dat zelfs een groot paneel van 523 genen belangrijke kansen bij ongeveer één op de tien patiënten zou hebben gemist, met name complexe genfusies en een patroon dat homologe recombinatiedeficiëntie genoemd wordt en wijst op gevoeligheid voor bepaalde geneesmiddelen. Whole-genome sequencing bracht ook klinisch relevante erfelijke varianten aan het licht bij circa 6,5% van de patiënten, waarvan de helft niet was ontdekt door eerdere genetische diagnostiek.
Het oplossen van mysterie-kankers en het sturen van behandeling
Een opvallend voordeel deed zich voor bij mensen met kankers van onbekende primaire oorsprong, waarbij artsen metastasen zien maar niet kunnen vaststellen waar de kanker is begonnen. In 63% van deze gevallen hielp de genoomtest een waarschijnlijke weefselherkomst vast te stellen of de diagnose aan te scherpen, waardoor artsen vaak konden overstappen van vage “unknown primary”-regimes naar meer op maat gemaakte, tumor-type-specifieke behandelingen. In totaal ondervond 41% van alle geteste patiënten een concreet klinisch gevolg van het whole-genome-rapport: het starten van een biomarker-gestuurd geneesmiddel, deelname aan een trial, het ontvangen van een herzien of verduidelijkt diagnose, of verwijzing naar genetische counseling. Voor sommige patiënten met een vastgestelde diagnose leidde de test zelfs tot herclassificatie of fijnere subtypering van hun kanker, met directe behandelwijzigingen tot gevolg.
Wat het voor overleving betekende
Aangezien dit geen gerandomiseerde studie was, konden de onderzoekers geen oorzaak en gevolg bewijzen, maar ze konden wel groepen vergelijken. Onder patiënten wier tumoren minstens één actieerbare marker droegen, leefden degenen die daadwerkelijk biomarker-geïnformeerde therapie ontvingen na whole-genome sequencing een mediaan van 405 dagen na het rapport, versus 309 dagen voor vergelijkbare patiënten die zo’n behandeling niet kregen—ongeveer een winst van 31%. Het voordeel was het duidelijkst wanneer de genoomtest werd gedaan vóór enige systemische therapie: in deze groep was de overleving voor patiënten die gerichte behandeling kregen na vier jaar nog niet tot een mediaan gedaald, duidelijk langer dan voor degenen die zonder genomische begeleiding werden behandeld of helemaal niet systemisch werden behandeld. Daarentegen verdween het overlevingsvoordeel grotendeels wanneer sequencing werd uitgesteld tot na één of meer behandelingslijnen.
Wat dit voor de toekomst betekent
Voor patiënten en clinici toont deze studie dat het uitlezen van het volledige tumorgenoom in de routinezorg niet alleen technisch uitvoerbaar is; het verandert vaak diagnoses, opent deuren naar gerichte behandelingen en hangt samen met langere overleving wanneer het vroeg wordt ingezet. Whole-genome sequencing bouwt ook een rijke databron op die kan helpen de kankerzorg voor toekomstige patiënten te verbeteren. De auteurs betogen dat nu de kosten dalen en datasystemen verbeteren, deze brede DNA-test een hoeksteen van precisie-oncologie zou moeten worden in plaats van een laatste redmiddel.
Bronvermelding: van Putten, J., Snaebjornsson, P., Bosch, L.J.W. et al. Real-world clinical utility of tumor whole-genome sequencing in solid cancers. Nat Med 32, 1286–1295 (2026). https://doi.org/10.1038/s41591-026-04280-2
Trefwoorden: genoomsequencing van het hele genoom, precisie-oncologie, actieerbare biomarkers, kanker van onbekende primaire locatie, biomarker-gestuurde therapie