Clear Sky Science · fr
Utilité clinique réelle du séquençage du génome tumoral complet dans les cancers solides
Pourquoi c’est important pour les personnes atteintes de cancer
Pour de nombreuses personnes atteintes d’un cancer avancé, la partie la plus difficile du traitement consiste à savoir si un médicament donné est réellement susceptible d’aider. Cette étude examine un test puissant appelé séquençage du génome complet, qui lit en une seule fois presque toutes les modifications de l’ADN d’une tumeur. Les chercheurs ont posé une question simple mais essentielle : lorsque ce test est utilisé dans la pratique hospitalière courante, modifie‑t‑il réellement le parcours des patients ?
Un test unique au lieu de plusieurs
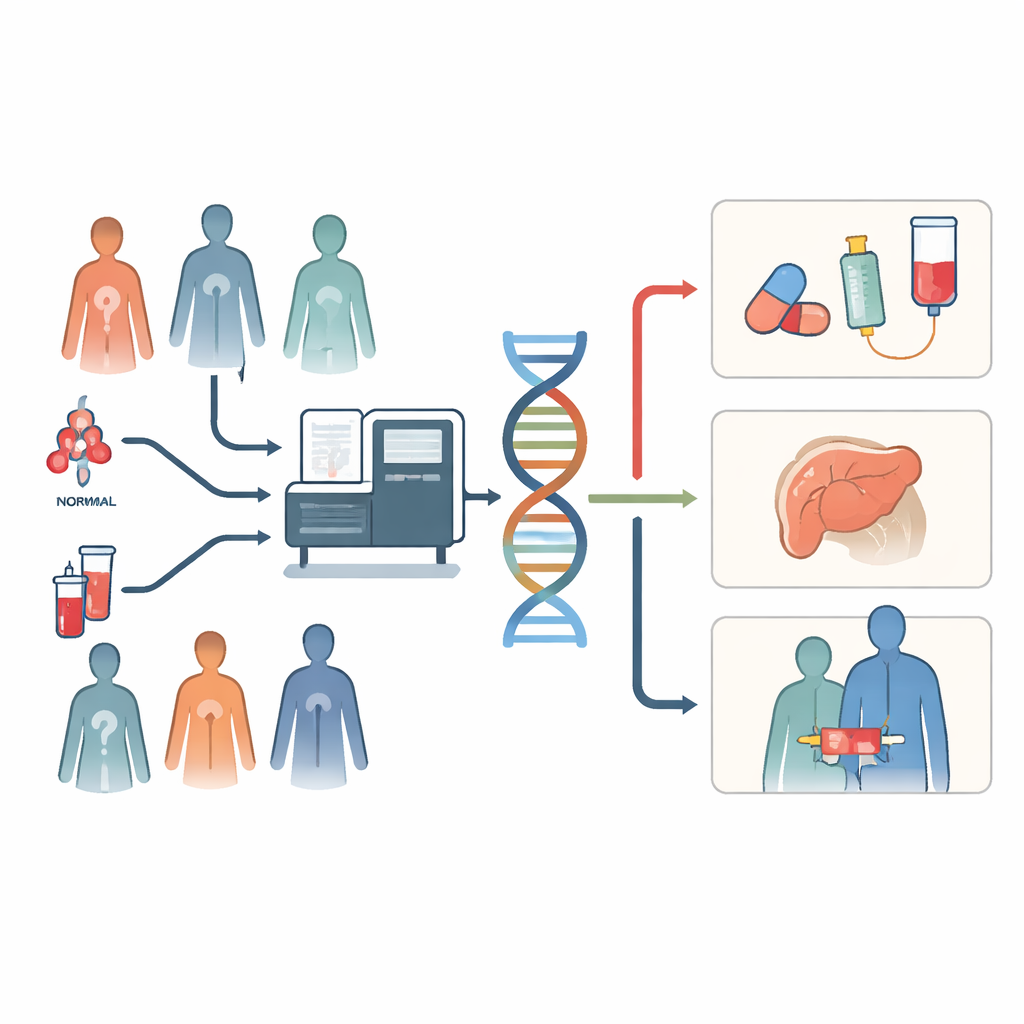
Les tests conventionnels du cancer fonctionnent souvent comme une course de relais lente. Les médecins prescrivent un test d’ADN, attendent le résultat, puis en prescrivent un autre, chacun recherchant un marqueur différent pouvant correspondre à un médicament spécifique. Cette approche par étapes peut épuiser un tissu tumoral précieux et prendre beaucoup de temps. Le séquençage du génome complet adopte une autre stratégie : à partir d’un échantillon tumoral congelé rapidement et d’un prélèvement sanguin, il capture presque toutes les altérations de l’ADN en une seule fois. Cela inclut les cibles médicamenteuses courantes, les réarrangements complexes, les signes que la tumeur pourrait répondre à l’immunothérapie, et les variants héréditaires pertinents pour les membres de la famille. Aux Pays‑Bas, un centre anticancer a intégré ce test étendu dans les soins de routine pour des patients atteints de tumeurs solides difficiles à traiter et a suivi les conséquences.
Comment le test a fonctionné en situation réelle
L’équipe a examiné 1 052 demandes de séquençage du génome complet entre début 2021 et fin 2022. Après exclusion des échantillons contenant trop peu de cellules tumorales ou d’ADN, ils ont obtenu des rapports exploitables pour 793 échantillons tumoraux provenant de 723 patients. La plupart des échantillons provenaient de cancers du poumon, de cancers d’origine primaire inconnue et de sarcomes des tissus mous. Les délais étaient suffisamment rapides pour guider des décisions cliniques : en général six jours ouvrables depuis l’arrivée de l’échantillon au laboratoire de séquençage jusqu’au rapport transmis à l’hôpital. À partir des lectures d’ADN, des spécialistes ont catalogué les tumeurs présentant des caractéristiques pouvant indiquer des traitements existants ou expérimentaux et ont consigné ces décisions dans un comité moléculaire de tumeurs.
Trouver plus d’options que les panels standards
Chez l’ensemble des patients, 73 % présentaient au moins un signal d’ADN « exploitable » pouvant orienter la sélection ou l’évitement d’un traitement. Environ un quart avaient des marqueurs associés à des médicaments déjà remboursés comme soins standard, tandis que près des deux tiers avaient des marqueurs les rendant éligibles à des essais cliniques ou à des programmes d’accès précoce. Lorsque les chercheurs ont simulé numériquement ce qui aurait été détecté avec des panels géniques ciblés plus petits, ils ont constaté que même un grand panel de 523 gènes aurait manqué des opportunités importantes chez environ un patient sur dix, en particulier des fusions géniques complexes et un profil appelé déficit de recombinaison homologue, qui signale une sensibilité à certains médicaments. Le séquençage du génome complet a également révélé des variants héréditaires d’intérêt clinique chez environ 6,5 % des patients, dont la moitié n’avaient pas été détectés par des tests génétiques antérieurs.
Résoudre les cancers « mystères » et orienter le traitement
Un bénéfice marquant est apparu pour les personnes atteintes de cancers d’origine primaire inconnue, où l’on observe des métastases sans pouvoir retrouver le site d’origine. Dans 63 % de ces cas, le test génomique a aidé à identifier un tissu d’origine probable ou à affiner le diagnostic, permettant souvent aux médecins de passer de schémas thérapeutiques vagues « d’origine inconnue » à des traitements plus ciblés, spécifiques au type de tumeur. Globalement, 41 % de tous les patients testés ont subi une conséquence clinique concrète liée au rapport de séquençage : démarrage d’un médicament guidé par un biomarqueur, inclusion dans un essai, diagnostic révisé ou précisé, ou orientation vers un conseil génétique. Pour certains patients avec des diagnostics établis, le test a même entraîné une reclassification ou un sous‑typage plus fin de leur cancer, avec des modifications de traitement directes.
Ce que cela a signifié pour la survie
Comme il ne s’agissait pas d’un essai randomisé, les chercheurs n’ont pas pu démontrer de causalité, mais ils ont pu comparer des groupes. Parmi les patients dont les tumeurs portaient au moins un marqueur exploitable, ceux qui ont effectivement reçu une thérapie guidée par le biomarqueur après le séquençage vivaient une médiane de 405 jours après le rapport, contre 309 jours pour des patients comparables qui n’ont pas reçu ce traitement — soit un gain d’environ 31 %. Le bénéfice était le plus net lorsque le test génomique était réalisé avant toute thérapie systémique : dans ce groupe, la survie des patients ayant reçu un traitement guidé n’avait pas encore atteint de médiane à quatre ans, clairement supérieure à celle des patients traités sans orientation génomique ou n’ayant pas reçu de traitement systémique. En revanche, lorsque le séquençage était retardé après une ou plusieurs lignes de traitement, l’avantage en survie disparaissait en grande partie.
Ce que cela implique pour l’avenir
Pour les patients et les cliniciens, cette étude montre que lire l’ensemble du génome tumoral en soins de routine n’est pas seulement techniquement faisable ; cela modifie fréquemment les diagnostics, ouvre l’accès à des traitements personnalisés et s’associe à une survie plus longue lorsqu’il est utilisé précocement. Le séquençage du génome complet constitue également une riche ressource de données pouvant aider à améliorer la prise en charge des futurs patients. Les auteurs soutiennent que, à mesure que les coûts diminuent et que les systèmes de données s’améliorent, ce test ADN étendu devrait devenir une pierre angulaire de l’oncologie de précision plutôt qu’une option de dernier recours.
Citation: van Putten, J., Snaebjornsson, P., Bosch, L.J.W. et al. Real-world clinical utility of tumor whole-genome sequencing in solid cancers. Nat Med 32, 1286–1295 (2026). https://doi.org/10.1038/s41591-026-04280-2
Mots-clés: séquençage du génome complet, oncologie de précision, biomarqueurs exploitables, cancer d’origine primaire inconnue, thérapie guidée par biomarqueurs