Clear Sky Science · zh
用于晚期实体肿瘤的PPARγ小分子逆激动剂:一期临床试验
为何对膀胱癌需要新方法
已发生远处转移的膀胱癌治疗非常困难。即便有现代免疫治疗和靶向药物,许多患者最终仍会出现疾病进展。本文介绍了一种名为FX-909口服药物的首个人体试验,该药旨在关闭许多膀胱癌细胞内的一个关键生长程序。对于关注癌症研究的人来说,它展示了一种新的肿瘤治疗思路:通过针对癌细胞的内部“身份”来改变其行为,而不仅仅是直接杀灭细胞。 
肿瘤细胞内部的隐秘开关
许多晚期膀胱癌属于所谓的发光型(luminal)肿瘤,与某些乳腺癌共享一套基因表达模式。这一模式的核心是名为PPARγ的蛋白,它像一个主控开关,帮助细胞表现得像正常的膀胱上皮。当该开关被过度激活时,癌细胞可能对其产生依赖,就像某些乳腺癌依赖雌激素信号、前列腺癌依赖雄激素一样。对数千例肿瘤的基因研究表明,发光型膀胱癌常带有使该开关过度激活的改变,这提示关闭它可能是一种强有力的减缓或缩小这些癌瘤的策略。
设计用以关闭开关的药物
早期阻断PPARγ的尝试效果有限,部分原因是那些药物更像简单的路障,阻止天然信号结合但未能真正沉默该通路。FX-909的设计有所不同。它是一种口服小分子,能够与PPARγ结合并将其锁定为一种高度抑制的构象。这种构象会吸引细胞内的天然“刹车”因子并阻止“油门”因子结合,即便在强烈促瘤信号存在下也能关闭PPARγ驱动的基因活性。对癌细胞和携带人源肿瘤的小鼠所做的实验表明,这种深度沉默可导致持久的肿瘤缩小,尤其在高度依赖PPARγ的癌症中更为明显。 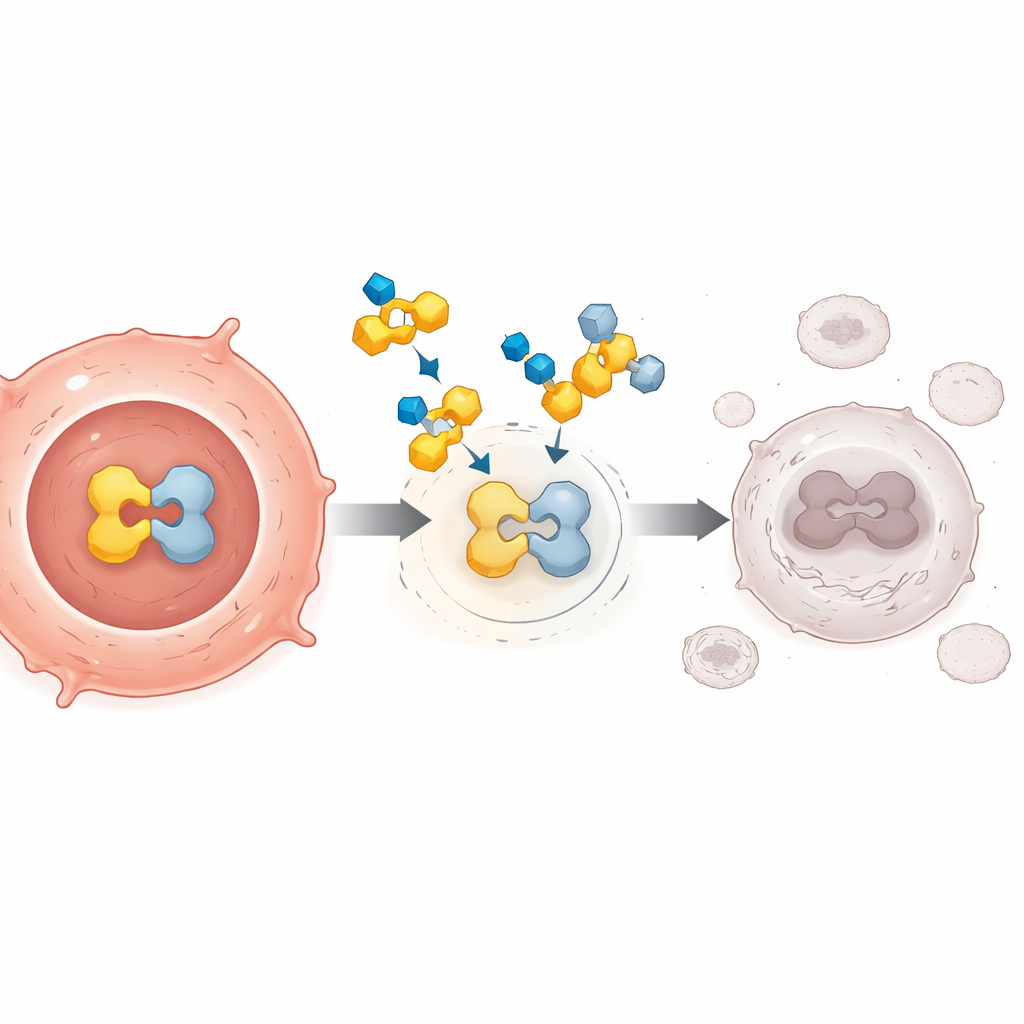
安全性评估与早期益处信号
这项1A期研究纳入了56名晚期实体肿瘤患者,其中包括46名已接受多线治疗的晚期尿路(膀胱及泌尿道)癌患者。志愿者每日口服30至100毫克不等剂量的FX-909,以28天为一循环重复给药。主要目标是评估安全性、确定适合后续研究的剂量范围并寻找药物对肿瘤影响的任何信号。总体而言,FX-909具有可控的安全性谱。几乎所有患者均出现某种副作用,但诸如红细胞减少、血小板减少、乏力和高血糖等严重问题通常可逆,且仅在较高剂量下更为常见。未有与药物相关的死亡。基于耐受性、血药浓度和生物学活性的综合评估,最终选定每日30毫克和50毫克为进一步研究的剂量。
谁最可能获益?
在可通过影像进行评估的晚期膀胱癌患者中,7名患者出现确诊的肿瘤缩小,包括1例完全缓解,许多其他患者则出现长期疾病稳定。值得注意的是,这些反应出现在所有剂量组,而非仅限于最高剂量。为了解谁获益最多,研究者分析了肿瘤样本中的发光程序标志物以及癌细胞核内PPARγ蛋白含量。他们开发了一种简单的染色检测,评估有多少比例的肿瘤细胞在细胞核中呈现PPARγ染色。若至少60%的细胞呈阳性,该肿瘤便被标注为“PPARγ-高”。在这一亚组中,大多数患者出现不同程度的肿瘤缩小,5例获得确诊反应,有些反应持续数月之久。
通过血液追踪肿瘤
研究团队还探索了一种基于血液的“液体活检”,跟踪循环血液中的肿瘤DNA片段。在有治疗前后血样的29名晚期膀胱癌患者中,超过一半在开始服用FX-909后出现肿瘤相关DNA的显著下降。这些分子学反应与影像学结果高度一致:血液肿瘤标志物下降的患者更有可能出现可见的肿瘤缩小。值得注意的是,这些分子学应答者大多也属于PPARγ-高肿瘤,进一步支持该生物标志物可用于筛选最可能从药物中获益的患者的观点。
这对未来治疗意味着什么
对普通读者来说,主要信息是FX-909代表了一类新的靶向疗法,它针对许多膀胱癌的核心“身份”程序。在这项早期试验中,药物在每日30或50毫克剂量下可安全给药,能够明确抑制患者体内的既定靶点,并在多线治疗失败的患者中显示出令人鼓舞的肿瘤控制信号。用于检测PPARγ的简单肿瘤染色检测为筛选适合的患者提供了一种可行方法。更大规模的正在进行的研究将评估FX-909与现有治疗相比的疗效,以及该策略是否可推广至其他具有相同过度活化生长开关的癌种。
引用: Galsky, M.D., Mantia, C., Bowden, M. et al. A small-molecule inverse agonist of PPARγ for advanced solid tumors: a phase 1 trial. Nat Med 32, 1249–1256 (2026). https://doi.org/10.1038/s41591-026-04263-3
关键词: 尿路上皮癌, PPARγ, 靶向疗法, FX-909, 一期临床试验