Clear Sky Science · pl
Małocząsteczkowy odwrócony agonista PPARγ dla zaawansowanych guzów litych: badanie fazy 1
Dlaczego nowe podejście do raka pęcherza ma znaczenie
Rak pęcherza, który rozprzestrzenił się po organizmie, jest wyjątkowo trudny w leczeniu. Nawet przy nowoczesnych immunoterapiach i lekach ukierunkowanych wielu pacjentów ostatecznie doświadcza progresji choroby. Artykuł opisuje pierwsze badanie u ludzi tabletki o nazwie FX-909, zaprojektowanej tak, by wyłączyć kluczowy program wzrostu w wielu komórkach raka pęcherza. Dla osób śledzących badania nad rakiem daje to wgląd w nowe podejście: zamiast jedynie próbować zabijać komórki nowotworowe, atakuje się ich wewnętrzną „tożsamość”. 
Ukryty przełącznik w komórkach guza
Wiele zaawansowanych raków pęcherza należy do grupy zwanej guzami luminalnymi, które wykazują wzór aktywności genów podobny do niektórych raków piersi. U podstaw tego wzoru leży białko zwane PPARγ, rodzaj głównego przełącznika pomagającego komórkom zachowywać się jak normalne komórki wyścielające pęcherz. Gdy ten przełącznik jest nadmiernie aktywowany, komórki nowotworowe mogą stać się od niego zależne, podobnie jak niektóre raki piersi zależą od sygnałów estrogenowych, a raki prostaty od androgenów. Badania genetyczne tysięcy guzów wykazały, że nowotwory luminalne pęcherza często noszą zmiany nadmiernie aktywujące ten przełącznik, co sugeruje, że jego wyłączenie mogłoby być skutecznym sposobem spowolnienia lub zmniejszenia tych nowotworów.
Projektowanie leku, który wyłącza przełącznik
Wcześniejsze próby blokowania PPARγ nie przynosiły dobrych rezultatów, częściowo dlatego, że działały jak proste zapory — uniemożliwiały wiązanie naturalnych sygnałów, ale nie potrafiły prawdziwie wyciszyć szlaku. FX-909 został zaprojektowany inaczej. To mała cząsteczka doustna, która przyczepia się do PPARγ w sposób blokujący jego aktywność, utrzymując białko w mocno represyjnym stanie. Ta zmieniona konformacja przyciąga naturalne „hamulce” w komórce i zapobiega przyłączaniu „akceleratorów”, wyłączając aktywność genów zależnych od PPARγ nawet przy silnych sygnałach sprzyjających guzowi. Doświadczenia na liniach komórkowych i u myszy z wszczepionymi ludzkimi guzami sugerowały, że takie głębokie wyciszenie może prowadzić do trwałego zmniejszenia guza, szczególnie w nowotworach silnie zależnych od PPARγ. 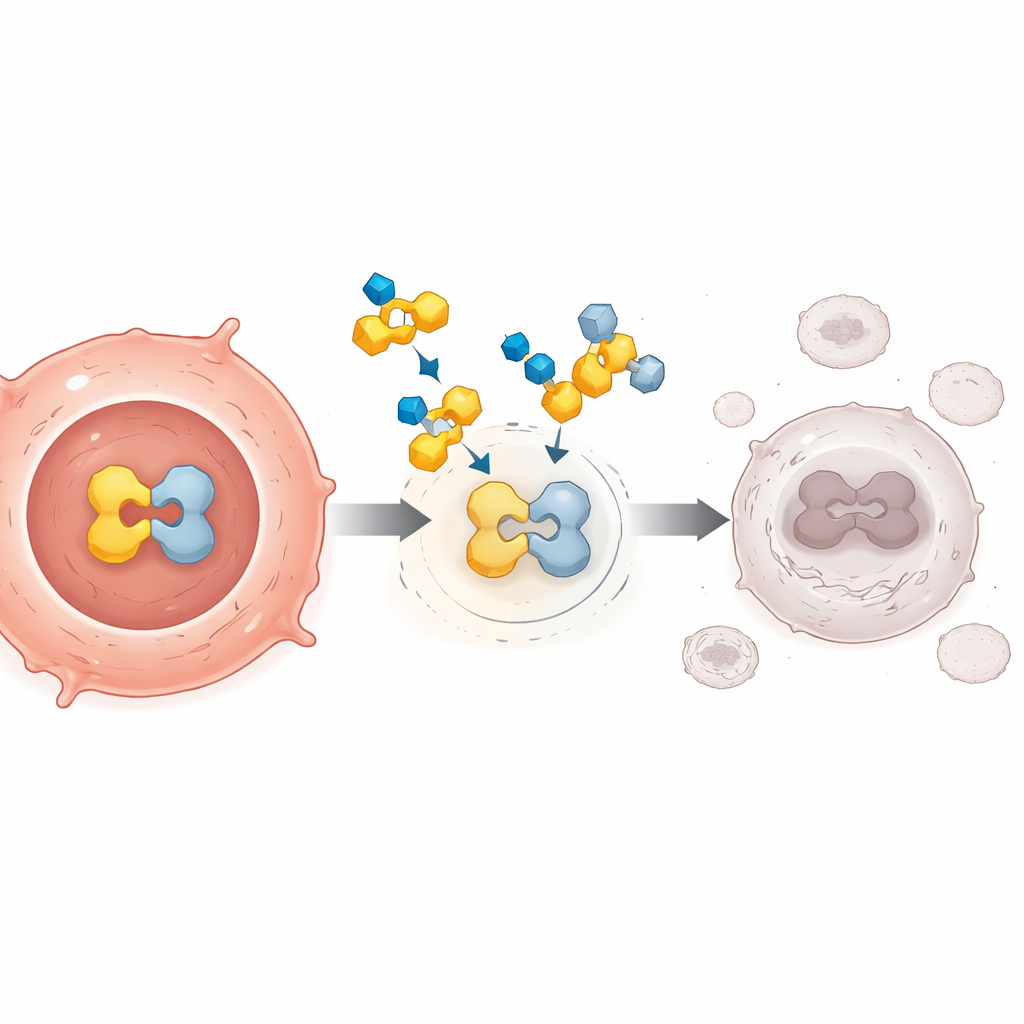
Ocena bezpieczeństwa i wczesne sygnały korzyści
Badanie fazy 1A objęło 56 osób z zaawansowanymi guzami litymi, w tym 46 z zaawansowanym rakiem urotelialnym (pęcherza i dróg moczowych), które wcześniej otrzymały kilka linii leczenia. Ochotnicy przyjmowali codzienne dawki FX-909 w zakresie od 30 do 100 miligramów w powtarzających się 28-dniowych cyklach. Główne cele to ocena bezpieczeństwa, ustalenie zakresów dawek nadających się do dalszych badań oraz poszukiwanie oznak wpływu leku na guzy. Ogólnie FX-909 wykazał akceptowalny profil bezpieczeństwa. Niemal wszyscy pacjenci doświadczyli pewnych działań niepożądanych, lecz poważne problemy, takie jak niedokrwistość, małopłytkowość, osłabienie i wysoki poziom cukru we krwi były zazwyczaj odwracalne i występowały częściej jedynie przy wyższych dawkach. Żadna śmierć nie została przypisana lekowi. Na podstawie bilansu tolerancji, stężeń leku we krwi i aktywności biologicznej wybrano do dalszych badań dawki 30 i 50 miligramów dziennie.
Kto wydaje się najbardziej prawdopodobny, by odnieść korzyść?
Wśród pacjentów z zaawansowanym rakiem pęcherza, u których guzy dało się zmierzyć w badaniach obrazowych, siedem osób doświadczyło potwierdzonego zmniejszenia guzów, w tym jedna całkowitej regresji, a wielu innych utrzymywało długotrwałą stabilizację choroby. Co ważne, odpowiedzi pojawiły się na wszystkich badanych dawkach, a nie tylko przy najwyższych. Aby określić, kto odniósł korzyść, badacze przeanalizowali próbki guza pod kątem markerów programu luminalnego oraz ilości białka PPARγ w jądrze komórek nowotworowych. Opracowali prosty test barwienia, który ocenia, jaki odsetek komórek guza wykazuje PPARγ w jądrze. Guzy, w których co najmniej 60% komórek barwiło się pozytywnie, oznaczono jako „PPARγ-wysokie”. W tej podgrupie większość pacjentów wykazała pewne zmniejszenie guza, a pięć osób miało potwierdzone odpowiedzi, niektóre trwające wiele miesięcy.
Śledzenie guzów we krwi
Zespół badał także „płynną biopsję” opartą na krążącym w osoczu DNA nowotworu. U 29 pacjentów z zaawansowanym rakiem pęcherza, którzy mieli próbki krwi przed leczeniem i podczas niego, ponad połowa wykazała wyraźny spadek markerów DNA związanego z guzem po rozpoczęciu FX-909. Te molekularne odpowiedzi dobrze korelowały z wynikami badań obrazowych: pacjenci, u których markery krążącego DNA spadły, znacznie częściej mieli widoczne zmniejszenie guzów. Co istotne, większość tych molekularnych responderów miała też guzy PPARγ-wysokie, co wzmacnia przekonanie, że ten biomarker może pomóc wybrać pacjentów najbardziej skłonnych do korzyści z leku.
Co to może znaczyć dla przyszłej opieki
Dla czytelnika nieprofesjonalnego kluczowy przekaz jest taki, że FX-909 reprezentuje nowy rodzaj terapii celowanej, która atakuje podstawowy program tożsamościowy w wielu rakach pęcherza. W tym wczesnym badaniu lek można było podawać bezpiecznie w dawkach 30 lub 50 miligramów dziennie, skutecznie wyłączał zamierzony cel u pacjentów i wykazał obiecujące sygnały kontroli guza u osób, których nowotwory oporne były na wielokrotne terapie. Prosty test barwienia guza na PPARγ oferuje praktyczny sposób identyfikacji tych pacjentów. Większe, trwające badania ustalą, jak skuteczny jest FX-909 w porównaniu z dostępnymi opcjami oraz czy tę strategię można rozszerzyć na inne nowotwory dzielące ten sam nadaktywny przełącznik wzrostu.
Cytowanie: Galsky, M.D., Mantia, C., Bowden, M. et al. A small-molecule inverse agonist of PPARγ for advanced solid tumors: a phase 1 trial. Nat Med 32, 1249–1256 (2026). https://doi.org/10.1038/s41591-026-04263-3
Słowa kluczowe: carcinoma urotelialne, PPAR gamma, terapia celowana, FX-909, badanie kliniczne fazy 1