Clear Sky Science · ar
مُناهِض عكسي صغير الجزيء لـ PPARγ للأورام الصلبة المتقدمة: تجربة المرحلة الأولى
لماذا نهج جديد لسرطان المثانة مهم
سرطان المثانة المنتشر في أنحاء الجسم يصعب علاجه بشدة. حتى مع العلاجات المناعية الحديثة والأدوية المستهدفة، كثير من المرضى يتقدم لديهم المرض في نهاية المطاف. تصف هذه المقالة التجربة البشرية الأولى لحبة تدعى FX-909، صُممت لإيقاف برنامج نمو رئيسي داخل العديد من خلايا سرطان المثانة. لمن يتابع أبحاث السرطان، تقدّم التجربة لمحة عن طريقة جديدة لمعالجة الأورام من خلال استهداف «هوية» الخلايا السرطانية الداخلية بدلاً من محاولة قتلها مباشرة فقط. 
مفتاح مخفي داخل خلايا الورم
ينتمي العديد من سرطانات المثانة المتقدمة إلى مجموعة تُدعى الأورام اللمعية (luminal)، التي تشترك في نمط نشاط جيني مع بعض أنواع سرطان الثدي. في قلب هذا النمط يوجد بروتين يُسمى PPARγ، وهو نوع من مفاتيح التحكم الرئيسية التي تساعد الخلايا على التصرف كأنسجة بطانة المثانة الطبيعية. عندما يصبح هذا المفتاح مفعَّلاً بشدة، قد تعتمد الخلايا السرطانية عليه للبقاء، على غرار اعتماد بعض سرطانات الثدي على إشارات الإستروجين أو سرطان البروستات على الهرمونات الذكرية. أظهرت دراسات جينية على آلاف الأورام أن سرطانات المثانة اللمعية غالباً ما تحمل تغييرات تفرط في تفعيل هذا المفتاح، مما يوحي بأن إيقافه قد يكون وسيلة قوية لإبطاء هذه السرطانات أو تقليصها.
تصميم دواء لقلب المفتاح وإيقافه
لم تنجح المحاولات السابقة لعرقلة PPARγ جيداً، جزئياً لأنها عملت كحواجز بسيطة تمنع الارتباطات الطبيعية لكنها فشلت في إسكات المسار فعلاً. صُمم FX-909 بطريقة مختلفة. إنه جزيء صغير يُؤخذ عن طريق الفم ويلتصق بـ PPARγ بطريقة تقبِله في حالة كبت شديدة. هذا الشكل المتغير يجذب «المكابح» الطبيعية داخل الخلية ويمنع ارتباط «المسرّعات»، فيُطفئ نشاط الجينات المُحرَّك بواسطة PPARγ حتى عندما توجد إشارات قوية محفزة للورم. أشارت تجارب على خلايا سرطان وفي فئران تُزرع فيها أورام بشرية إلى أن هذا الإغلاق العميق قد يُسبب تقلصاً مستداماً للأورام، لا سيما في السرطانات المعتمدة بشدة على PPARγ. 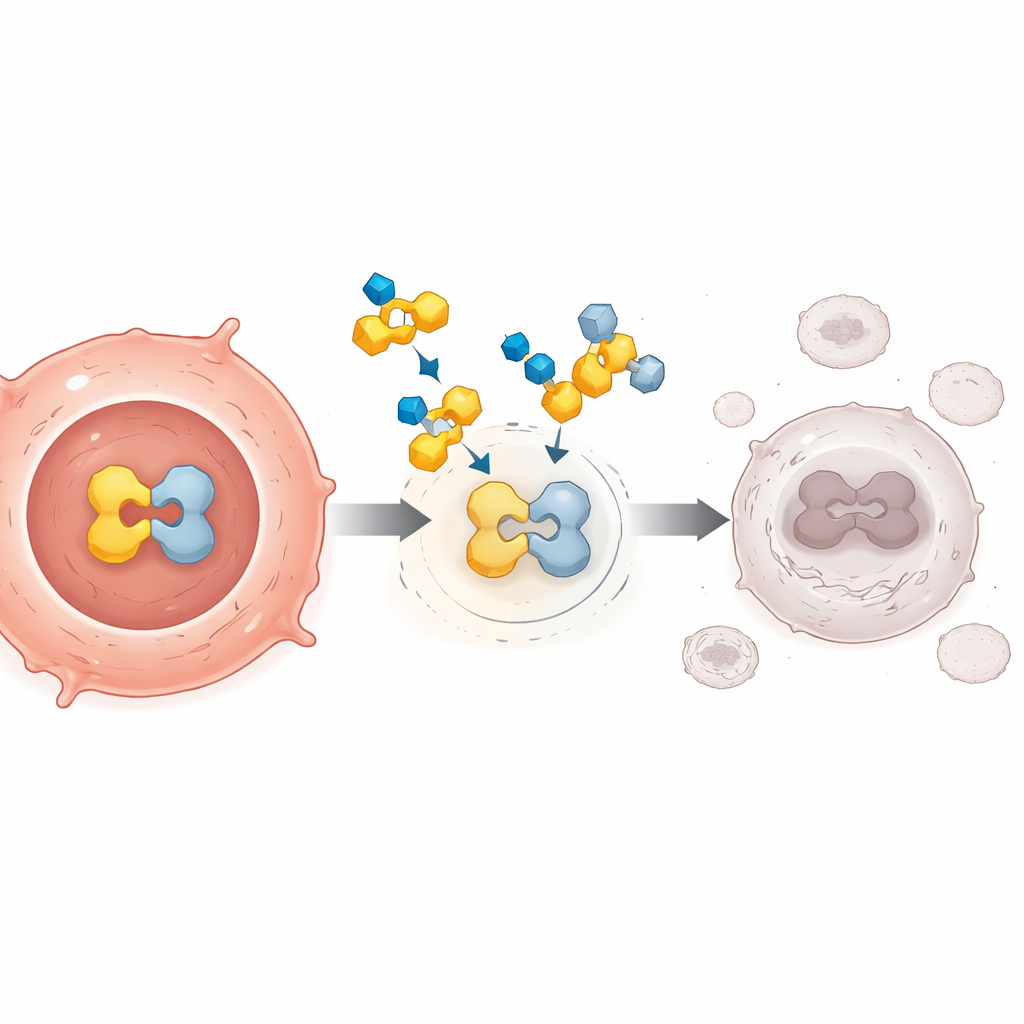
اختبار السلامة والدلائل المبكرة على الفائدة
سجلت دراسة المرحلة 1A ستة وخمسين شخصاً مصابين بأورام صلبة متقدمة، منهم 46 مريضاً بسرطان اليوذيال المتقدم (المثانة والمسالك البولية) الذين خضعوا بالفعل لعدة خطوط علاجية. تناول المتطوعون جرعات يومية من FX-909 تتراوح بين 30 و100 ملليغرام ضمن دورات متكررة مدتها 28 يوماً. كانت الأهداف الرئيسية تقييم السلامة، وتحديد نطاقات الجرعات المناسبة للاختبارات اللاحقة، والبحث عن أي إشارات أن الدواء يؤثر على الأورام. عموماً كان لملف سلامة FX-909 قابلية للتحمّل. عانى معظم المرضى آثاراً جانبية، لكن المشاكل الخطيرة مثل انخفاض خلايا الدم الحمراء، انخفاض الصفائح الدموية، التعب وارتفاع سكر الدم كانت قابلة للانعكاس عموماً وازدادت تواتراً فقط عند الجرعات الأعلى. لم تُعزَ أي وفيات إلى الدواء. بناءً على توازن التحمل ومستويات الدواء في الدم والنشاط البيولوجي، تم اختيار جرعتَي 30 و50 ملليغرام يومياً للدراسات اللاحقة.
من يبدو الأكثر استفادة؟
من بين المرضى المصابين بسرطان المثانة المتقدم الذين كانت أورامهم قابلة للقياس بالمسح، شهد سبعة انخفاضات مؤكدة في حجم الأورام، بما في ذلك حالة اختفاء كامل واحد، وكثيرون آخرون أظهروا استقراراً طويلاً للمرض. ومن المهم أن هذه الاستجابات ظهرت عند جميع مستويات الجرعات المختبرة وليس فقط عند أعلى الجرعات. لفهم من استفاد أكثر، حلل الباحثون عينات الأورام بحثاً عن علامات البرنامج اللمعي وعن كمية بروتين PPARγ الموجودة في نوى الخلايا السرطانية. طوروا اختباراً بسيطاً لصبغ يقيِّم نسبة الخلايا الورمية التي تظهر PPARγ في النواة. وصفت الأورام التي صبغت إيجابياً في 60% أو أكثر من الخلايا بأنها «عالية PPARγ». في هذه الشريحة، أظهر معظم المرضى بعض تقلصات الأورام، وخمسة منهم سجلوا استجابات مؤكدة، استمرت بعضُها لعدة أشهر.
تتبع الأورام عبر الدم
استكشف الفريق أيضاً «خزعة سائلة» قائمة على الدم تتعقّب شظايا من الحمض النووي الورمي المتداولة في مجرى الدم. لدى 29 مريضاً بسرطان المثانة المتقدم الذين أخذت لهم عينات دم قبل وأثناء العلاج، أظهر أكثر من نصفهم انخفاضات كبيرة في الحمض النووي المرتبط بالورم بعد بدء FX-909. توافقت هذه الاستجابات الجزيئية جيداً مع نتائج الأشعة: كان المرضى الذين انخفضت لديهم علامات الورم في الدم أكثر عرضة بكثير لأن يظهر لديهم تقلص مرئي للأورام. ومن الجدير بالذكر أن معظم هؤلاء المستجيبين جزيئياً كانوا أيضاً من حاملي أورام «عالية PPARγ»، مما يعزز فكرة أن هذا العلامة الحيوية يمكن أن تساعد في اختيار المرضى الأكثر احتمالاً للاستفادة من الدواء.
ما الذي قد يعنيه هذا للرعاية المستقبلية
للقارئ العام، الرسالة الأساسية أن FX-909 يمثل نوعاً جديداً من العلاجات المستهدفة التي تهاجم برنامج هوية أساسي داخل العديد من سرطانات المثانة. في هذه التجربة المبكرة، كان من الممكن إعطاء الدواء بأمان بجرعات يومية قدرها 30 أو 50 ملليغرام، وأوقف بوضوح هدفه المقصود في المرضى، وأظهر إشارات واعدة للتحكم في الأورام لدى أشخاص سبق أن قاوم سرطانهم عدة علاجات. اختبار الصبغ البسيط لـ PPARγ يقدم وسيلة عملية لتحديد هؤلاء المرضى. ستحدد دراسات أكبر جارية مدى فعالية FX-909 مقارنةً بالخيارات الحالية وما إذا كان يمكن توسيع هذه الاستراتيجية إلى سرطانات أخرى تشترك في نفس مفتاح النمو المفرط النشاط.
الاستشهاد: Galsky, M.D., Mantia, C., Bowden, M. et al. A small-molecule inverse agonist of PPARγ for advanced solid tumors: a phase 1 trial. Nat Med 32, 1249–1256 (2026). https://doi.org/10.1038/s41591-026-04263-3
الكلمات المفتاحية: سرطان اليوذيال, PPAR جاما, العلاج المستهدف, FX-909, تجربة سريرية مرحلة 1