Clear Sky Science · sv
En liten molekyl som invers agonist mot PPARγ för avancerade solida tumörer: en fas 1-studie
Varför en ny metod mot blåscancer spelar roll
Blåscancer som har spridit sig i kroppen är svår att behandla. Trots moderna immunterapier och riktade läkemedel förvärras sjukdomen ofta med tiden. Den här artikeln beskriver den första mänskliga prövningen av en tablett kallad FX-909, utvecklad för att stänga av ett centralt tillväxtprogram i många blåscancerceller. För den som följer cancerforskning ger det en inblick i ett nytt sätt att behandla tumörer genom att rikta in sig på cancercellernas inre ”identitet” snarare än att bara försöka döda dem direkt. 
En dold strömbrytare inne i tumörceller
Många avancerade blåscancerformer tillhör en grupp som kallas luminala tumörer, vilka delar ett genuttrycksmönster med vissa bröstcancerformer. I centrum för detta mönster finns ett protein kallat PPARγ, en slags huvudströmbrytare som hjälper celler att bete sig som normalt blåsslemhinnevävnad. När denna brytare är överaktiv kan cancerceller bli beroende av den för överlevnad, på samma sätt som vissa bröstcancerformer är beroende av östrogensignaler eller prostatacancer av manliga hormoner. Genetiska studier av tusentals tumörer har visat att luminala blåscancer ofta bär förändringar som överaktiverar denna brytare, vilket tyder på att dess inaktivering kan vara ett kraftfullt sätt att bromsa eller krympa dessa tumörer.
Att utforma ett läkemedel för att slå av brytaren
Tidigare försök att blockera PPARγ fungerade inte bra, delvis eftersom de agerade som enkla hinder: de förhindrade naturliga signaler från att binda men tystade inte vägen ordentligt. FX-909 är byggt annorlunda. Det är en liten molekyl som tas peroralt och som binder till PPARγ så att proteinet låses i ett starkt repressivt tillstånd. Denna förändrade form attraherar cellens naturliga ”bromsar” och hindrar ”gaspedaler” från att fästa, vilket stänger av PPARγ-drivet genuttryck även när starka tumörfrämjande signaler finns närvarande. Experiment i cancerceller och i möss med mänskliga tumörer föreslog att denna djupa nedstängning kan ge varaktig tumörkrympning, särskilt i cancerformer som är starkt beroende av PPARγ. 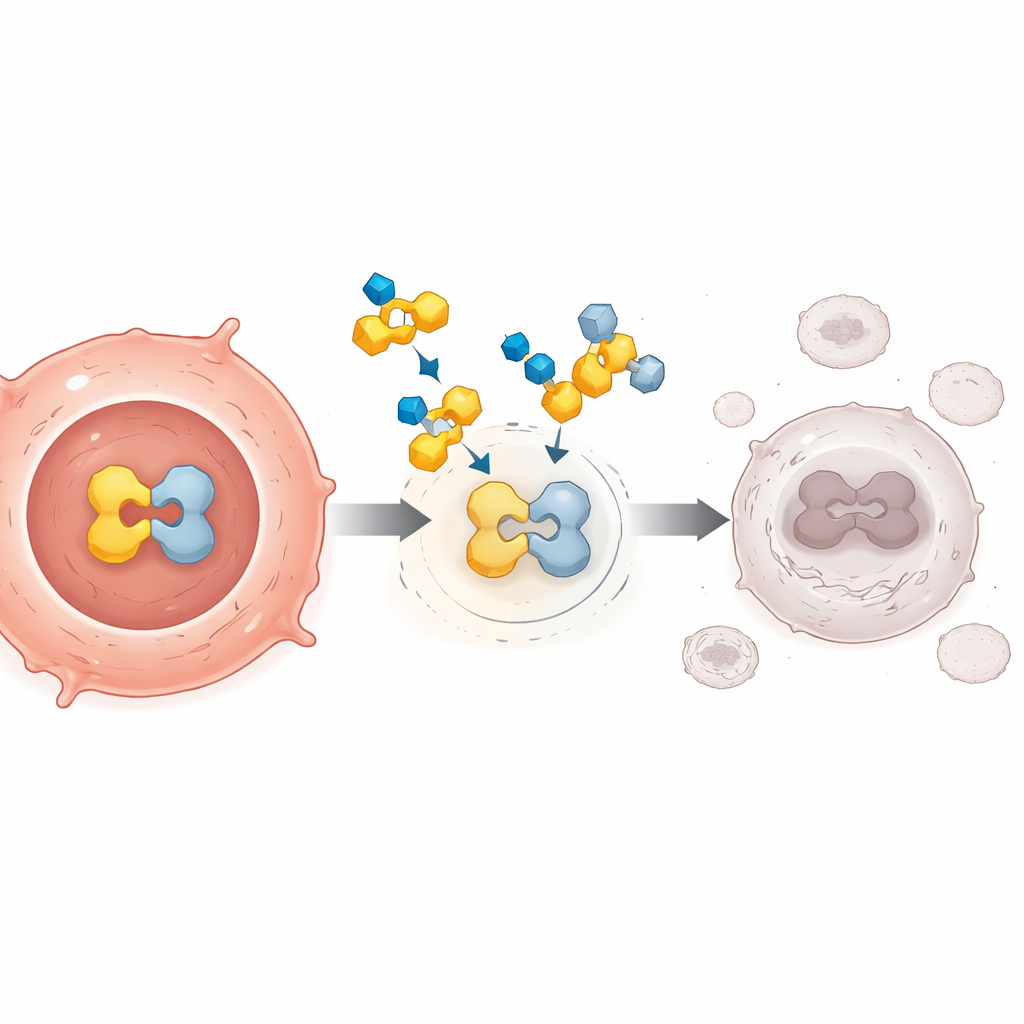
Testa säkerhet och tidiga tecken på nytta
Fas 1A-studien rekryterade 56 personer med avancerade solida tumörer, inklusive 46 med avancerad urotelial (blåsa och urinväg) cancer som redan fått flera behandlingslinjer. Deltagarna tog dagliga doser av FX-909 mellan 30 och 100 milligram i upprepade 28-dagarscykler. Huvudmålen var att bedöma säkerhet, hitta dosintervall för vidare prövning och att söka tecken på att läkemedlet påverkade tumörerna. Övergripande hade FX-909 en hanterbar säkerhetsprofil. Nästan alla patienter upplevde vissa biverkningar, men allvarliga problem såsom låga röda blodkroppar, låga blodplättar, trötthet och högt blodsocker var i regel reversibla och blev mer frekventa först vid högre doser. Inga dödsfall kunde tillskrivas läkemedlet. Baserat på tolerabilitet, läkemedelsnivåer i blodet och biologisk aktivitet valdes dagliga doser om 30 och 50 milligram för fortsatt studier.
Vem ser ut att ha störst nytta?
Bland patienter med avancerad blåscancer där tumörerna kunde mätas på röntgen upplevde sju bekräftad tumörkrympning, inklusive en fullständig försvinnande, och många andra hade långvarig sjukdomsstabilitet. Viktigt är att dessa svar visade sig vid alla testade dosnivåer och inte enbart vid de högsta doserna. För att förstå vem som drog mest nytta analyserade forskarna tumörprover för markörer för det luminala programmet och för mängden PPARγ-protein i cellkärnorna. De utvecklade ett enkelt färgningstest som skattar vilken andel av tumörcellerna som visar PPARγ i kärnan. Tumörer där minst 60 % av cellerna färgade positivt betecknades som ”PPARγ-höga”. I denna undergrupp visade de flesta patienter någon tumörkrympning, och fem hade bekräftade svar, några varande i många månader.
Att följa tumörer via blodet
Teamet undersökte också en blodbaserad ”liquid biopsy” som följer fragment av tumör-DNA i blodomloppet. Bland 29 patienter med avancerad blåscancer som hade blodprover före och under behandling visade mer än hälften markanta minskningar i tumörrelaterat DNA efter påbörjad behandling med FX-909. Dessa molekylära svar överensstämde väl med röntgenresultat: patienter vars blod-baserade tumörmarkörer föll var mycket mer benägna att uppvisa synlig tumörkrympning. Noterbart var att de flesta av dessa molekylära responderande också hade PPARγ-höga tumörer, vilket stärker idén att denna biomarkör kan hjälpa till att välja de patienter som mest sannolikt gynnats av läkemedlet.
Vad detta kan innebära för framtida vård
För en lekmannaläsare är huvudbudskapet att FX-909 representerar en ny typ av riktad terapi som angriper ett centralt identitetsprogram i många blåscancerformer. I denna tidiga prövning kunde läkemedlet ges säkert vid dagliga doser om 30 eller 50 milligram, det stängde tydligt av sitt avsedda mål i patienter och visade lovande tecken på tumörkontroll hos personer vars cancer redan motstått flera behandlingar. Det enkla tumörfärgningstestet för PPARγ erbjuder ett praktiskt sätt att hitta dessa patienter. Större, pågående studier kommer att avgöra hur väl FX-909 fungerar jämfört med befintliga alternativ och om denna strategi kan utsträckas till andra cancerformer som delar samma överaktiva tillväxtbrytare.
Citering: Galsky, M.D., Mantia, C., Bowden, M. et al. A small-molecule inverse agonist of PPARγ for advanced solid tumors: a phase 1 trial. Nat Med 32, 1249–1256 (2026). https://doi.org/10.1038/s41591-026-04263-3
Nyckelord: urotelialt karcinom, PPAR gamma, riktad terapi, FX-909, fas 1-klinisk prövning