Clear Sky Science · zh
POU1F1通过激活IL-6/JAK2/STAT3并富集ALDH,使乳腺癌细胞呈现癌症干细胞样特征
这项研究为何重要
许多乳腺癌患者对初始治疗反应良好,但仍面临多年后疾病复发或转移的风险。科学家越来越怀疑,一小部分格外顽固的肿瘤细胞,常被称为癌症干样细胞,能帮助肿瘤抵抗药物和放疗并播种新肿瘤。本研究探讨了乳腺癌细胞内的单一蛋白如何激活这些耐受性强的细胞,并指向了未来可能关闭该“开关”的方法。
肿瘤内部的隐秘“麻烦制造者”
并非所有癌细胞都相同。一小部分细胞表现得有点像干细胞,能够自我更新并在大多数细胞被消灭后启动新的肿瘤。在乳腺癌中,这些细胞常带有某些表面标志和一种称为ALDH的酶,帮助科学家识别它们。它们在体外能很好地形成微小悬浮球体,对化疗和放疗耐受,并在动物体内极易引发肿瘤。由于这些特性,它们被认为是导致复发和转移的主要嫌疑者。
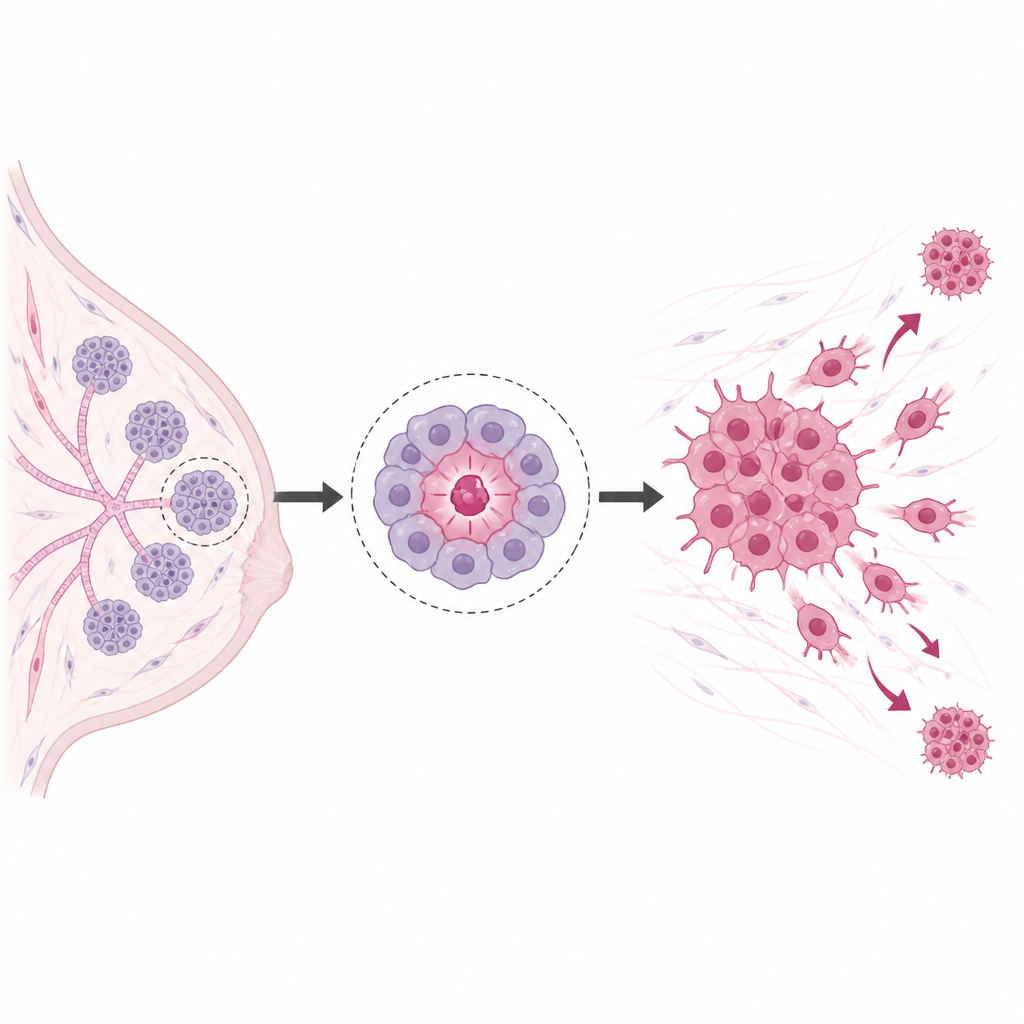
名为POU1F1的总控开关
研究者将注意力集中在名为POU1F1的基因上,该基因长期以来以其在垂体中的作用而闻名,但在乳腺肿瘤中也比正常乳腺组织表达更高。当他们促使常见的Luminal A型乳腺癌细胞额外产生POU1F1时,细胞发生了身份改变。它们丧失了与更成熟细胞相关的标志,获得了与干样行为相关的标志,包括ALDH活性的显著上升。细胞形成更多克隆,产生更致密的三维球体,并将能量代谢转向更依赖糖代谢的模式——这在侵袭性癌症中常见。当在另一种天然高表达该基因的乳腺癌细胞系中降低POU1F1水平时,这些干样特征则减弱或消失。
最危险的亚群
在被POU1F1增强的细胞中,研究团队进一步分离出一小群ALDH极高的细胞。该亚群在体外试验中更易迁移和侵袭,并在小鼠中更可能转移到肺、脑和肝等器官。当将极少量细胞注入免疫缺陷小鼠的乳腺组织时,高POU1F1且高ALDH的细胞比其他组更常形成肿瘤。这些肿瘤显示出更多的细胞增殖、更高水平的增殖标志物Ki67,以及与癌症干样行为相关的CD44标记更强的染色。总体而言,即便接受旨在模拟患者护理的激素治疗和放疗,携带这些细胞的小鼠寿命也更短。
助长抗药性的信号链
为弄清POU1F1如何驱动这种危险状态,研究者考察了POU1F1上调时哪些基因和通路被激活。他们发现一条炎症通路被强烈激活,涉及信号分子IL-6及其传导蛋白JAK2和STAT3。额外表达POU1F1的细胞分泌更多IL-6及相关信号,并表现出JAK2、STAT3及其他生长通路更高的活性。用抑制Janus激酶的药物或阻断IL-6受体的抗体阻断该通路,会降低ALDH水平并减少克隆形成和乳球体形成。简而言之,POU1F1似乎开启了一条由IL-6驱动的回路,进而建立并维持了对治疗有抵抗性的干样乳腺癌细胞群体。
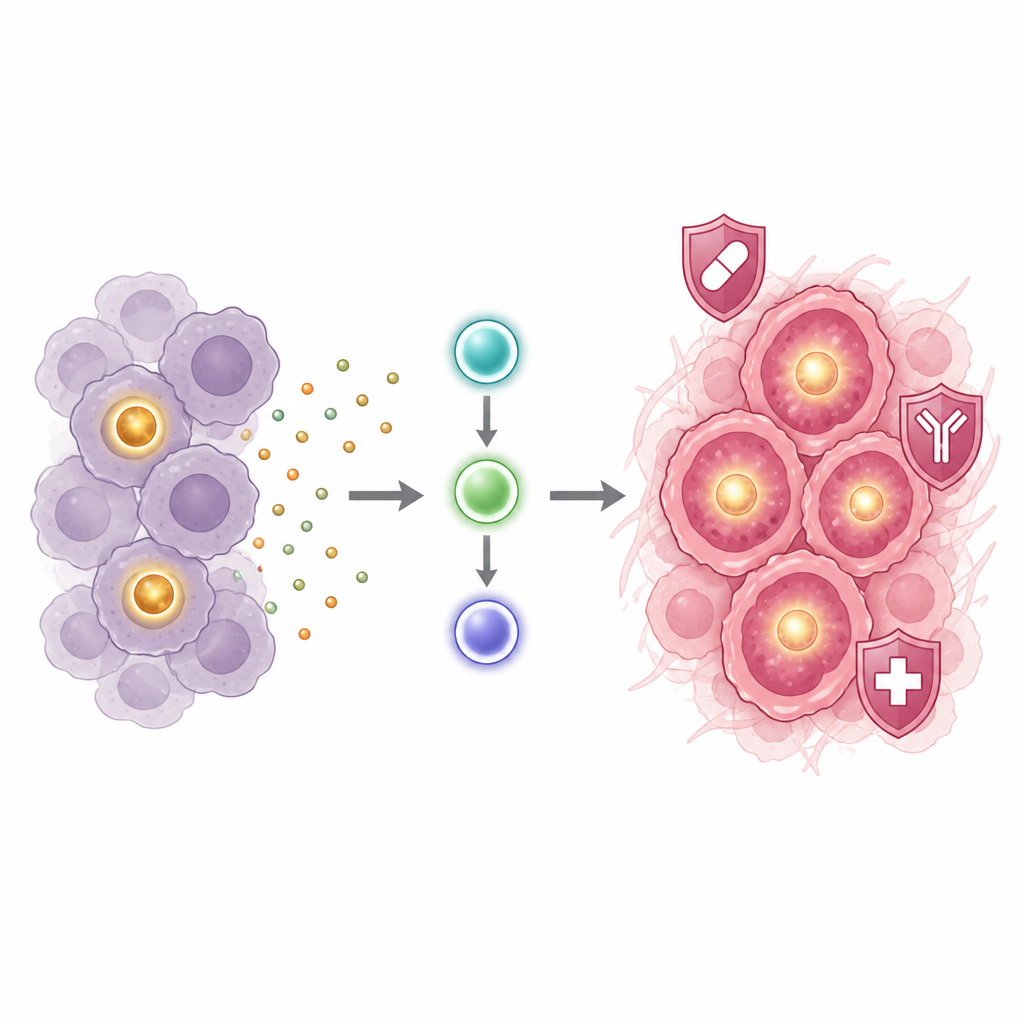
这对患者可能意味着什么
通过将POU1F1与一条已知的炎症信号通路以及富含ALDH的干样乳腺癌细胞的兴起联系起来,这项工作有助于解释为何高POU1F1和高ALDH的肿瘤与较差的患者预后相关。研究结果表明,在该蛋白丰富的肿瘤中,阻断IL-6 JAK2 STAT3通路的药物可能削弱最具韧性的癌细胞并降低复发风险。尽管还需更多研究和临床试验,但该研究描绘出从单一基因到治疗抵抗的清晰事件链,并指向已有的潜在药物靶点。
引用: Avila, L., Seoane, S., Rodriguez-Gonzalez, S. et al. POU1F1 induces cancer stem cell-like traits in breast cancer cells by IL-6/JAK2/STAT3 activation and enrichment of ALDH. npj Breast Cancer 12, 70 (2026). https://doi.org/10.1038/s41523-026-00929-w
关键词: 乳腺癌, 癌症干细胞, POU1F1, IL-6 JAK2 STAT3, ALDH1A1