Clear Sky Science · fr
POU1F1 induit des caractéristiques de cellules souches cancéreuses dans les cellules du cancer du sein par activation IL-6/JAK2/STAT3 et enrichissement en ALDH
Pourquoi cette recherche est importante
Beaucoup de patientes atteintes de cancer du sein répondent bien au traitement initial mais conservent un risque que la maladie réapparaisse ou se propage des années plus tard. Les scientifiques pensent de plus en plus qu’un petit groupe de cellules tumorales particulièrement tenaces, parfois appelées cellules de type souche cancéreuses, aide les cancers à survivre aux médicaments et aux rayonnements et à initier de nouvelles tumeurs. Cette étude explore comment une seule protéine à l’intérieur des cellules du cancer du sein peut activer ces cellules résistantes et indique une voie que les médecins pourraient un jour essayer d’éteindre.
Les fauteurs de trouble cachés dans les tumeurs
Toutes les cellules cancéreuses ne sont pas égales. Une minorité se comporte un peu comme des cellules souches, capable de se renouveler et de lancer de nouvelles tumeurs après que la plupart des autres cellules ont été éliminées. Dans le cancer du sein, ces cellules portent souvent une certaine combinaison de marqueurs de surface et une enzyme appelée ALDH qui aide les chercheurs à les repérer. Elles prolifèrent bien sous forme de petites sphères flottantes en laboratoire, résistent à la chimiothérapie et à la radiothérapie, et sont très efficaces pour initier des tumeurs chez l’animal. À cause de ces caractéristiques, elles sont des suspects privilégiés derrière les récidives et les métastases.
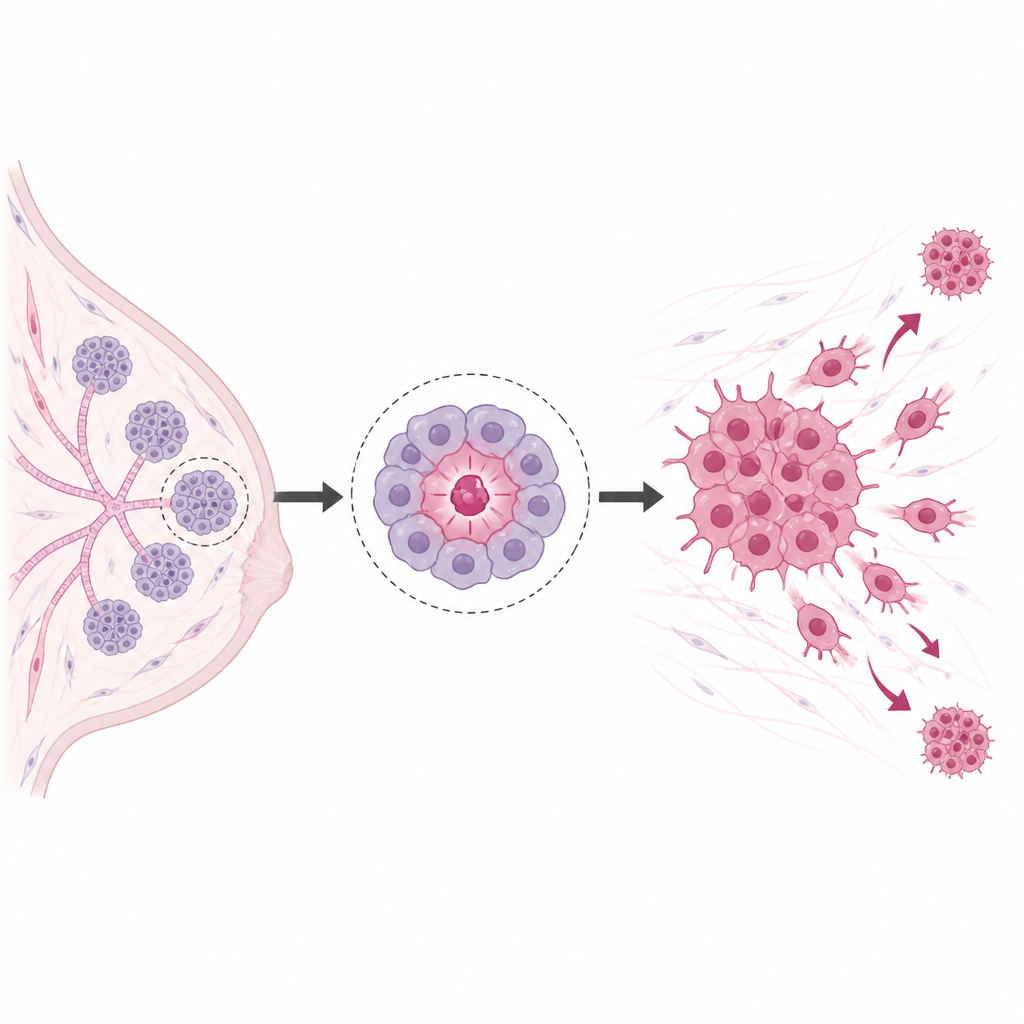
Un interrupteur maître nommé POU1F1
Les chercheurs se sont concentrés sur un gène nommé POU1F1, longtemps connu pour son rôle dans l’hypophyse mais également exprimé à des niveaux plus élevés dans les tumeurs mammaires que dans le tissu mammaire normal. Lorsqu’ils ont contraint des cellules de cancer du sein de type luminal A à produire davantage de POU1F1, les cellules ont changé d’identité. Elles ont perdu des marqueurs associés aux cellules plus matures et acquis des marqueurs liés au comportement de type souche, y compris une forte augmentation de l’activité d’ALDH. Les cellules ont formé davantage de colonies, produit des sphères tridimensionnelles plus denses et modifié leur métabolisme vers une utilisation accrue du glucose, un schéma souvent observé dans les cancers agressifs. Quand les niveaux de POU1F1 ont été réduits dans une autre lignée de cancer du sein qui en exprime naturellement beaucoup, ces traits de type souche ont diminué.
La sous‑population la plus dangereuse
Parmi les cellules enrichies en POU1F1, l’équipe a ensuite isolé un plus petit groupe présentant une activité d’ALDH particulièrement élevée. Cette sous‑population migré et envahi plus facilement dans des tests in vitro et avait une propension accrue à se disséminer vers des organes tels que le poumon, le cerveau et le foie chez la souris. Lorsqu’un très petit nombre de cellules a été injecté dans le tissu mammaire de souris immunodéficientes, celles exprimant des niveaux élevés de POU1F1 et d’ALDH ont formé des tumeurs beaucoup plus souvent que les autres groupes. Ces tumeurs présentaient une division cellulaire plus importante, des niveaux plus élevés d’un marqueur de prolifération appelé Ki67, et une coloration plus intense du marqueur CD44 associé au comportement de type souche cancéreuse. Globalement, les souris porteuses de ces cellules ont vécu moins longtemps, même lorsqu’elles ont reçu un traitement hormonal et une radiothérapie visant à imiter la prise en charge des patientes.
Une chaîne de signalisation qui alimente la résistance
Pour comprendre comment POU1F1 induit cet état dangereux, les chercheurs ont examiné quels gènes et quelles voies s’activent lorsque les niveaux de POU1F1 augmentent. Ils ont trouvé une forte activation d’une voie inflammatoire impliquant le signal IL‑6 et les protéines relais JAK2 et STAT3. Les cellules surexprimant POU1F1 sécrétaient davantage d’IL‑6 et de signaux associés, et présentaient une activité accrue de JAK2, STAT3 et d’autres voies de croissance. Bloquer cette chaîne avec des médicaments inhibiteurs des kinases Janus, ou avec un anticorps bloquant le récepteur de l’IL‑6, réduisait les niveaux d’ALDH et diminuait la formation de colonies et de mammosphères. En termes simples, POU1F1 semble activer un circuit piloté par l’IL‑6 qui, à son tour, crée et maintient le réservoir de cellules cancéreuses mammaires de type souche résistantes au traitement.
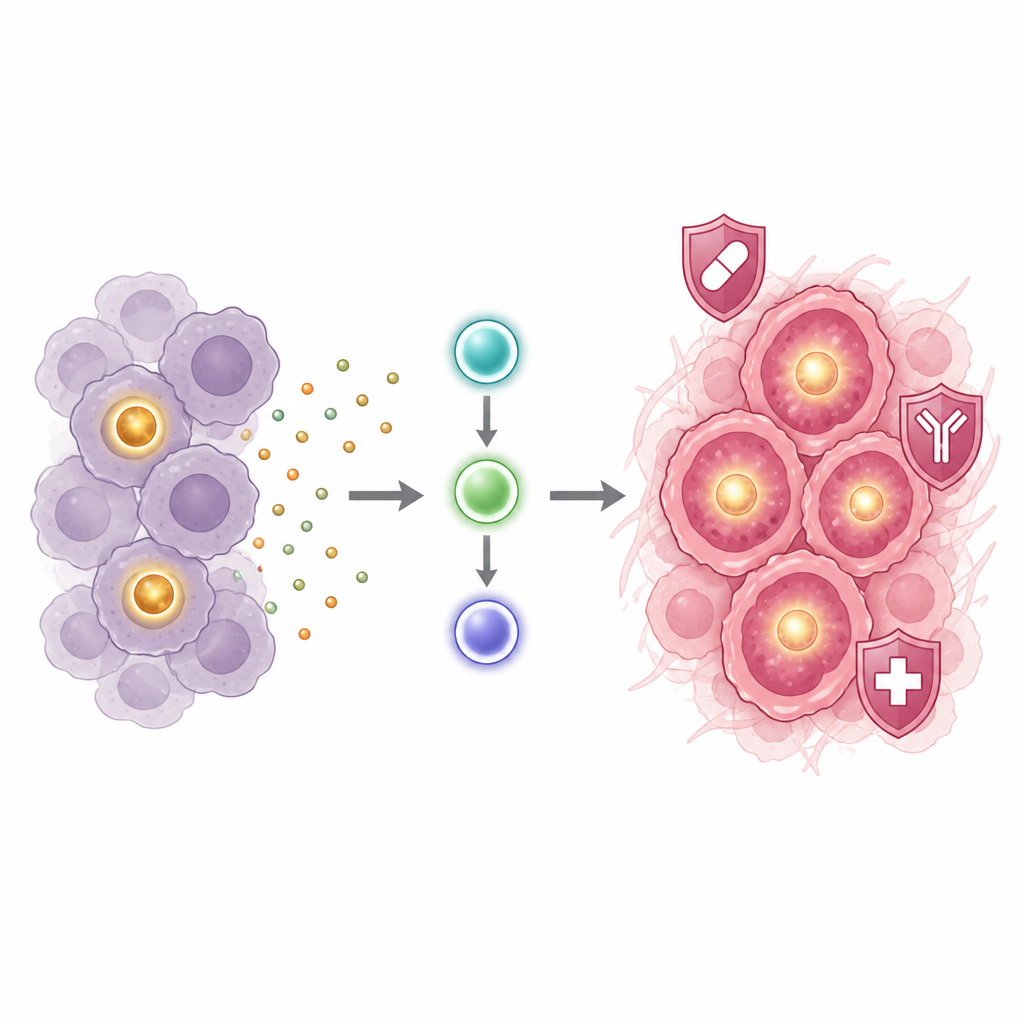
Ce que cela pourrait signifier pour les patientes
En reliant POU1F1 à une voie de signalisation inflammatoire bien connue et à l’augmentation des cellules mammaires de type souche riches en ALDH, ce travail aide à expliquer pourquoi les tumeurs à forte expression de POU1F1 et d’ALDH sont associées à de moins bons résultats pour les patientes. Les résultats suggèrent que, dans les tumeurs où cette protéine est abondante, des médicaments bloquant la voie IL‑6 JAK2 STAT3 pourraient affaiblir les cellules cancéreuses les plus résilientes et réduire le risque de récidive. Bien que des recherches supplémentaires et des essais cliniques soient nécessaires, l’étude cartographie une chaîne d’événements claire reliant un gène unique à la résistance au traitement et pointe vers des cibles médicamenteuses déjà existantes.
Citation: Avila, L., Seoane, S., Rodriguez-Gonzalez, S. et al. POU1F1 induces cancer stem cell-like traits in breast cancer cells by IL-6/JAK2/STAT3 activation and enrichment of ALDH. npj Breast Cancer 12, 70 (2026). https://doi.org/10.1038/s41523-026-00929-w
Mots-clés: cancer du sein, cellules souches cancéreuses, POU1F1, IL-6 JAK2 STAT3, ALDH1A1