Clear Sky Science · de
POU1F1 induziert krebsstammzellähnliche Eigenschaften in Brustkrebszellen durch Aktivierung von IL-6/JAK2/STAT3 und Anreicherung von ALDH
Warum diese Forschung wichtig ist
Viele Brustkrebspatientinnen und -patienten sprechen zunächst gut auf die Behandlung an, bleiben aber in Gefahr, dass die Krankheit Jahre später zurückkehrt oder streut. Wissenschaftler vermuten zunehmend, dass eine kleine Gruppe besonders hartnäckiger Tumorzellen, oft als krebsstammzellähnliche Zellen bezeichnet, Krebsereignisse übersteht, Therapien widersteht und neue Tumoren aussät. Diese Studie untersucht, wie ein einzelnes Protein in Brustkrebszellen jene widerstandsfähigen Zellen aktivieren kann, und zeigt einen Ansatz auf, mit dem man diesen Schalter künftig abschalten könnte.
Die verborgenen Übeltäter in Tumoren
Nicht alle Krebszellen sind gleich. Eine Minderheit verhält sich ein Stück weit wie Stammzellen: Sie kann sich selbst erneuern und neue Tumoren starten, nachdem die meisten anderen Zellen beseitigt wurden. Bei Brustkrebs tragen diese Zellen häufig eine bestimmte Kombination von Oberflächenmarkern sowie das Enzym ALDH, was Forschern hilft, sie zu identifizieren. Im Labor wachsen sie gut als kleine schwebende Kugelkolonien (Mammosphären), widerstehen Chemo‑ und Strahlentherapie und sind sehr effektiv beim Auslösen von Tumoren in Tieren. Wegen dieser Eigenschaften gelten sie als Hauptverdächtige hinter Rückfällen und Metastasen.
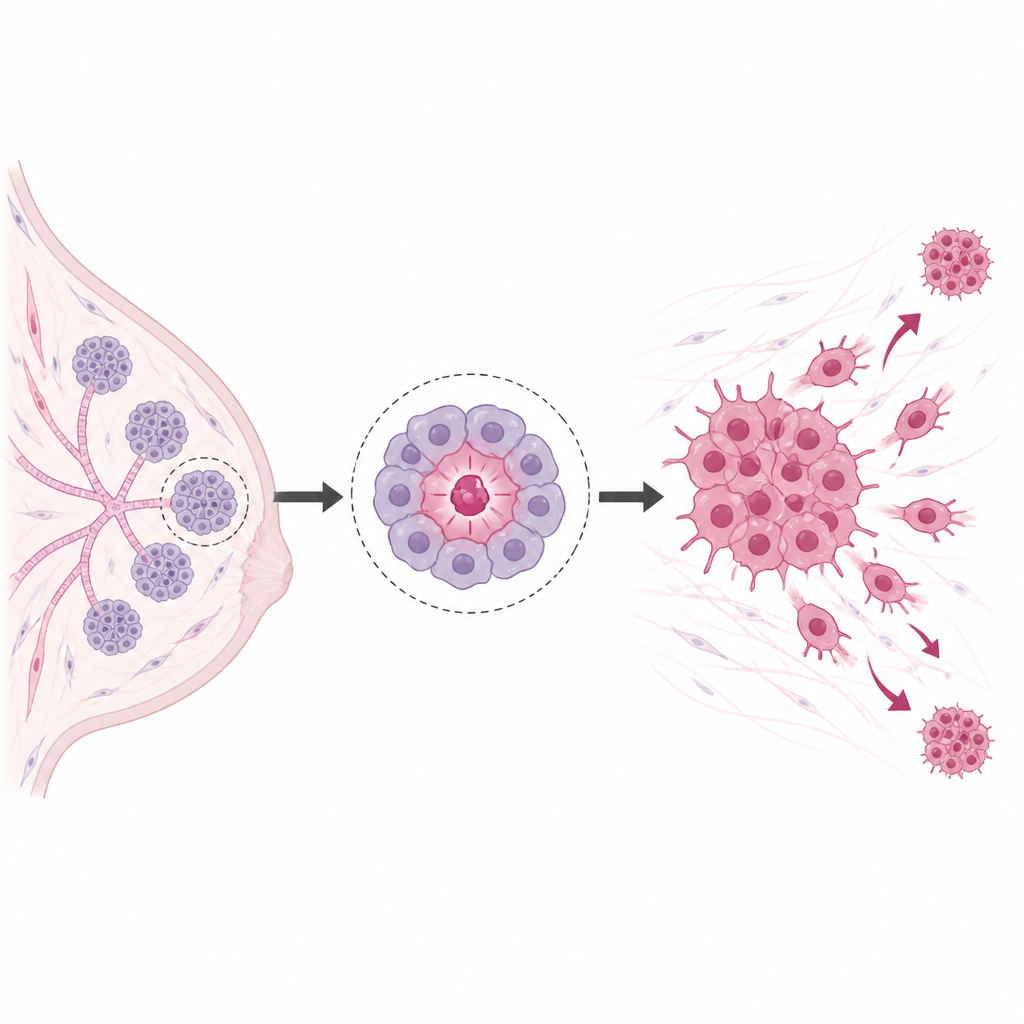
Ein Hauptschalter namens POU1F1
Die Forschenden konzentrierten sich auf ein Gen namens POU1F1, das zwar lange für seine Rolle in der Hypophyse bekannt war, aber in Brusttumoren höher exprimiert vorkommt als im normalen Brustgewebe. Wenn sie Brustkrebszellen des häufigen Luminal‑A‑Typs zwangen, zusätzlich POU1F1 zu produzieren, veränderte sich die Identität der Zellen. Sie verloren Marker reiferer Zellen und gewannen Marker, die mit stammzellähnlichem Verhalten verbunden sind, einschließlich eines starken Anstiegs der ALDH‑Aktivität. Die Zellen bildeten mehr Kolonien, produzierten dichtere dreidimensionale Sphären und verlagerten ihren Energiestoffwechsel stärker auf Zuckerverbrennung, ein Muster, das oft in aggressiven Tumoren zu sehen ist. Wurden POU1F1‑Spiegel in einer anderen Zelllinie, die natürlicherweise viel davon produziert, gesenkt, gingen diese stammzellähnlichen Merkmale zurück.
Die gefährlichste Untergruppe
Innerhalb der durch POU1F1 verstärkten Zellen isolierte das Team eine kleinere Gruppe mit besonders hoher ALDH‑Aktivität. Diese Subpopulation bewegte sich und invasierte in Labortests leichter und streute in Mäusen eher in Organe wie Lunge, Gehirn und Leber. Wurden sehr kleine Zellmengen in das Mammagewebe immundefizienter Mäuse injiziert, bildeten jene mit hohem POU1F1 und hohem ALDH deutlich häufiger Tumoren als andere Gruppen. Diese Tumoren zeigten mehr Zellteilung, höhere Werte des Proliferationsmarkers Ki67 und stärkere Färbung des CD44‑Markers, der mit krebsstammzellähnlichem Verhalten assoziiert ist. Insgesamt hatten Mäuse mit diesen Zellen eine kürzere Überlebenszeit, selbst wenn sie Hormonbehandlung und Strahlung erhielten, um die Patientenversorgung nachzuahmen.
Eine Signalkette, die Resistenz nährt
Um zu verstehen, wie POU1F1 diesen gefährlichen Zustand antreibt, untersuchten die Forschenden, welche Gene und Signalwege hochreguliert werden, wenn POU1F1‑Spiegel ansteigen. Sie fanden eine starke Aktivierung einer entzündlichen Kaskade, die das Signal IL‑6 und die Relay‑Proteine JAK2 und STAT3 umfasst. Zellen mit zusätzlichem POU1F1 sekretieren mehr IL‑6 und verwandte Signale und zeigten erhöhte Aktivität von JAK2, STAT3 und anderen Wachstumswegen. Das Blockieren dieser Kette mit Januskinase‑Inhibitoren oder mit einem Antikörper gegen den IL‑6‑Rezeptor verringerte ALDH‑Spiegel und reduzierte sowohl Kolonie‑ als auch Mammosphärenbildung. Einfach gesagt scheint POU1F1 einen IL‑6‑gesteuerten Schaltkreis einzuschalten, der wiederum den behandlungsresistenten, stammzellähnlichen Pool von Brustkrebszellen aufbaut und erhält.
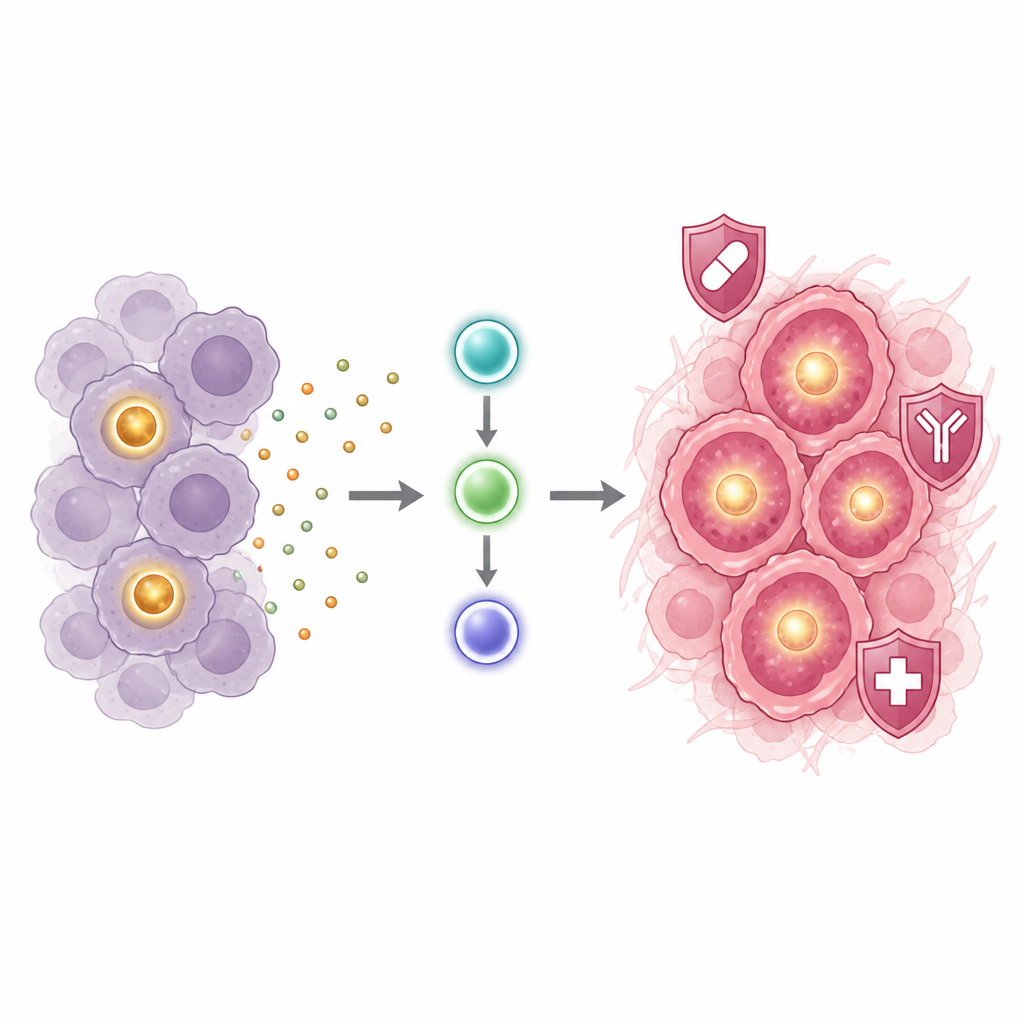
Was das für Patientinnen und Patienten bedeuten könnte
Indem die Studie POU1F1 mit einem bekannten entzündlichen Signalkanal und mit dem Anstieg von ALDH‑reichen, stammzellähnlichen Brustkrebszellen verbindet, trägt sie dazu bei zu erklären, warum Tumoren mit hohem POU1F1‑ und ALDH‑Gehalt mit schlechterer Prognose verknüpft sind. Die Ergebnisse legen nahe, dass in Tumoren mit hoher Expression dieses Proteins Medikamente, die den IL‑6–JAK2–STAT3‑Weg blockieren, die widerstandsfähigsten Krebszellen schwächen und das Rezidivrisiko senken könnten. Zwar sind weitere Forschung und klinische Prüfungen nötig, doch die Studie beschreibt eine klare Abfolge von Ereignissen von einem einzelnen Gen zur Therapieresistenz und weist auf bereits vorhandene Arzneimittelziele hin.
Zitation: Avila, L., Seoane, S., Rodriguez-Gonzalez, S. et al. POU1F1 induces cancer stem cell-like traits in breast cancer cells by IL-6/JAK2/STAT3 activation and enrichment of ALDH. npj Breast Cancer 12, 70 (2026). https://doi.org/10.1038/s41523-026-00929-w
Schlüsselwörter: Brustkrebs, Krebsstammzellen, POU1F1, IL-6 JAK2 STAT3, ALDH1A1