Clear Sky Science · pl
POU1F1 indukuje cechy podobne do komórek macierzystych nowotworu w komórkach raka piersi poprzez aktywację IL-6/JAK2/STAT3 i wzbogacenie ALDH
Dlaczego te badania są istotne
Wielu pacjentów z rakiem piersi dobrze reaguje na początkowe leczenie, lecz wciąż istnieje ryzyko, że choroba powróci lub rozsieje się po latach. Coraz częściej naukowcy podejrzewają, że niewielka grupa wyjątkowo opornych komórek nowotworowych, nazywanych czasem komórkami podobnymi do macierzystych, pomaga rakom przetrwać leki i radioterapię oraz zasiewać nowe guzy. To badanie bada, jak pojedyncze białko wewnątrz komórek raka piersi może włączyć te odporne komórki i wskazuje drogę, którą lekarze mogą kiedyś wykorzystać, by ten przełącznik wyłączyć.
Ukryci sprawcy wewnątrz guzów
Nie wszystkie komórki nowotworowe są takie same. Mniejszość zachowuje się jak komórki macierzyste, potrafią odnawiać się i zakładać nowe guzy po tym, jak większość innych komórek zostanie zniszczona. W raku piersi komórki te często mają pewną kombinację markerów powierzchniowych oraz enzym o nazwie ALDH, co ułatwia ich identyfikację. Dobrze rosną jako małe pływające kuleczki w laboratorium, opierają się chemioterapii i radioterapii oraz są bardzo skuteczne w zapalaniu guzów u zwierząt. Z tych cech wynikają podejrzenia, że odpowiadają za nawroty i przerzuty.
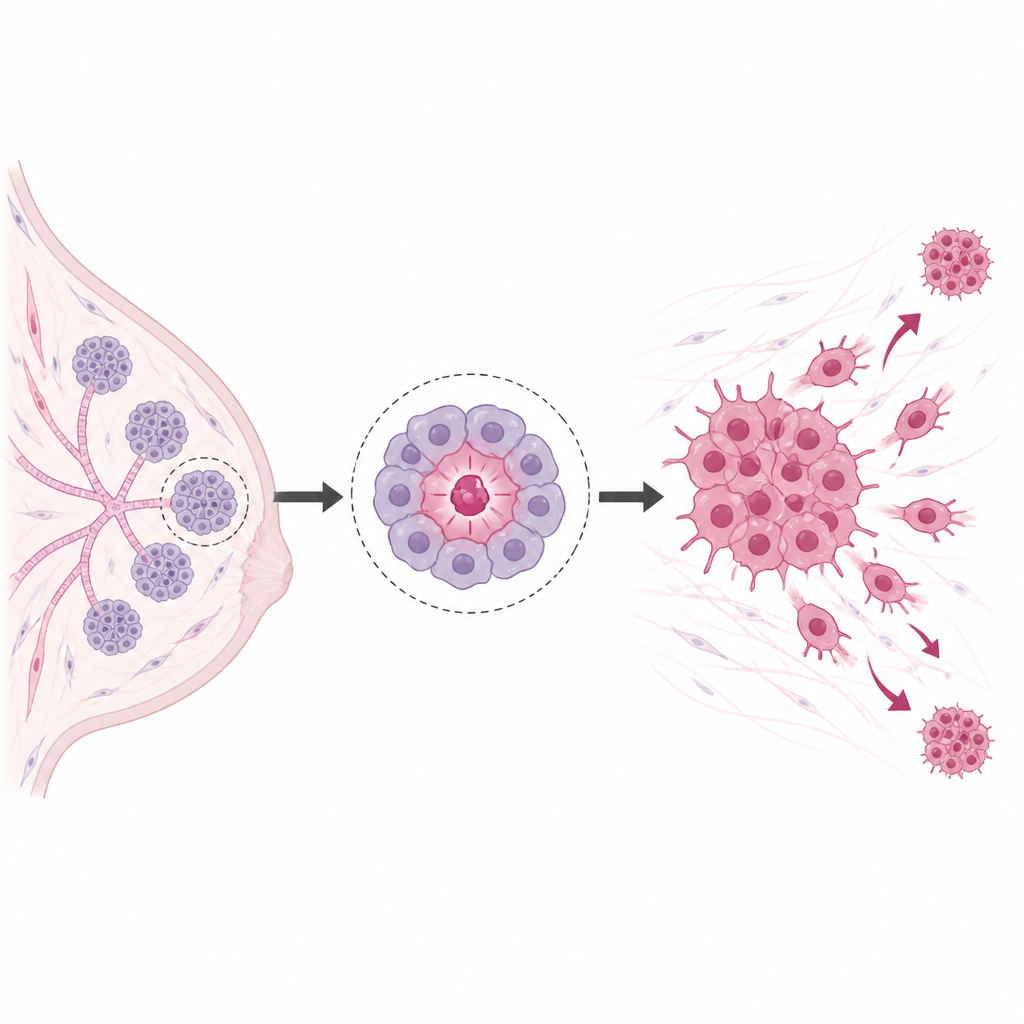
Przełącznik główny o nazwie POU1F1
Naukowcy skupili się na genie o nazwie POU1F1, długo znanym z roli w przysadce mózgowej, ale również występującym w wyższych poziomach w guzach piersi niż w tkance piersi normalnej. Gdy wymusili u komórek raka piersi typu luminal A produkcję dodatkowego POU1F1, komórki zmieniły swoją tożsamość. Utraciły markery związane z bardziej dojrzałymi komórkami i zyskały markery powiązane z zachowaniem przypominającym komórki macierzyste, w tym wyraźny wzrost aktywności ALDH. Komórki tworzyły więcej kolonii, wytwarzały gęstsze trójwymiarowe sfery i przesunęły swój metabolizm w kierunku utleniania glukozy, wzorca często obserwowanego w agresywnych nowotworach. Gdy poziomy POU1F1 obniżono w innej linii komórek raka piersi, która naturalnie wytwarza go dużo, te cechy przypominające komórki macierzyste zanikały.
Najbardziej niebezpieczna subpopulacja
Wśród komórek z podwyższonym POU1F1 zespół wyizolował następnie mniejszą grupę o szczególnie wysokim poziomie ALDH. Ta subpopulacja poruszała się i inwadowała łatwiej w testach laboratoryjnych i częściej rozprzestrzeniała się do narządów takich jak płuca, mózg i wątroba u myszy. Gdy bardzo małe liczby komórek wstrzyknięto do tkanki gruczołu mlekowego myszy z niedoborem układu odpornościowego, te z wysokim POU1F1 i wysokim ALDH tworzyły guzy znacznie częściej niż inne grupy. Guzy te wykazywały większy podział komórek, wyższe poziomy markera wzrostu Ki67 oraz silniejsze barwienie markera CD44 związanego z zachowaniem podobnym do komórek macierzystych nowotworu. Ogólnie rzecz biorąc, myszy noszące te komórki przeżywały krócej, nawet gdy otrzymywały leczenie hormonalne i radioterapię naśladujące opiekę pacjenta.
Łańcuch sygnałowy, który zasila oporność
Aby zrozumieć, jak POU1F1 napędza ten niebezpieczny stan, badacze przeanalizowali, które geny i szlaki włączają się, gdy rosną poziomy POU1F1. Stwierdzili silną aktywację zapalnego łańcucha obejmującego sygnał IL-6 oraz białka przekaźnikowe JAK2 i STAT3. Komórki z dodatkowym POU1F1 wydzielały więcej IL-6 i sąsiednich sygnałów oraz wykazywały wyższą aktywność JAK2, STAT3 i innych szlaków wzrostu. Blokowanie tego łańcucha lekami hamującymi kinazy Janusowe lub przeciwciałem blokującym receptor IL-6 zmniejszało poziomy ALDH i ograniczało zarówno tworzenie kolonii, jak i sfer w hodowli. Prościej mówiąc, POU1F1 wydaje się włączać obwód kierowany przez IL-6, który z kolei buduje i podtrzymuje oporną na leczenie pulę komórek raka piersi o cechach macierzystych.
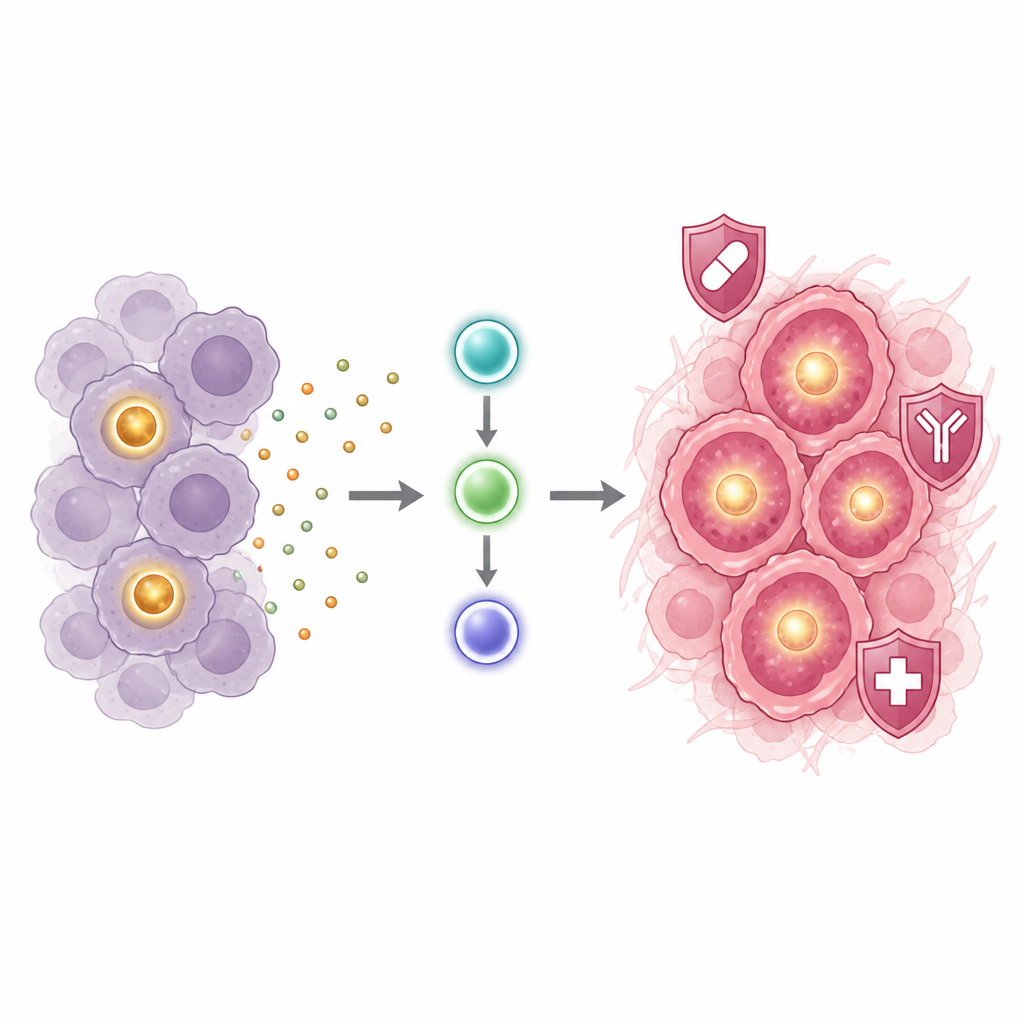
Co to może znaczyć dla pacjentów
Łącząc POU1F1 z powszechnie znanym zapalnym szlakiem sygnalizacyjnym i ze wzrostem komórek bogatych w ALDH o cechach macierzystych, praca ta pomaga wyjaśnić, dlaczego guzy z wysokim poziomem POU1F1 i ALDH związane są z gorszymi wynikami u pacjentów. Wyniki sugerują, że w guzach, w których to białko jest obfite, leki blokujące szlak IL-6 JAK2 STAT3 mogą osłabić najbardziej oporne komórki nowotworowe i zmniejszyć ryzyko nawrotu. Choć potrzeba więcej badań i testów klinicznych, badanie mapuje wyraźny łańcuch zdarzeń prowadzący od pojedynczego genu do oporności na leczenie i wskazuje na istniejące już cele lekowe.
Cytowanie: Avila, L., Seoane, S., Rodriguez-Gonzalez, S. et al. POU1F1 induces cancer stem cell-like traits in breast cancer cells by IL-6/JAK2/STAT3 activation and enrichment of ALDH. npj Breast Cancer 12, 70 (2026). https://doi.org/10.1038/s41523-026-00929-w
Słowa kluczowe: rak piersi, komórki macierzyste nowotworu, POU1F1, IL-6 JAK2 STAT3, ALDH1A1