Clear Sky Science · zh
由布鲁氏复发热螺旋体一簇独特免疫调节外表面蛋白介导的补体抑制
为什么一种血液传播的致热菌难以被清除
虱媒复发热是一种严重但被忽视的疾病,仍然影响生活在贫困和拥挤环境中的人群。其致病菌为布鲁氏复发热螺旋体(Borrelia recurrentis),这种细菌能在人体血液中长期存活,尽管人体具有强大的免疫监视系统。本研究发现了一类新的五个表面蛋白家族,命名为ChiA到ChiE,它们帮助微生物躲避天然防御。理解这些蛋白如何起作用,可能为改进诊断、治疗或针对这种致命感染的疫苗研发提供途径。 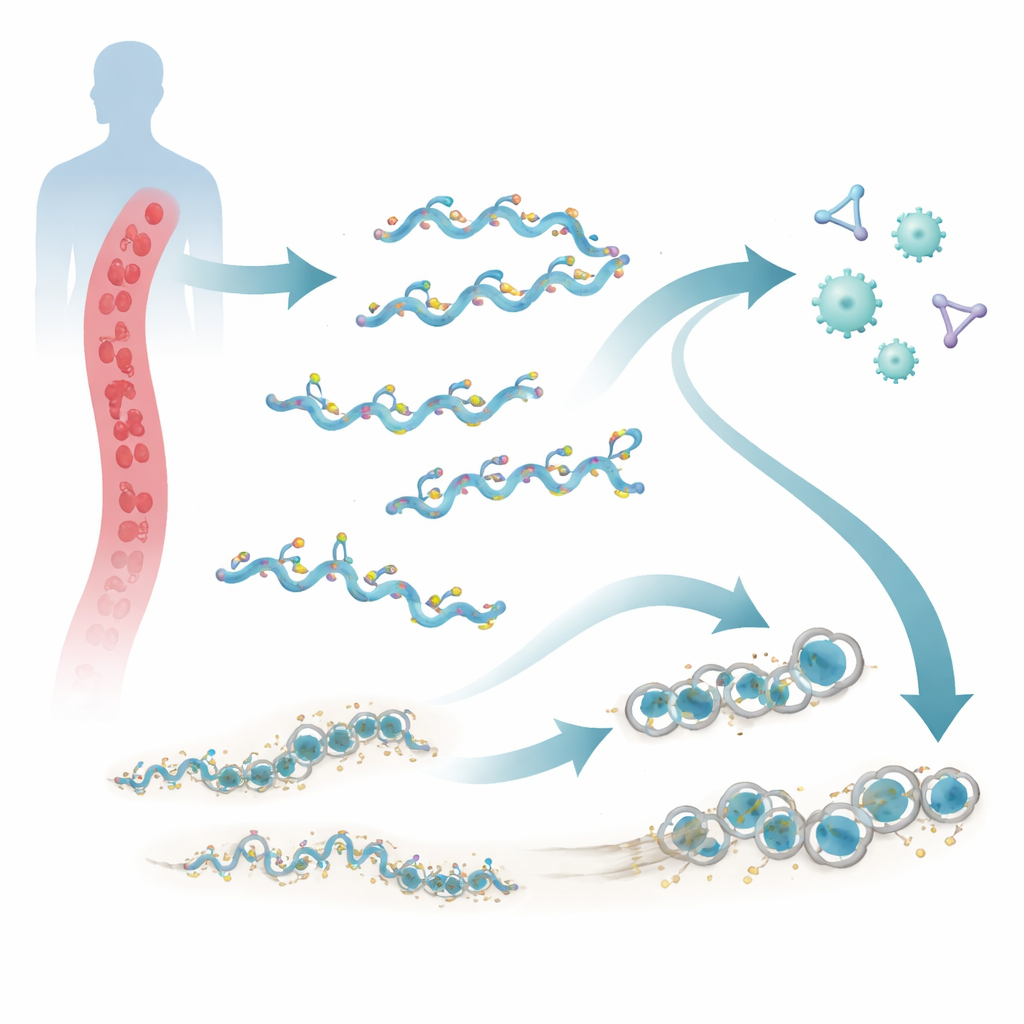
人体的防护网与病原如何突破它
我们的血液中有一套被称为补体系统的蛋白网络,负责巡查入侵者。补体被激活时会标记微生物以便清除,并能以环状武器——膜攻击复合体——在其膜上打洞。布鲁氏复发热螺旋体直接生活在血流中,因此从进入体内的那一刻起就面临这种攻击。早期研究表明,该细菌能借用人体的防护因子来削弱补体反应。新研究进一步揭示,B. recurrentis还携带自身工具:一簇五个相关的外表面蛋白ChiA至ChiE,它们位于称为巨型质粒(megaplasmid)的大片段DNA上。
隐藏的表面蛋白工具箱
通过对不同患者分离株的基因比较,研究者发现Chi基因簇在B. recurrentis中高度保守,暗示其对生存重要。Chi蛋白为锚定在细菌外表面的脂蛋白,可直接与来袭的免疫分子接触。通过X射线晶体学和先进的计算建模进行的结构研究显示,五者均具有紧凑的八螺旋核心及作者称之为S域的突出区域。每个蛋白的核心处都有一个深而疏油的口袋;在ChiB中,该口袋容纳了一种磷脂,提示这些分子可能结合周围环境中的脂类。两种成员ChiC和ChiE含有成对的含硫氨基酸,位置使其能形成可逆的二硫键,提示这些蛋白可能根据宿主体内的局部化学环境切换其行为。 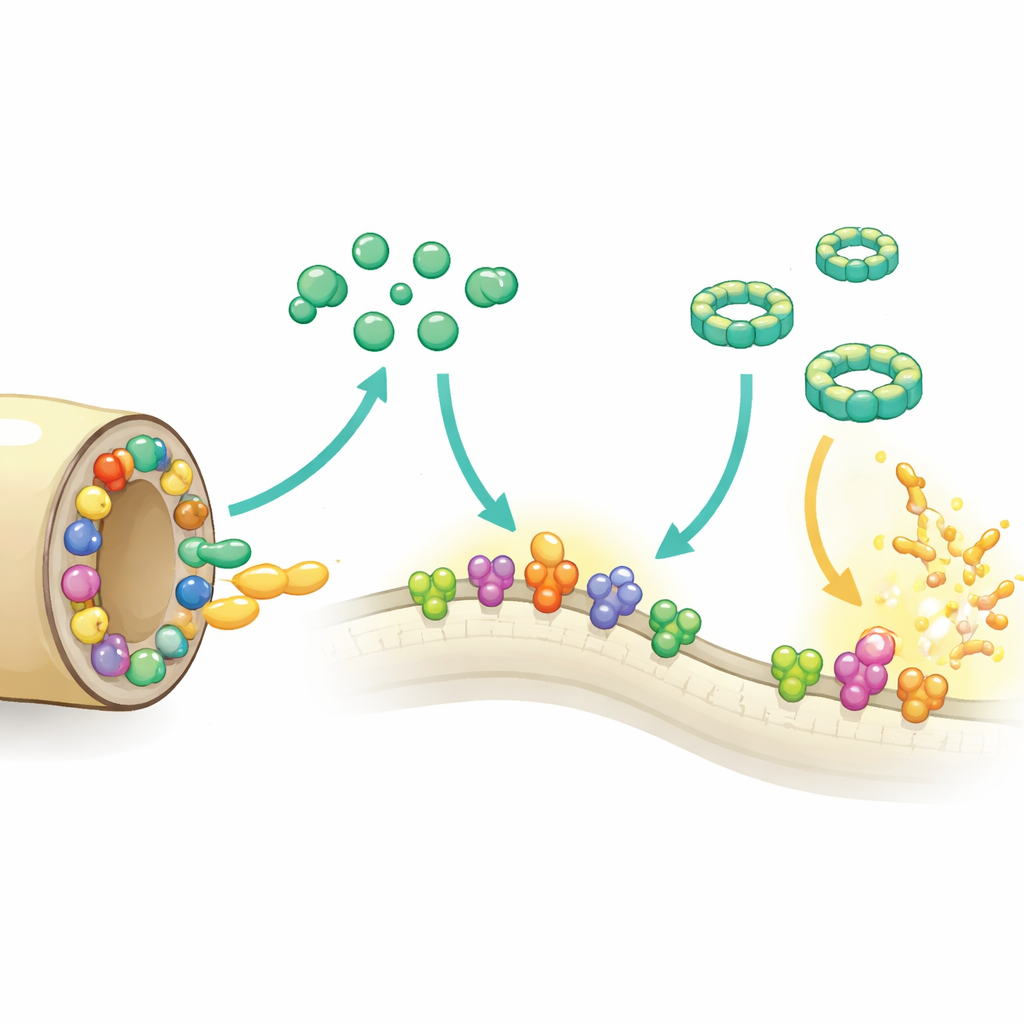
在多个步骤上关闭免疫攻击
研究组在试管实验中检测了各Chi蛋白对补体系统的影响。五种蛋白均能抑制所谓的替代途径——补体被触发的主要通路之一,尽管ChiA的作用较弱。ChiE更进一步,还抑制了由抗体或微生物糖模式激活的经典途径和凝集素途径。若干Chi蛋白,尤其是ChiB、ChiC、ChiD和ChiE,干扰了补体蛋白在细胞表面组装成有害环状结构的最终阶段,阻止了完整环的形成,并在溶血实验中保护了红细胞。这些蛋白能结合关键的补体成分,如C3b及经典途径的部分组分,借此阻断级联反应,而无需自身切割这些分子。
借用人源酶以开辟通路
除直接阻断补体外,Chi蛋白还利用了另一个人体系统:纤溶酶原,即组织溶解酶纤溶酶的非活性形式。大多数Chi蛋白能与纤溶酶原牢固结合,一旦加入人体激活因子,被捕获的纤溶酶即可切割补体成分C3b。这意味着B. recurrentis可在其表面装饰宿主来源的酶,帮助切除补体标记以及可能的其他屏障,如组织结构,从而助力在体内扩散。当研究者将纯化的Chi蛋白加入对血清敏感的布鲁氏菌株,或将该菌株工程化表达特定Chi蛋白时,这些细菌在人体血清中的存活明显提高,证实这些分子在实践中使补体攻击不那么致命。
对患者和预防的意义
综上所述,研究揭示了一组专门的表面蛋白家族,使布鲁氏复发热螺旋体获得对人体免疫系统的分层防御。Chi蛋白在多个阶段阻断补体并招募人体酶进一步削弱免疫标记,使细菌得以在血液中持久存在并引发反复发热。对于非专业读者,关键信息是该微生物并非靠躲藏生存,而是通过主动解除我们分子防御来存活。通过描绘这些Chi蛋白的形状与功能,研究为未来设计中和它们的药物或疫苗提供了蓝图,可能恢复人体清除这一被忽视但危险感染的能力。
引用: Röttgerding, F., Reyer, F., Gerlach, E. et al. Complement inhibition by a unique cluster of immunomodulatory outer surface proteins of Borrelia recurrentis. Nat Commun 17, 3900 (2026). https://doi.org/10.1038/s41467-026-72359-y
关键词: 虱媒复发热, 布鲁氏复发热螺旋体, 补体逃逸, 细菌表面蛋白, 纤溶酶原结合