Clear Sky Science · it
Inibizione del complemento da parte di un unico cluster di proteine di superficie immunomodulatorie di Borrelia recurrentis
Perché un agente febbrile ematico è difficile da eliminare
La febbre ricorrente trasmessa da pidocchi è una malattia grave ma trascurata che continua a colpire persone che vivono in condizioni di povertà e sovraffollamento. È causata dal batterio Borrelia recurrentis, che può sopravvivere per lunghi periodi nel sangue umano nonostante un potente sistema di sorveglianza immunitaria. Questo studio mette in luce una nuova famiglia di cinque proteine di superficie, chiamate ChiA fino a ChiE, che aiutano il microrganismo a sfuggire alle nostre difese naturali. Comprendere come funzionano queste proteine potrebbe aprire la strada a migliori strumenti diagnostici, terapie o vaccini contro questa infezione letale. 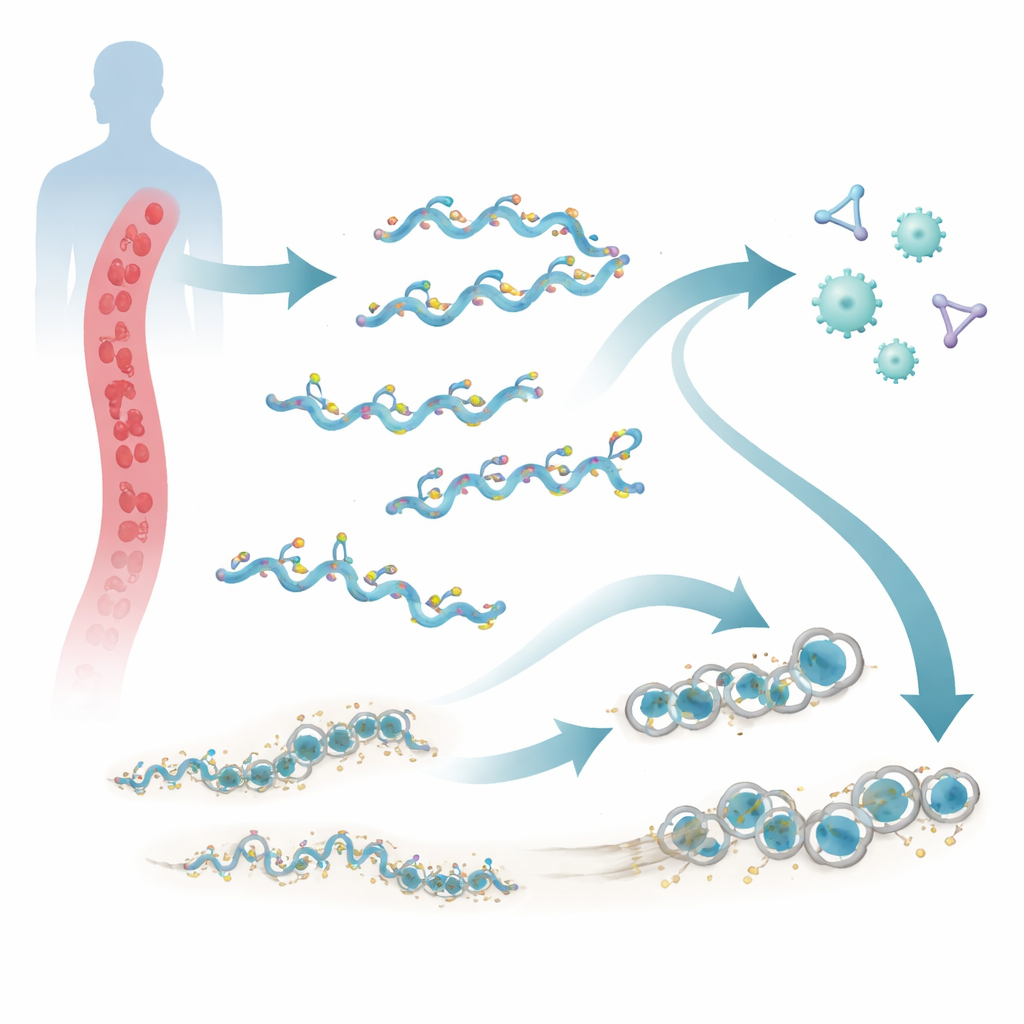
Lo scudo dell’organismo e come questo germe lo oltrepassa
Il nostro sangue ospita una rete di proteine nota come sistema del complemento, che pattuglia alla ricerca di intrusi. Quando si attiva, il complemento segna i microrganismi per la distruzione e può perforare le loro membrane con un’arma ad anello chiamata complesso di attacco alla membrana. Borrelia recurrentis vive direttamente nel flusso sanguigno e quindi si trova ad affrontare questo attacco dal momento in cui entra nell’organismo. Lavori precedenti avevano dimostrato che il batterio può sfruttare fattori protettivi umani per attenuare il complemento. La nuova ricerca rivela che B. recurrentis porta anche i propri strumenti: un cluster di cinque proteine correlate di superficie esterna, ChiA fino a ChiE, localizzate insieme su un grande segmento di DNA chiamato megaplasmide.
Un kit nascosto di proteine di superficie
Attraverso confronti genetici tra diversi isolati clinici, gli autori hanno scoperto che questo cluster genico Chi è altamente conservato in B. recurrentis, il che suggerisce che sia importante per la sopravvivenza. Le proteine Chi sono lipoproteine ancorate alla superficie esterna del batterio, dove possono incontrare direttamente le molecole immunitarie in arrivo. Lavori strutturali con cristallografia a raggi X e sofisticati modelli computazionali hanno mostrato che tutte e cinque condividono un nucleo compatto a otto eliche e una regione sporgente che gli autori chiamano dominio S. Al centro di ciascuna proteina si trova una profonda tasca oleosa; in una proteina, ChiB, questa tasca contiene un fosfolipide, suggerendo che queste molecole possano legare lipidi provenienti dall’ambiente. Due membri, ChiC e ChiE, contengono coppie di amminoacidi contenenti zolfo posizionati in modo da poter formare legami reversibili, suggerendo che queste proteine possano modificare il loro comportamento a seconda dell’ambiente chimico locale nell’ospite. 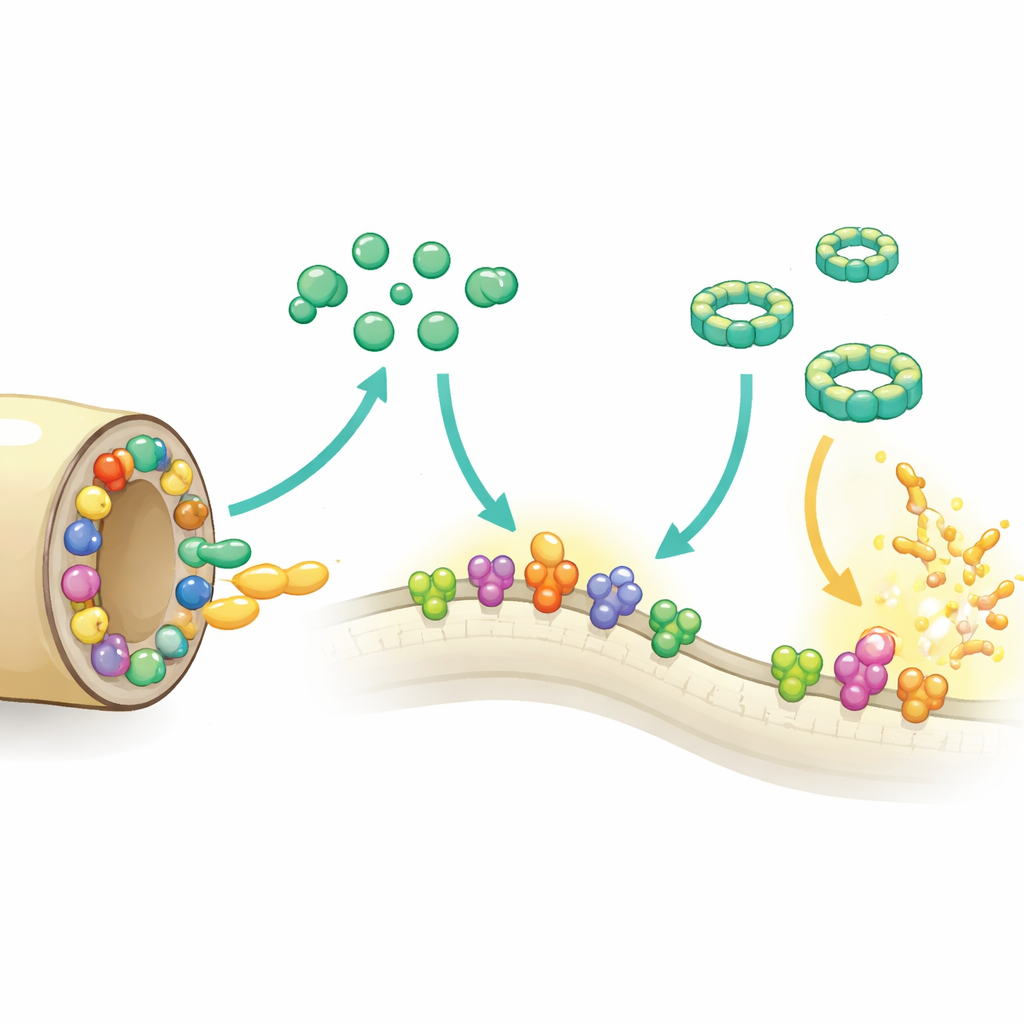
Disattivare l’attacco immunitario a più livelli
Il gruppo ha testato come ogni proteina Chi influenzi il sistema del complemento in esperimenti in provetta. Tutte e cinque sono state in grado di attenuare la cosiddetta via alternativa, una delle principali vie con cui il complemento viene attivato, sebbene ChiA fosse più debole. ChiE è andata oltre e ha anche smorzato le vie classica e lectina, che sono attivate da anticorpi o da motivi zuccherini sui microrganismi. Diverse proteine Chi, in particolare ChiB, ChiC, ChiD e ChiE, interferivano con la fase finale in cui le proteine del complemento si assemblano in anelli dannosi sulle superfici cellulari, impedendo la formazione completa degli anelli e proteggendo i globuli rossi in un saggio di emolisi. Le proteine legavano componenti chiave del complemento, come C3b e parti della via classica, bloccando così la cascata senza la necessità di tagliare queste molecole da sé.
Prendere in prestito un enzima umano per farsi strada
Oltre a bloccare direttamente il complemento, le proteine Chi sfruttano anche un altro sistema umano: il plasminogeno, la forma inattiva dell’enzima che dissolve i tessuti, la plasmina. La maggior parte delle proteine Chi legava strettamente il plasminogeno e, una volta aggiunto un attivatore umano, la plasmina catturata poteva tagliare il componente del complemento C3b. Questo significa che B. recurrentis può decorare la propria superficie con enzimi derivati dall’ospite che aiutano a rimuovere i marchi del complemento e possibilmente altre barriere, come strutture tissutali, agevolando la diffusione nell’organismo. Quando i ricercatori hanno aggiunto proteine Chi purificate a un ceppo di Borrelia sensibile al siero, o hanno ingegnerizzato quel ceppo per produrre specifiche proteine Chi, i batteri sono sopravvissuti molto meglio nel siero umano, confermando che queste molecole rendono l’attacco del complemento meno letale nella pratica.
Cosa significa per i pazienti e la prevenzione
Complessivamente, i risultati rivelano una famiglia specializzata di proteine di superficie che conferiscono a Borrelia recurrentis una difesa stratificata contro il sistema immunitario umano. Le proteine Chi bloccano il complemento in più fasi e reclutano enzimi umani per indebolire ulteriormente il marchio immunitario, permettendo al batterio di persistere nel sangue e causare episodi febbrili ricorrenti. Per i non specialisti, il messaggio chiave è che questo microrganismo sopravvive non nascondendosi, ma disarmando attivamente le nostre difese molecolari. Mappando le forme e le funzioni di queste proteine Chi, lo studio fornisce un progetto di riferimento per lavori futuri volti a progettare farmaci o vaccini che le neutralizzino, ripristinando potenzialmente la capacità dell’organismo di eliminare questa infezione trascurata ma pericolosa.
Citazione: Röttgerding, F., Reyer, F., Gerlach, E. et al. Complement inhibition by a unique cluster of immunomodulatory outer surface proteins of Borrelia recurrentis. Nat Commun 17, 3900 (2026). https://doi.org/10.1038/s41467-026-72359-y
Parole chiave: febbre ricorrente trasmessa da pidocchi, Borrelia recurrentis, evasione del complemento, proteine di superficie batteriche, legame con plasminogeno