Clear Sky Science · nl
Remming van het complement door een unieke cluster immunomodulerende oppervlakproteïnen van Borrelia recurrentis
Waarom een bloedgedragen koortsverwekker moeilijk te doden is
Vlooien-gedragen terugkerende koorts is een ernstige maar verwaarloosde ziekte die nog steeds mensen treft die in armoede en overbevolkte omstandigheden leven. Ze wordt veroorzaakt door de bacterie Borrelia recurrentis, die lange tijd in menselijk bloed kan overleven ondanks een krachtig immuurbewakingssysteem. Deze studie onthult een nieuwe familie van vijf oppervlakproteïnen, genoemd ChiA tot ChiE, die de microbe helpen onze natuurlijke afweer te ontwijken. Begrijpen hoe deze eiwitten werken kan de weg openen naar betere diagnostiek, behandelingen of vaccins tegen deze dodelijke infectie. 
Het schild van het lichaam en hoe deze kiem erdoorheen glipt
Ons bloed bevat een netwerk van eiwitten dat bekendstaat als het complementsysteem, dat op zoek gaat naar indringers. Wanneer het geactiveerd wordt, markeert complement microben voor vernietiging en kan het gaten in hun membranen slaan met een ringvormig wapen dat het membraan-aanvalscomplex heet. Borrelia recurrentis leeft direct in de bloedbaan en staat dus vanaf het eerste moment bloot aan deze aanval. Eerder werk toonde aan dat de bacterie menselijke beschermende factoren kan lenen om complement te temperen. Het nieuwe onderzoek laat zien dat B. recurrentis ook eigen instrumenten meebrengt: een cluster van vijf verwante buitenoppervlakproteïnen, ChiA tot ChiE, die samen op een groot DNA-segment genaamd een megaplasmide zijn gelegen.
Een verborgen gereedschapsset van oppervlakproteïnen
Met genetische vergelijkingen van verschillende patiëntenisolaten vonden de auteurs dat deze Chi-gencluster sterk geconserveerd is in B. recurrentis, wat erop wijst dat hij belangrijk is voor overleving. De Chi-eiwitten zijn lipoproteïnen die in het buitenoppervlak van de bacterie verankerd zitten, waar ze direct in contact kunnen komen met binnenkomende immuunmoleculen. Structureel werk met röntgendiffractie en geavanceerde computermodellering toonde aan dat alle vijf een compact, acht-helixcore delen en een uitstekende regio die de auteurs de S-domein noemen. In het hart van elk eiwit ligt een diepe olieachtige pocket; in één eiwit, ChiB, bevindt zich in deze pocket een fosfolipide, wat suggereert dat deze moleculen vetten uit hun omgeving kunnen binden. Twee leden, ChiC en ChiE, bevatten paren zwavelhoudende aminozuren die zo gepositioneerd zijn dat ze reversibele bindingen kunnen vormen, wat erop wijst dat deze eiwitten hun gedrag kunnen schakelen afhankelijk van de lokale chemische omgeving in de gastheer. 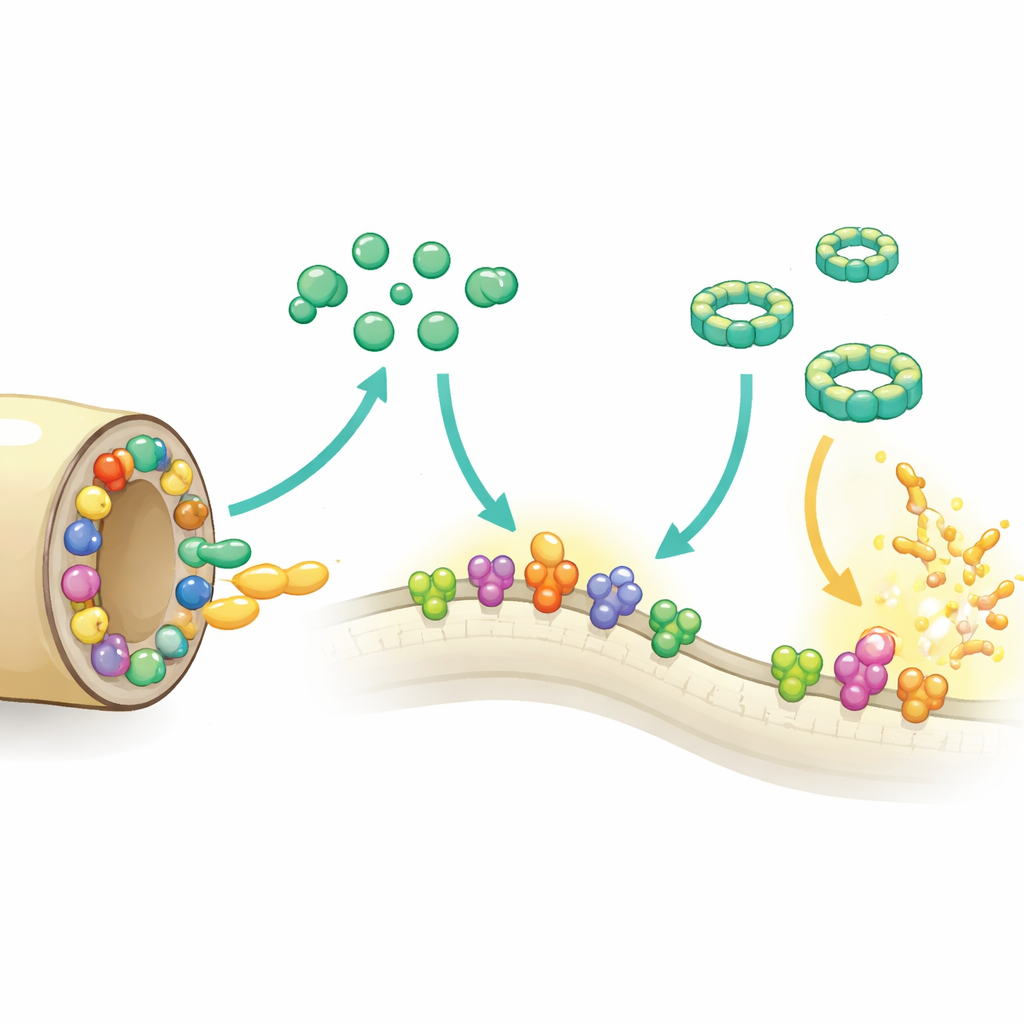
Het immuunaanval op meerdere stappen stilleggen
Het team testte in proefbuisexperimenten hoe elk Chi-eiwit het complementsysteem beïnvloedt. Alle vijf konden de zogenaamde alternatieve route temperen, een van de belangrijkste wegen waarop complement geactiveerd wordt, hoewel ChiA zwakker was. ChiE ging verder en dempte ook de klassieke en lectine-route, die worden geactiveerd door antilichamen of suikergroeperingen op microben. Verschillende Chi-eiwitten, vooral ChiB, ChiC, ChiD en ChiE, interfereerden met de laatste fase waarbij complement-eiwitten zich op cellulaire oppervlakken samenvoegen tot schadelijke ringen, en voorkwamen zo de volledige ringvorming en beschermden rode bloedcellen in een hemolyse-assay. De eiwitten bonden sleutelcomponenten van complement, zoals C3b en onderdelen van de klassieke route, en blokkeerden daarmee de cascade zonder deze moleculen zelf te hoeven knippen.
Het lenen van een menselijk enzym om een pad vrij te maken
Naast het direct blokkeren van complement maken de Chi-eiwitten ook gebruik van een ander menselijk systeem: plasminogeen, de inactieve vorm van het weefseloplossende enzym plasmine. De meeste Chi-eiwitten bonden plasminogeen sterk, en zodra een menselijke activator werd toegevoegd, kon het gevangen plasmine complementcomponent C3b knippen. Dit betekent dat B. recurrentis zijn oppervlak kan versieren met gastheer-afgeleide enzymen die helpen complementlabels en mogelijk andere barrières, zoals weefselstructuren, weg te knippen, wat de verspreiding door het lichaam bevordert. Wanneer de onderzoekers gezuiverde Chi-eiwitten toevoegden aan een serum-gevoelige Borrelia-stam, of die stam zo ontwierpen dat ze bepaalde Chi-eiwitten produceerde, overleefden de bacteriën veel beter in menselijk serum, wat bevestigt dat deze moleculen complementaanvallen in de praktijk minder dodelijk maken.
Wat dit betekent voor patiënten en preventie
Samen onthullen de bevindingen een gespecialiseerde familie van oppervlakproteïnen die Borrelia recurrentis een gelaagde verdediging tegen het menselijk immuunsysteem geven. De Chi-eiwitten blokkeren complement op verschillende stappen en rekruteren menselijke enzymen om de immuunmarkering verder te verzwakken, waardoor de bacterie in het bloed kan blijven bestaan en herhaalde koortsepisodes kan veroorzaken. Voor niet-specialisten is de kernboodschap dat deze microbe niet overleeft door zich te verbergen, maar door actief onze moleculaire verdedigingsmechanismen uit te schakelen. Door de vormen en functies van deze Chi-eiwitten in kaart te brengen, biedt de studie een blauwdruk voor toekomstig werk om geneesmiddelen of vaccins te ontwerpen die ze neutraliseren en mogelijk het herstel van het vermogen van het lichaam om deze verwaarloosde maar gevaarlijke infectie te verwijderen weer mogelijk maken.
Bronvermelding: Röttgerding, F., Reyer, F., Gerlach, E. et al. Complement inhibition by a unique cluster of immunomodulatory outer surface proteins of Borrelia recurrentis. Nat Commun 17, 3900 (2026). https://doi.org/10.1038/s41467-026-72359-y
Trefwoorden: vlooien-gedragen terugkerende koorts, Borrelia recurrentis, ontwijking van complement, bacteriële oppervlakproteïnen, plasminogeenbinding