Clear Sky Science · de
Komplementinhibition durch einen einzigartigen Cluster immunmodulatorischer Oberflächenproteine von Borrelia recurrentis
Warum ein blutgetragenes Fieberkeim schwer zu töten ist
Das lausübertragene rezidivierende Fieber ist eine schwere, aber vernachlässigte Krankheit, die weiterhin Menschen betrifft, die unter Armut und beengten Wohnverhältnissen leben. Verursacht wird sie durch das Bakterium Borrelia recurrentis, das trotz eines starken Immunschirms lange im menschlichen Blut überdauern kann. Diese Studie identifiziert eine neue Familie von fünf Oberflächenproteinen, genannt ChiA bis ChiE, die dem Erreger helfen, unsere natürlichen Abwehrkräfte zu umgehen. Das Verständnis der Wirkungsweise dieser Proteine könnte den Weg für bessere Diagnostik, Behandlungen oder Impfstoffe gegen diese tödliche Infektion ebnen. 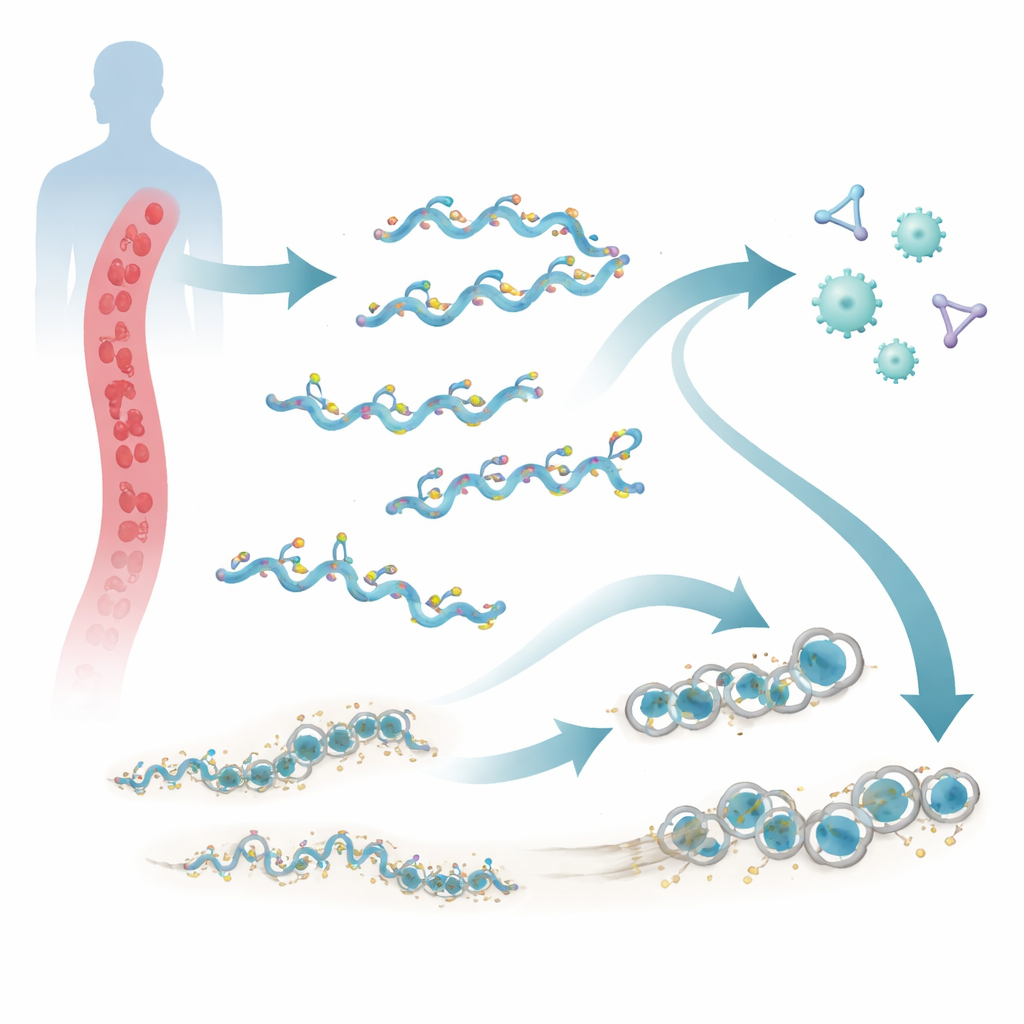
Der körpereigene Schild und wie dieser Erreger ihn umgeht
Unser Blut trägt ein Netzwerk von Proteinen, das als Komplementsystem bekannt ist und nach Eindringlingen fahndet. Bei Aktivierung markiert das Komplement Mikroben zur Zerstörung und kann mit einem ringförmigen Instrument, dem Membranangriffskomplex, Löcher in ihre Membranen reißen. Borrelia recurrentis lebt direkt im Blutkreislauf und ist daher sofort nach dem Eindringen dem Angriff ausgesetzt. Frühere Arbeiten zeigten, dass das Bakterium menschliche Schutzfaktoren ausnutzen kann, um das Komplement abzuschwächen. Die neue Forschung zeigt, dass B. recurrentis zudem eigene Werkzeuge mitbringt: einen Cluster aus fünf verwandten Außenflächenproteinen, ChiA bis ChiE, die zusammen auf einem großen DNA-Abschnitt liegen, dem sogenannten Megaplasmid.
Ein versteckter Werkzeugkasten an Oberflächenproteinen
Anhand genetischer Vergleiche verschiedener Patientenisolate fanden die Autoren, dass der Chi-Gencluster bei B. recurrentis stark konserviert ist, was darauf hindeutet, dass er für das Überleben wichtig ist. Die Chi-Proteine sind Lipoproteine, die in der Außenschicht des Bakteriums verankert sind und dort direkt auf eintreffende Immunmoleküle treffen können. Strukturelle Untersuchungen mittels Röntgenkristallographie und fortgeschrittener Computermodellierung zeigten, dass alle fünf ein kompaktes Kernmotiv aus acht Helices und eine hervorstehende Region aufweisen, die die Autoren als S-Domäne bezeichnen. Im Zentrum jedes Proteins liegt eine tiefe, ölige Tasche; in einem Protein, ChiB, enthält diese Tasche ein Phospholipid, was nahelegt, dass diese Moleküle Fette aus ihrer Umgebung binden könnten. Zwei Familienmitglieder, ChiC und ChiE, besitzen Paare schwefelhaltiger Aminosäuren, die so positioniert sind, dass sie reversible Bindungen eingehen können, was darauf hindeutet, dass diese Proteine ihr Verhalten je nach lokalem chemischem Milieu im Wirt umschalten könnten. 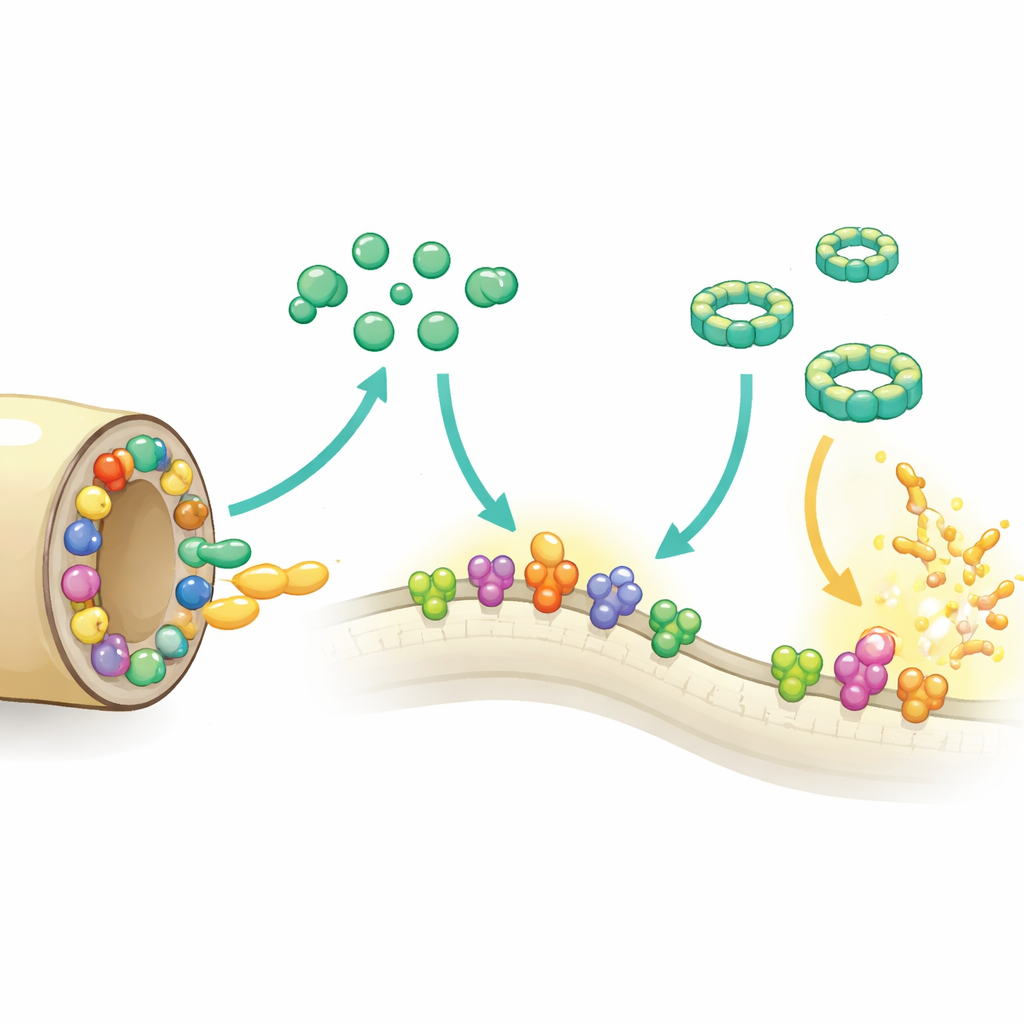
Die Immunabwehr an mehreren Stellen ausschalten
Das Team prüfte, wie jedes Chi-Protein das Komplementsystem in Reagenzglas-Experimenten beeinflusst. Alle fünf konnten den sogenannten alternativen Weg abschwächen, einer der Hauptwege, über die Komplement ausgelöst wird, wobei ChiA schwächer war. ChiE ging weiter und dämpfte zusätzlich den klassischen und den Lektin-Weg, die durch Antikörper bzw. Zuckermuster auf Mikroben aktiviert werden. Mehrere Chi-Proteine, insbesondere ChiB, ChiC, ChiD und ChiE, störten die Endphase, in der Komplementproteine sich zu schädlichen Ringen auf Zelloberflächen zusammenlagern, verhinderten die vollständige Ringbildung und schützten rote Blutkörperchen in einem Hämolyse-Assay. Die Proteine banden Schlüsselkomponenten des Komplements, wie C3b und Teile des klassischen Wegs, und blockierten dadurch die Kaskade, ohne diese Moleküle selbst zerschneiden zu müssen.
Ein menschliches Enzym ausleihen, um den Weg zu räumen
Über die direkte Blockade des Komplements hinaus nutzen die Chi-Proteine ein weiteres menschliches System: Plasminogen, die inaktive Form des gewebeauflösenden Enzyms Plasmin. Die meisten Chi-Proteine banden Plasminogen fest, und sobald ein menschlicher Aktivator hinzugefügt wurde, konnte das gebundene Plasmin das Komplementfragment C3b zerschneiden. Das bedeutet, dass B. recurrentis seine Oberfläche mit wirtseigenen Enzymen dekorieren kann, die helfen, Komplementmarkierungen und möglicherweise andere Barrieren wie Gewebsstrukturen abzuschneiden, was die Ausbreitung im Körper erleichtert. Wenn die Forscher gereinigte Chi-Proteine zu einem serumempfindlichen Borrelia-Stamm hinzufügten oder diesen Stamm gentechnisch so veränderten, dass er bestimmte Chi-Proteine produziert, überlebten die Bakterien im menschlichen Serum deutlich besser, was bestätigt, dass diese Moleküle den Komplementangriff in der Praxis weniger tödlich machen.
Was das für Patienten und Prävention bedeutet
Zusammen zeigen die Ergebnisse eine spezialisierte Familie von Oberflächenproteinen, die Borrelia recurrentis eine gestaffelte Verteidigung gegen das menschliche Immunsystem verleihen. Die Chi-Proteine blockieren Komplement in mehreren Stadien und rekrutieren menschliche Enzyme, um die Immunmarkierung weiter zu schwächen, sodass das Bakterium im Blut persistieren und wiederkehrende Fieberanfälle verursachen kann. Für Nichtfachleute lautet die Kernbotschaft: Dieser Erreger überlebt nicht durch Verbergen, sondern indem er unsere molekularen Abwehrmechanismen aktiv außer Gefecht setzt. Durch die Kartierung der Gestalt und Funktion dieser Chi-Proteine liefert die Studie eine Vorlage für künftige Arbeiten, die darauf abzielen, Wirkstoffe oder Impfstoffe zu entwickeln, die sie neutralisieren und so die Fähigkeit des Körpers wiederherstellen könnten, diese vernachlässigte, aber gefährliche Infektion zu beseitigen.
Zitation: Röttgerding, F., Reyer, F., Gerlach, E. et al. Complement inhibition by a unique cluster of immunomodulatory outer surface proteins of Borrelia recurrentis. Nat Commun 17, 3900 (2026). https://doi.org/10.1038/s41467-026-72359-y
Schlüsselwörter: lausübertragendes rezidivierendes Fieber, Borrelia recurrentis, Komplement-Evasion, bakterielle Oberflächenproteine, Plasminogen-Bindung