Clear Sky Science · zh
腹水可保护细胞免受铁死亡并促进卵巢癌在腹膜的生长
腹腔液为何重要
许多晚期卵巢癌患者会在腹腔内出现称为腹水的液体积聚。临床上长期知道这种液体意味着病情严重,但其具体如何帮助肿瘤存活和扩散并不清楚。本研究揭示了腹水中的成分如何保护卵巢癌细胞免受一种特定细胞死亡方式的侵害,从而支持癌细胞在腹膜上的生长。
液体与癌细胞之间的危险共谋
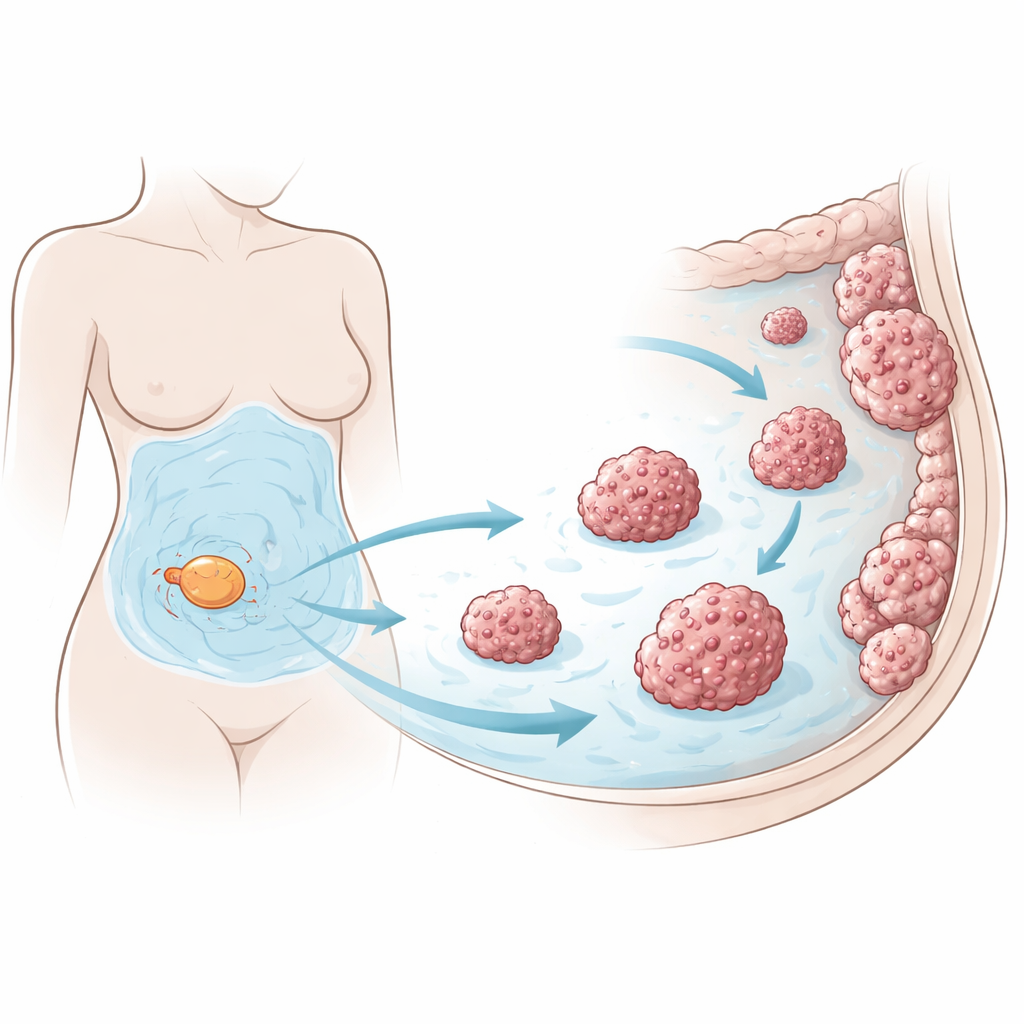
卵巢癌常沿腹腔内表面——腹膜——扩散。随着病情进展,血管通透性增加导致大量腹水在腔内积聚。研究者关注卵巢癌细胞的一个脆弱点:它们极易发生铁死亡,这是一种由铁和细胞膜脂质损伤驱动的细胞死亡形式。漂浮在腹腔中的游离癌细胞应当特别容易遭受此类压力,因此团队探讨了这些细胞如何在足够长时间内存活以播种新的肿瘤。
腹水屏蔽细胞免受致命压力
研究人员使用人源卵巢癌细胞系、来自患者的新鲜肿瘤细胞以及从患者组织培养的小型三维类器官,暴露于通常会诱导铁死亡的药物中。他们发现,即便少量来自卵巢癌患者的腹水也能强烈保护所有这些模型免于铁死亡,而并未对其它类型的毒性药物提供保护。在小鼠体内,将卵巢癌细胞与人源腹水共同注入导致腹腔肿瘤负荷增加、肿瘤内脂质损伤迹象减少且小鼠存活期缩短,表明这种液体的保护作用不仅在体外培养皿中存在,在活体动物中同样发挥作用。
富含脂质的货物驱动保护作用
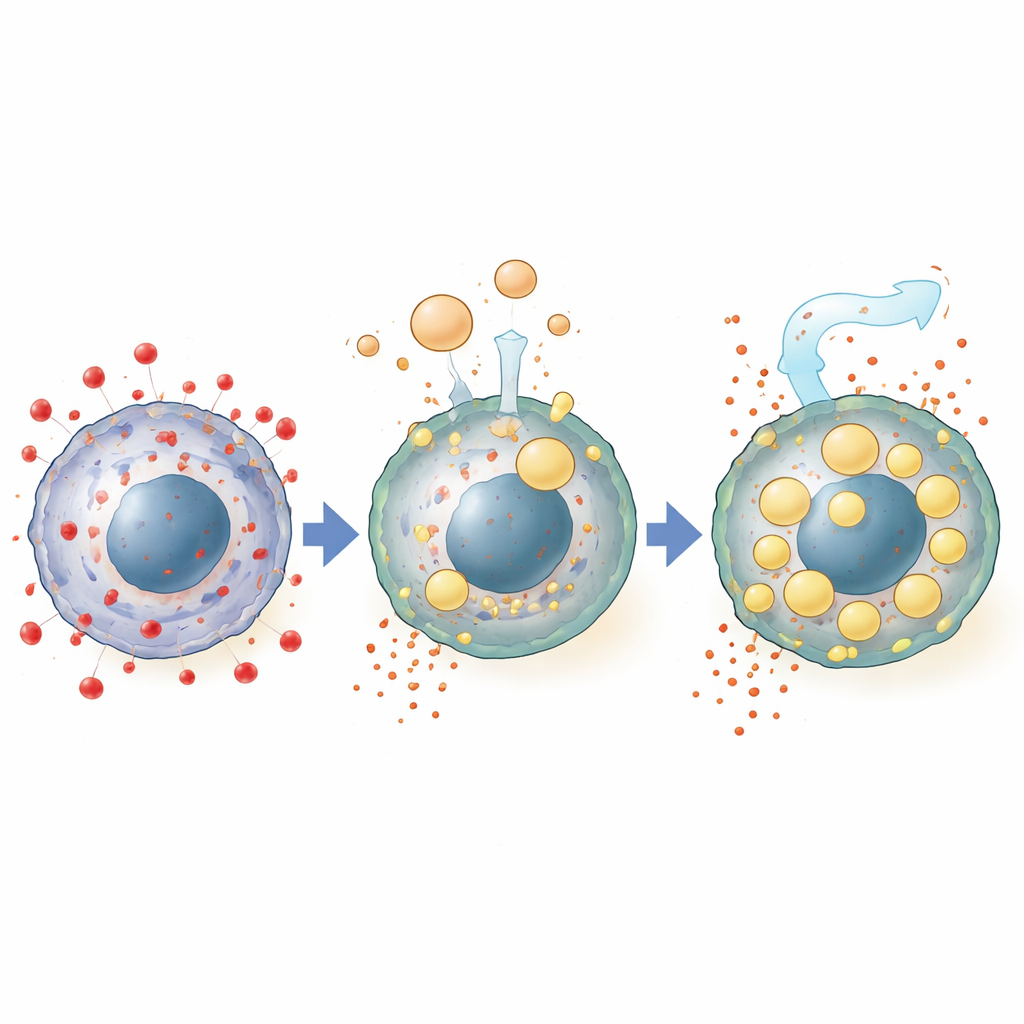
为查明腹水中何种成分具备这一能力,科学家去除了不同组分。去除脂质(而非蛋白质或小分子)会消除保护作用。详细的化学分析显示,暴露于腹水的癌细胞积累了大量中性脂肪,尤其是甘油三酯和胆固醇酯,其中许多种类与腹水本身存在的脂质相匹配。这些脂肪被封装进细胞内大量的脂质滴,脂质滴被认为是保护易损脂肪酸的安全储存库。阻断脂质滴的形成,或干扰细胞从高密度脂蛋白颗粒摄取脂质的关键通路,会降低这种保护效应,直接将铁死亡抗性与脂肪摄入和储存联系起来。
重编程细胞代谢与铁摄取
腹水的作用不仅是直接提供脂质。基因活性测定显示,腹水抑制了一种名为HMGCS2的线粒体酶,该酶通常有助于脂肪酸的燃烧。该酶活性降低使细胞从脂肪分解转向将脂肪储存在脂质滴中,进一步缓冲其免受损伤。与此同时,腹水降低了细胞表面铁转运受体TFRC的水平,减少了促进铁死亡的铁进入。丰含于卵巢癌腹水中的脂肪酸油酸可复制这些效应:降低TFRC活性和细胞内铁,同时在铁死亡压力下增强细胞生存。
将保护机制转化为治疗契机
因为这种屏蔽依赖于改变的脂质处理,研究者测试了被称为贝特类(纤维酸类)的药物,这类药通过激活名为PPARα的蛋白开关来降低血脂。贝扎特贝类和相关化合物部分逆转了腹水引起的脂质积累,缩小了脂质滴,并在细胞、类器官和小鼠模型中恢复了对诱导铁死亡药物的敏感性。当癌细胞在注入小鼠前同时经铁死亡诱导剂和贝扎特贝预处理,腹膜肿瘤生长减缓且小鼠存活期延长,这提示已有的靶向脂质的药物可能有助于削弱腹水赋予转移性癌细胞的优势。
对患者的意义
该研究表明,腹水并非晚期卵巢癌的被动副产物,而是一个主动的伙伴,通过保护肿瘤细胞免受一种以脂质为核心的细胞死亡方式来促进其生存。通过提供脂质、促进其安全储存并降低铁摄取,腹水帮助游离的癌细胞在腹腔中存活并形成新的种植灶。同时,这项研究强调了这种对脂质处理与铁控制的依赖可能构成一种脆弱性。经过谨慎设计的治疗策略——包括可能可重新利用的降脂药物——或许有一天能剥夺卵巢癌细胞的这种保护,使其对治疗更为敏感。
引用: Setayeshpour, Y., Chen, SY., Dayanidhi, D.L. et al. Ascites protects against ferroptosis and enables the peritoneal growth of ovarian cancer. Nat Commun 17, 4190 (2026). https://doi.org/10.1038/s41467-026-72116-1
关键词: 卵巢癌, 腹水, 铁死亡, 脂质滴, 贝特类(纤维酸类)