Clear Sky Science · it
L’ascite protegge dalla ferroptosi e favorisce la crescita peritoneale del cancro ovarico
Perché il fluido addominale conta
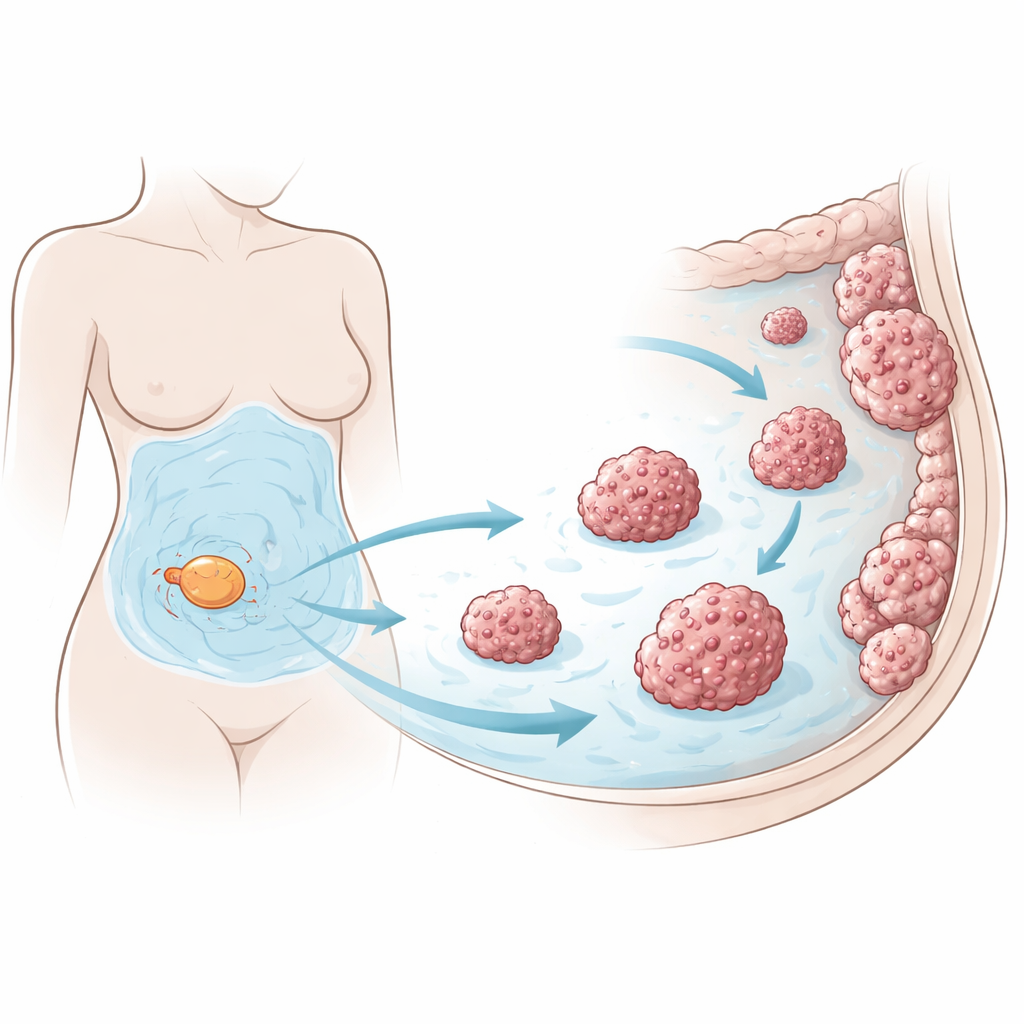
Molte donne con cancro ovarico avanzato sviluppano un accumulo di liquido nella cavità addominale chiamato ascite. I medici sanno da tempo che questo fluido indica una malattia grave, ma non esattamente come aiuti i tumori a sopravvivere e a diffondersi. Questo studio svela come componenti dell’ascite proteggano le cellule del cancro ovarico da un particolare tipo di morte cellulare e, così facendo, favoriscano la crescita del tumore sulla parete addominale.
Una collaborazione pericolosa tra fluido e tumore
Il cancro ovarico spesso si diffonde sulla superficie interna dell’addome, una regione chiamata peritoneo. Con il progredire della malattia, vasi sanguigni permeabili fanno accumulare litri di fluido ascitico in questa cavità. I ricercatori si sono concentrati su una vulnerabilità delle cellule di cancro ovarico: sono molto suscettibili alla ferroptosi, una forma di morte cellulare guidata dal ferro e dal danno ai lipidi delle membrane cellulari. Poiché le cellule tumorali staccate e in sospensione nell’addome dovrebbero essere particolarmente esposte a questo stress, il gruppo ha indagato come riescano a restare vive abbastanza a lungo da dare origine a nuovi tumori.
L’ascite protegge le cellule da uno stress letale
Utilizzando linee cellulari umane di cancro ovarico, cellule tumorali fresche prelevate da pazienti e piccoli organoidi tridimensionali coltivati dal tessuto dei pazienti, il gruppo ha esposto le cellule a farmaci che normalmente inducono la ferroptosi. Hanno scoperto che anche piccole quantità di ascite proveniente da donne con cancro ovarico proteggevano in modo marcato tutti questi modelli dalla morte ferroptotica, senza però proteggerli da altri tipi di farmaci tossici. Nei topi, l’iniezione di cellule di cancro ovarico insieme ad ascite umana portò a un carico tumorale maggiore nella cavità peritoneale, a minori segnali di danno lipidico nei tumori e a una sopravvivenza ridotta, indicando che l’effetto protettivo del fluido opera anche in animali vivi e non solo in colture.
Un carico ricco di grassi nel fluido guida la protezione
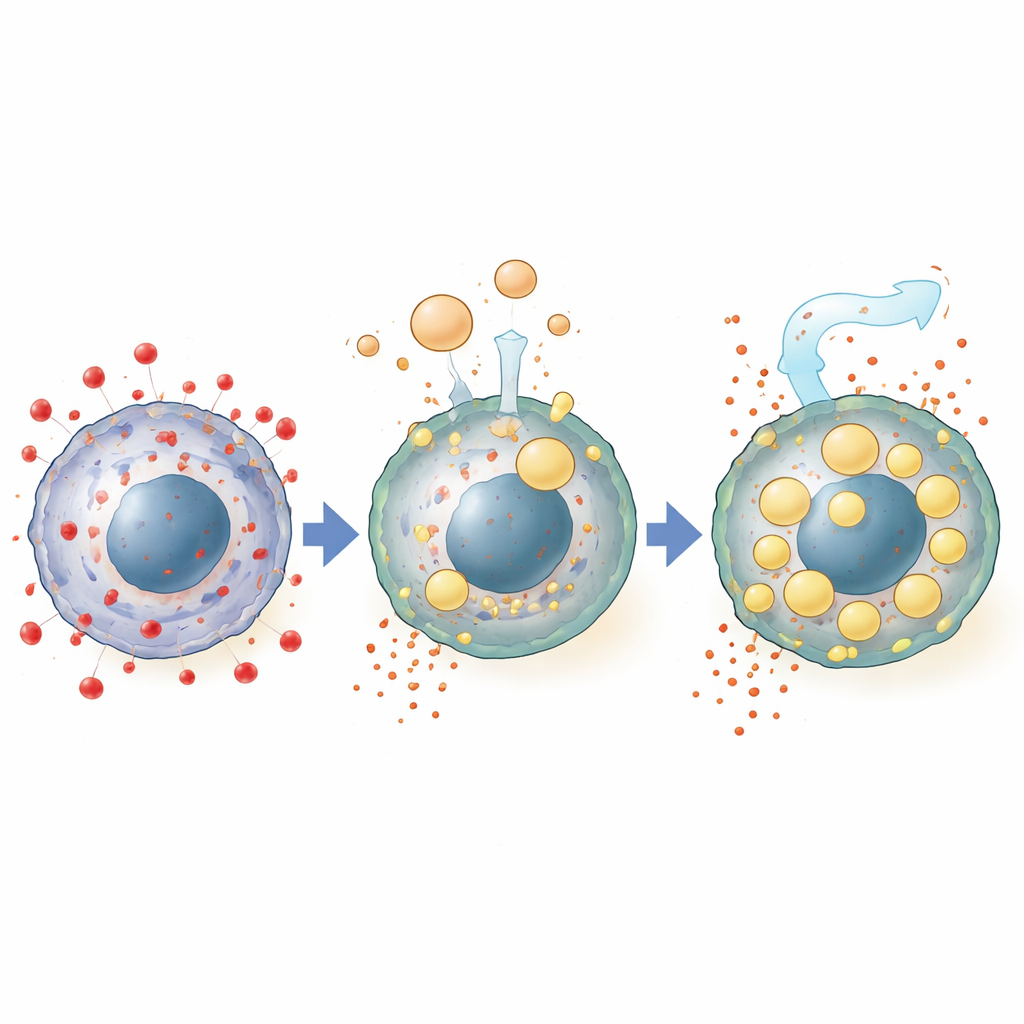
Per individuare cosa nell’ascite portasse questa capacità, gli scienziati rimossero diversi componenti. Eliminare i lipidi, ma non le proteine o le piccole molecole, annullò la protezione. Un profilo chimico dettagliato mostrò che le cellule esposte all’ascite accumulavano grandi quantità di grassi neutri, in particolare trigliceridi ed esteri del colesterolo, molti dei quali corrispondevano a specie presenti nel fluido stesso. Questi lipidi si impaccavano in numerose gocce lipidiche all’interno delle cellule, strutture ritenute depositi sicuri per gli acidi grassi vulnerabili. Bloccare la formazione di queste gocce, o interferire con le vie chiave di captazione dei grassi a partire dalle particelle lipoproteiche ad alta densità presenti nel fluido, ridusse l’effetto protettivo, collegando direttamente la resistenza alla ferroptosi all’importazione e allo stoccaggio dei lipidi.
Rimodellamento del metabolismo cellulare e dell’ingresso del ferro
L’ascite fece più che donare semplicemente grassi. Le misure dell’espressione genica rivelarono che il fluido sopprimeva un enzima mitocondriale chiamato HMGCS2, che normalmente sostiene l’ossidazione degli acidi grassi. La perdita di questo enzima spostò le cellule lontano dalla degradazione dei lipidi e verso il loro accumulo in gocce, proteggendole ulteriormente dal danno. Allo stesso tempo, l’ascite abbassò i livelli del recettore della transferrina TFRC sulla superficie cellulare, riducendo l’afflusso di ferro che alimenta la ferroptosi. L’acido oleico, abbondante nell’ascite del cancro ovarico, poté mimare questi effetti, abbassando l’attività di TFRC e il ferro intracellulare mentre aumentava la sopravvivenza sotto stress ferroptotico.
Trasformare la protezione in un’opportunità terapeutica
Poiché questa protezione dipende da un alterato trattamento dei grassi, i ricercatori testarono farmaci detti fibrati, comunemente usati per abbassare i lipidi ematici attivando un interruttore proteico chiamato PPARα. Bezafibrato e composti affini invertirono parzialmente l’accumulo lipidico indotto dall’ascite, ridussero le gocce lipidiche e ripristinarono la sensibilità ai farmaci che inducono la ferroptosi in cellule, organoidi e modelli murini. Quando le cellule tumorali furono pretrattate sia con un agente che induce la ferroptosi sia con bezafibrato prima di essere impiantate nei topi, la crescita tumorale peritoneale rallentò e gli animali vissero più a lungo, suggerendo che farmaci esistenti mirati ai lipidi potrebbero aiutare a sminuire i vantaggi che l’ascite conferisce alle cellule metastatiche.
Cosa significa per i pazienti
Questo lavoro mostra che l’ascite non è solo un sottoprodotto passivo del cancro ovarico avanzato, ma un partner attivo che protegge le cellule tumorali da una specifica forma di morte cellulare basata sui lipidi. Donando lipidi, promuovendo il loro stoccaggio sicuro e riducendo l’assorbimento di ferro, il fluido aiuta le cellule tumorali fluttuanti a sopravvivere nel loro viaggio attraverso l’addome e a formare nuovi impianti. Allo stesso tempo, lo studio mette in luce che questa dipendenza dalla gestione dei grassi e dal controllo del ferro può rappresentare una debolezza. Terapie progettate con cura che perturbino questo equilibrio, includendo potenzialmente farmaci ipolipemizzanti riproposti, potrebbero un giorno privare le cellule del cancro ovarico della loro protezione e renderle più vulnerabili al trattamento.
Citazione: Setayeshpour, Y., Chen, SY., Dayanidhi, D.L. et al. Ascites protects against ferroptosis and enables the peritoneal growth of ovarian cancer. Nat Commun 17, 4190 (2026). https://doi.org/10.1038/s41467-026-72116-1
Parole chiave: cancro ovarico, ascite, ferroptosi, gocce lipidiche, fibrati