Clear Sky Science · pl
Płyn w jamie brzusznej chroni przed ferroptoza i umożliwia wzrost raka jajnika w otrzewnej
Dlaczego płyn w brzuchu ma znaczenie
Wiele kobiet z zaawansowanym rakiem jajnika rozwija nagromadzenie płynu w jamie brzusznej zwane puchliną (ascites). Lekarze od dawna wiedzą, że obecność tego płynu świadczy o poważnej chorobie, lecz nie do końca jasne było, w jaki sposób pomaga on guzom przetrwać i się rozprzestrzeniać. To badanie ujawnia, jak składniki puchliny chronią komórki raka jajnika przed określonym typem śmierci komórkowej i w ten sposób wspierają wzrost nowotworu na wyściółce jamy brzusznej.
Niebezpieczne partnerstwo między płynem a rakiem
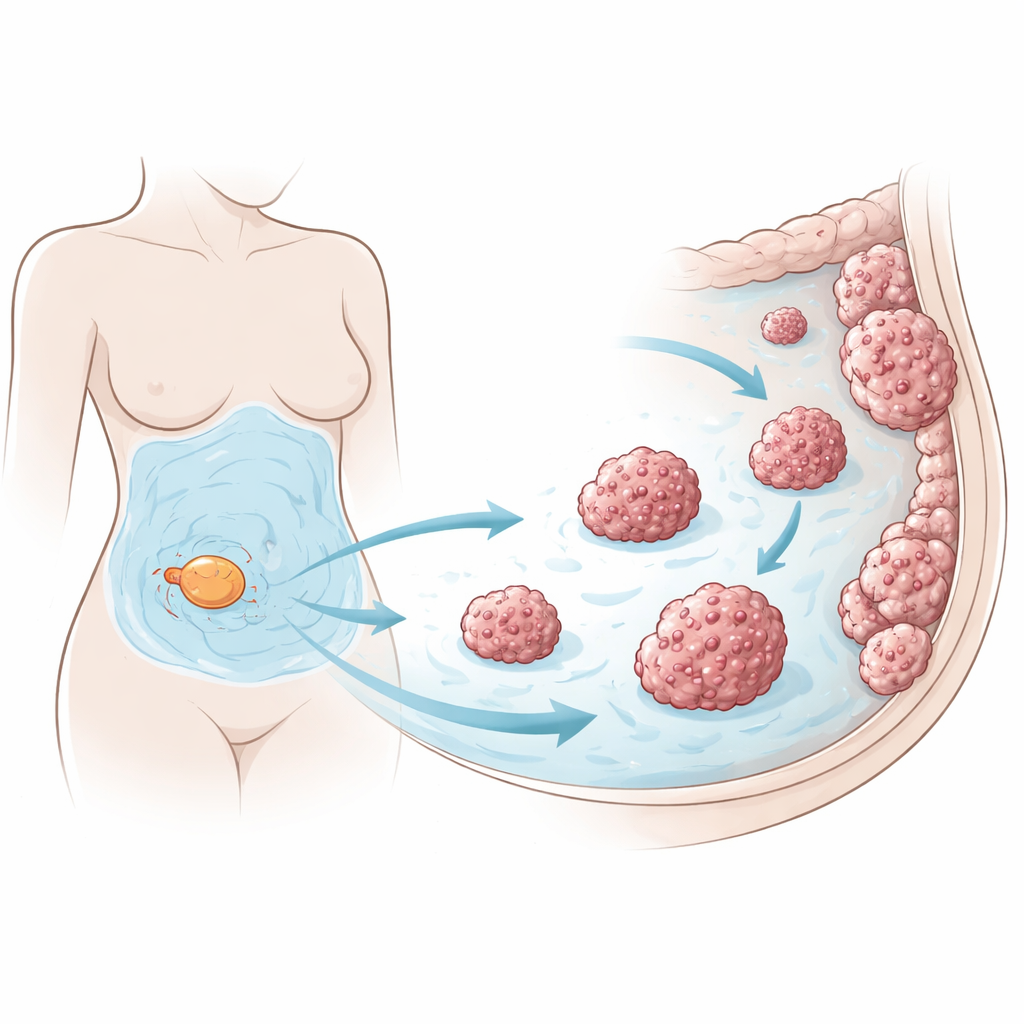
Rak jajnika często szerzy się po wewnętrznej powierzchni jamy brzusznej, zwanej otrzewną. W miarę postępu choroby nieszczelne naczynia krwionośne powodują gromadzenie się litrów puchliny w tej przestrzeni. Badacze skupili się na słabości komórek raka jajnika: są one wysoce podatne na ferroptozę, formę śmierci komórkowej napędzaną żelazem i uszkodzeniem lipidów w błonach komórkowych. Ponieważ oderwane komórki nowotworowe unoszące się w jamie brzusznej powinny być szczególnie narażone na ten stres, zespół badał, jak udaje im się przeżyć wystarczająco długo, by zainicjować nowe ogniska choroby.
Puchlina chroni komórki przed śmiertelnym stresem
Wykorzystując linie komórkowe raka jajnika pochodzące od ludzi, świeże komórki nowotworowe od pacjentek oraz maleńkie trójwymiarowe organoidy hodowane z tkanki pacjentek, zespół wystawił komórki na działanie leków, które zazwyczaj wywołują ferroptozę. Stwierdzono, że nawet niewielkie ilości puchliny od kobiet z rakiem jajnika silnie chroniły wszystkie te modele przed śmiercią ferroptotyczną, nie chroniąc ich jednocześnie przed innymi rodzajami toksycznych leków. U myszy wstrzyknięcie komórek raka jajnika razem z ludzką puchliną prowadziło do większego obciążenia nowotworowego w jamie otrzewnowej, mniejszej liczby oznak uszkodzeń lipidów w guzach i krótszego przeżycia, co wskazuje, że ochronny efekt płynu działa także in vivo, nie tylko w szalce.
Tłuszczowe ładunki w płynie napędzają ochronę
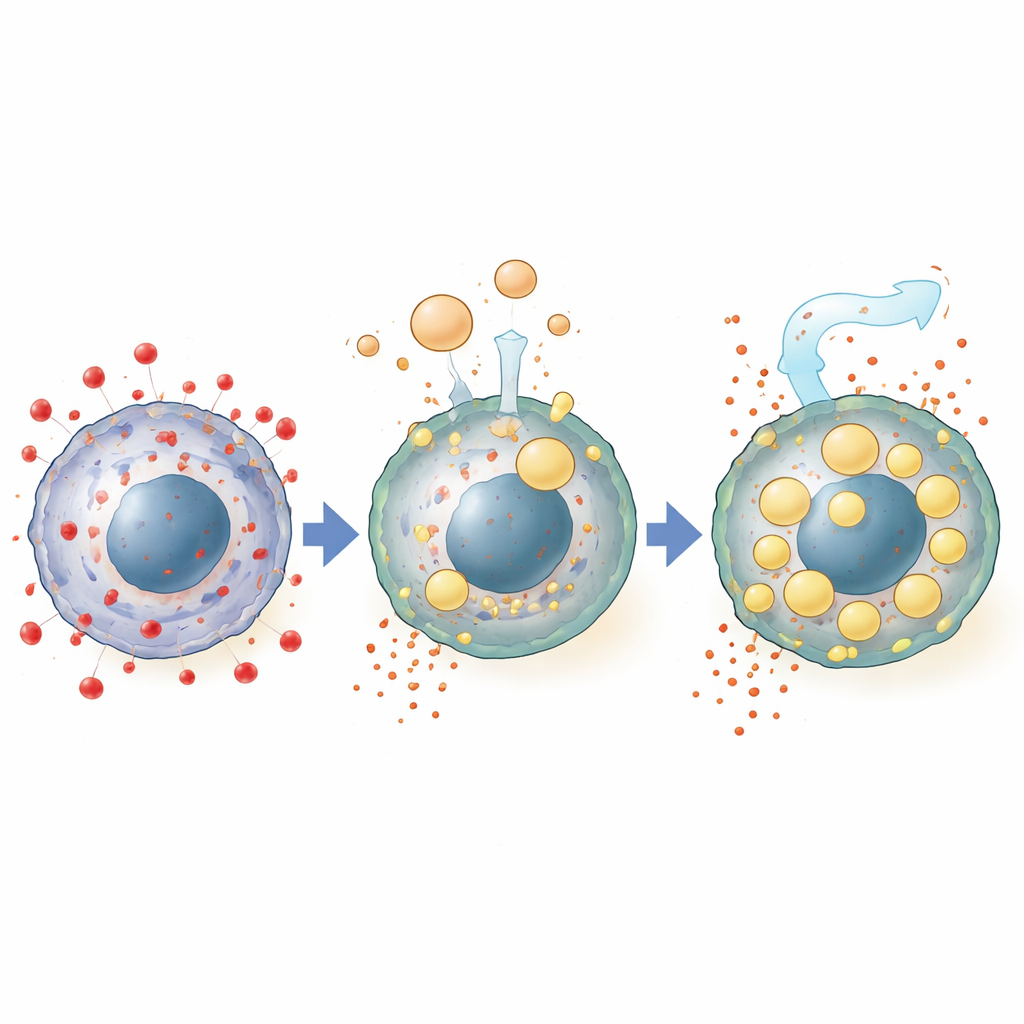
Aby ustalić, co w puchlinie niesie tę moc, naukowcy usunęli różne składniki. Usunięcie lipidów, ale nie białek ani małych cząsteczek, likwidowało ochronę. Szczegółowe profilowanie chemiczne wykazało, że komórki nowotworowe wystawione na działanie puchliny gromadziły duże ilości neutralnych tłuszczów, zwłaszcza trójglicerydów i estrów cholesterolu, z których wiele odpowiadało gatunkom obecnym w samym płynie. Te tłuszcze kumulowały się w licznych kroplach lipidowych wewnątrz komórek — strukturach uważanych za bezpieczne magazyny dla podatnych kwasów tłuszczowych. Blokowanie tworzenia tych kropli lub zakłócenie kluczowych szlaków pobierania tłuszczów z cząstek lipoprotein o dużej gęstości obecnych w płynie zmniejszało efekt ochronny, łącząc oporność na ferroptozę bezpośrednio z importem i magazynowaniem tłuszczu.
Przekierowanie metabolizmu komórki i poboru żelaza
Puchlina robiła więcej niż tylko dostarczała tłuszcze. Pomiar aktywności genów ujawnił, że płyn tłumił mitochondrialny enzym HMGCS2, który normalnie wspiera utlenianie kwasów tłuszczowych. Utrata tego enzymu przesuwała komórki od rozkładu tłuszczów w stronę ich magazynowania w kroplach lipidowych, co dodatkowo chroniło je przed uszkodzeniem. Jednocześnie puchlina obniżała poziomy receptora transferyny TFRC na powierzchni komórek, zmniejszając napływ żelaza, które napędza ferroptozę. Kwas oleinowy, obfity w puchlinie u pacjentek z rakiem jajnika, mógł naśladować te efekty — obniżał aktywność TFRC i poziom żelaza w komórkach, jednocześnie poprawiając ich przeżywalność w warunkach sprzyjających ferroptozie.
Przekształcenie ochrony w możliwość terapeutyczną
Ponieważ osłona zależy od zmienionego obchodzenia się z tłuszczami, badacze przetestowali leki zwane fibratami, stosowane powszechnie w celu obniżania lipidów we krwi przez aktywację przełącznika białkowego PPARα. Bezafibrat i związane związki częściowo odwracały nagromadzenie lipidów wywołane przez puchlinę, zmniejszały krople lipidowe i przywracały wrażliwość na leki indukujące ferroptozę w komórkach, organoidach i modelach mysich. Gdy komórki nowotworowe były wstępnie traktowane jednocześnie środkiem wywołującym ferroptozę i bezafibratem przed wprowadzeniem do myszy, wzrost guzów otrzewnowych zwalniał, a zwierzęta żyły dłużej, co sugeruje, że istniejące leki ukierunkowane na lipidy mogą pomóc osłabić przewagę, jaką puchlina daje komórkom przerzutowym.
Co to oznacza dla pacjentek
Praca ta pokazuje, że puchlina nie jest tylko biernym produktem ubocznym zaawansowanego raka jajnika, lecz aktywnym partnerem, który chroni komórki nowotworowe przed specyficzną, zależną od tłuszczów śmiercią komórkową. Poprzez dostarczanie lipidów, promowanie ich bezpiecznego magazynowania i ograniczanie poboru żelaza, płyn pomaga unoszącym się komórkom nowotworowym przetrwać podróż przez jamę brzuszną i tworzyć nowe ogniska. Jednocześnie badanie podkreśla, że to uzależnienie od gospodarki tłuszczowej i kontroli żelaza może stanowić słabość. Starannie zaprojektowane terapie, które zaburzają tę równowagę, być może włącznie z ponownym zastosowaniem leków obniżających lipidy, mogłyby w przyszłości pozbawić komórki raka jajnika ich ochrony i uczynić je bardziej podatnymi na leczenie.
Cytowanie: Setayeshpour, Y., Chen, SY., Dayanidhi, D.L. et al. Ascites protects against ferroptosis and enables the peritoneal growth of ovarian cancer. Nat Commun 17, 4190 (2026). https://doi.org/10.1038/s41467-026-72116-1
Słowa kluczowe: rak jajnika, puchlina brzuszna (ascites), ferroptoza, krople lipidowe, fibraty