Clear Sky Science · sv
Ascites skyddar mot ferroptos och möjliggör peritoneal tillväxt av ovarialcancer
Varför vätska i buken spelar roll
Många kvinnor med avancerad ovarialcancer utvecklar en ansamling av vätska i buken som kallas ascites. Läkare har länge vetat att denna vätska signalerar svår sjukdom, men inte exakt hur den hjälper tumörer att överleva och sprida sig. Denna studie avslöjar hur komponenter i ascites skyddar ovarialcancerceller från en särskild typ av celldöd och på så sätt understöder tumörväxt på bukhinnen.
Ett farligt partnerskap mellan vätska och cancer
Ovarialcancer sprider sig ofta över bukkavitetens inre yta, ett område som kallas peritoneum. När sjukdomen fortskrider orsakar läckande blodkärl att liter av ascitvätska samlas i denna hålighet. Forskarna fokuserade på en sårbarhet hos ovarialcancerceller: de är mycket mottagliga för ferroptos, en form av celldöd driven av järn och skada på fetter i cellmembran. Eftersom frisläppta cancerceller som driver runt i buken särskilt borde utsättas för denna stress, frågade teamet hur de lyckas överleva tillräckligt länge för att anlägga nya tumörer.
Ascites skyddar celler från en dödlig stress
Med hjälp av humana ovarialcancercellinjer, färska tumörceller från patienter och små tredimensionella organoider odlade från patientvävnad exponerade teamet celler för läkemedel som normalt utlöser ferroptos. De fann att även små mängder ascites från kvinnor med ovarialcancer starkt skyddade alla dessa modeller från ferroptotisk död, medan vätskan inte skyddade mot andra typer av toxiska läkemedel. Hos möss ledde injektion av ovarialcancerceller tillsammans med human ascites till större tumörbörda i peritonealhålan, färre tecken på fettskada i tumörerna och kortare överlevnad, vilket indikerar att vätskans skyddande effekt fungerar i levande djur, inte bara i skålar.
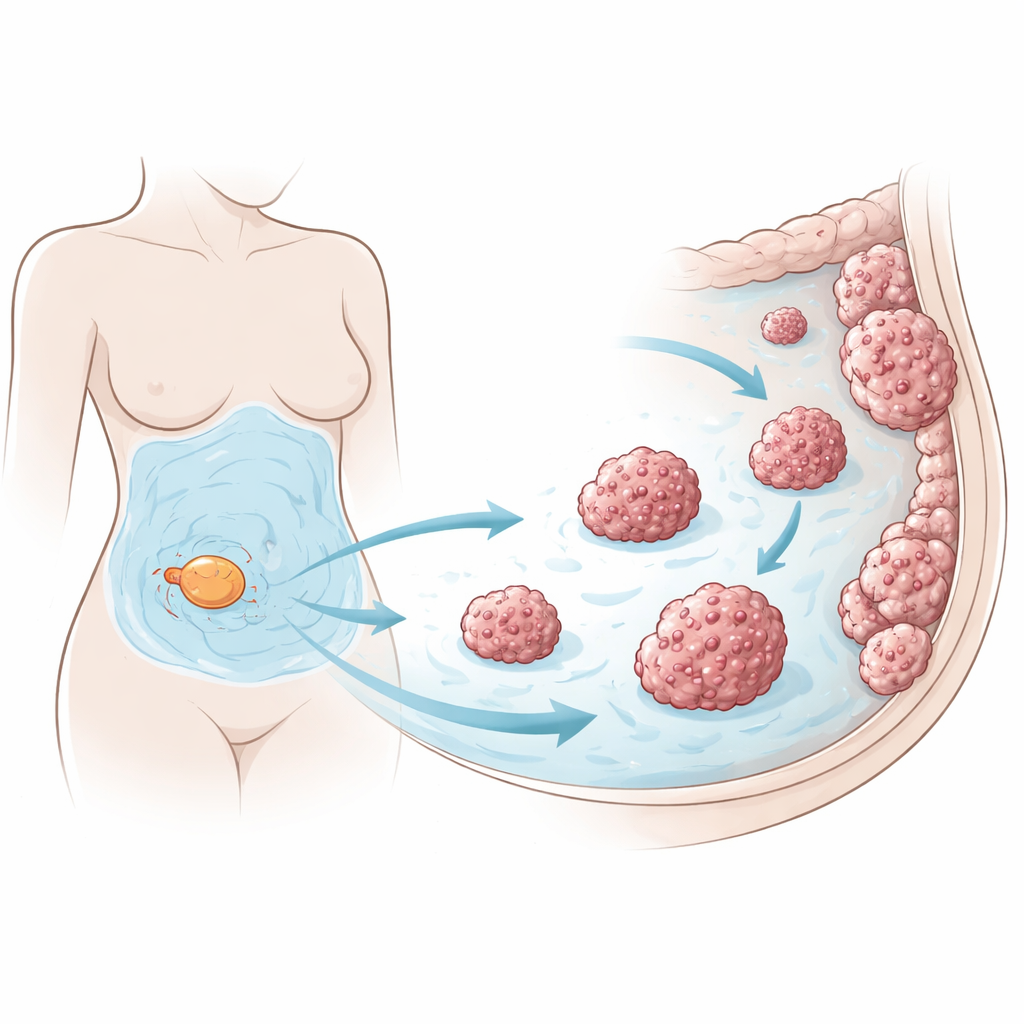
Fettrikt innehåll i vätskan driver skyddet
För att identifiera vad i ascites som bär denna förmåga tog forskarna bort olika komponenter. Att avlägsna lipider, men inte proteiner eller småmolekyler, utplånade skyddet. Detaljerad kemisk profilering visade att cancerceller exponerade för ascites ackumulerade stora mängder neutrala fetter, särskilt triglycerider och kolesterylester, många av vilka motsvarade arter som fanns i vätskan. Dessa fetter packades i talrika lipiddroppar inne i cellerna, strukturer som förmodas fungera som säkra förråd för utsatta fettsyror. Att blockera bildandet av dessa droppar eller störa viktiga vägar för upptag av fetter från högdensitetslipoproteinpartiklar i vätskan minskade det skyddande utfallet, vilket knyter ferroptosresistens direkt till fettimport och lagring.
Omläggning av cellmetabolism och järnupptag
Ascites gjorde mer än att bara donera fetter. Mätningar av genaktivitet visade att vätskan dämpade ett mitokondriellt enzym kallat HMGCS2, som normalt stödjer förbränning av fettsyror. Förlust av detta enzym försköt cellerna från fettnedbrytning mot att lagra fetter i droppar, vilket ytterligare buffrade dem mot skada. Samtidigt sänkte ascites nivåerna av transferrinreceptorn TFRC på cellytan, vilket minskade järninflödet som hjälper till att driva ferroptos. Fettsyran oleinsyra, riklig i ascites vid ovarialcancer, kunde efterlikna dessa effekter genom att sänka TFRC-aktivitet och järninnehåll i celler samtidigt som den förbättrade överlevnad under ferroptotisk stress.
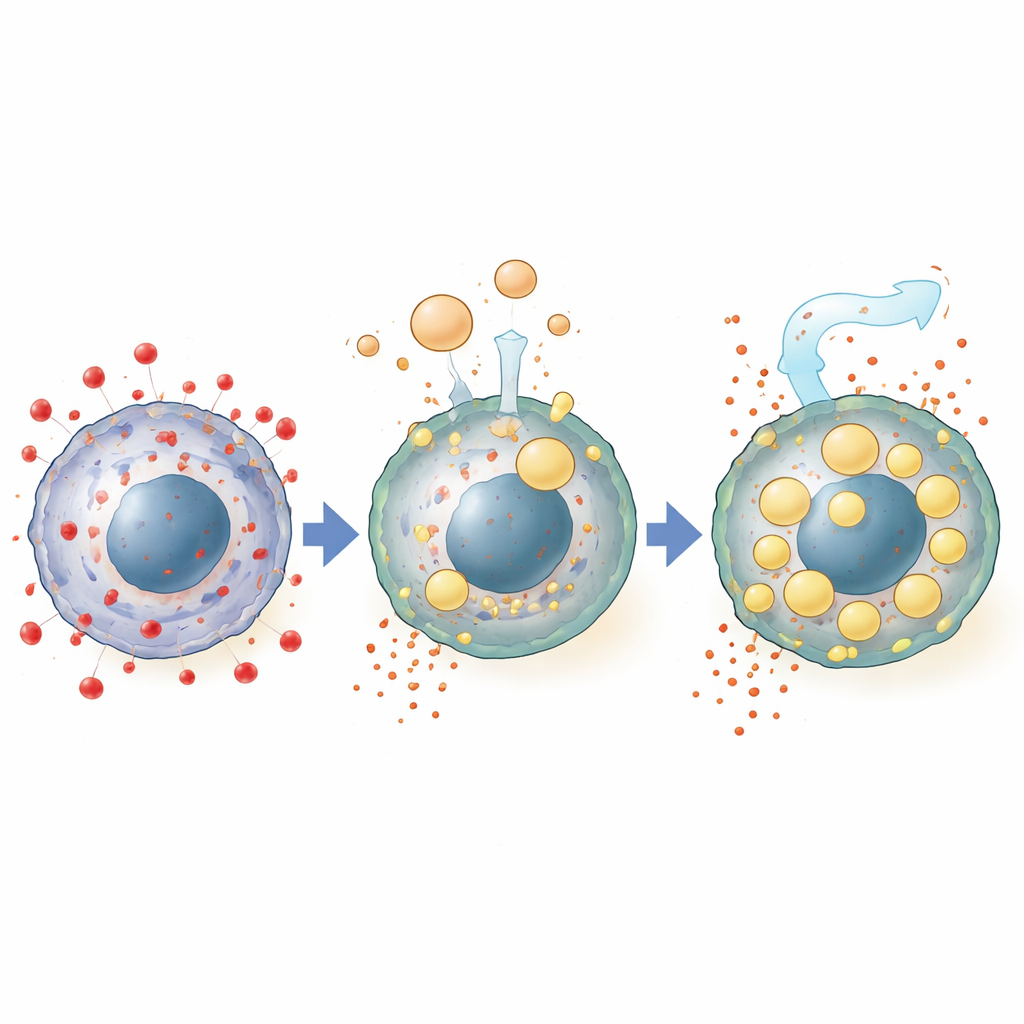
Att vända skydd till en behandlingsmöjlighet
Eftersom detta skydd beror på förändrad fettbehandling testade forskarna läkemedel kallade fibrater, som ofta används för att sänka blodlipider genom att aktivera en proteinswitch vid namn PPARα. Bezafibrat och relaterade föreningar reverserade delvis fettuppbyggnaden orsakad av ascites, krympte lipiddroppar och återställde känsligheten för ferroptosinducerande läkemedel i celler, organoider och musmodeller. När cancerceller förbehandlades med både ett ferroptosutlösande medel och bezafibrat innan de infördes i möss, bromsades peritoneal tumörtillväxt och djuren levde längre, vilket tyder på att befintliga läkemedel som riktar sig mot lipider kan hjälpa till att undergräva de fördelar ascites ger metastaserande cancerceller.
Vad detta betyder för patienter
Denna studie visar att ascites inte bara är en passiv biprodukt av avancerad ovarialcancer, utan en aktiv partner som skyddar tumörceller från en särskild form av fettbaserad celldöd. Genom att donera lipider, främja säker lagring av dem och dämpa järnupptaget hjälper vätskan fritt flytande cancerceller att överleva resan över buken och bilda nya implantat. Samtidigt belyser studien att detta beroende av fettmetabolism och järnkontroll kan vara en svaghet. Noggrant utformade behandlingar som rubbar denna balans, möjligen inklusive omdirigerade lipidsänkande läkemedel, skulle en dag kunna hjälpa till att beröva ovarialcancerceller deras skydd och göra dem mer sårbara för behandling.
Citering: Setayeshpour, Y., Chen, SY., Dayanidhi, D.L. et al. Ascites protects against ferroptosis and enables the peritoneal growth of ovarian cancer. Nat Commun 17, 4190 (2026). https://doi.org/10.1038/s41467-026-72116-1
Nyckelord: äggstockscancer, ascites, ferroptos, lipiddroppar, fibrater