Clear Sky Science · zh
唐氏综合征相关髓系白血病的单细胞转录进化
这项研究对家庭的重要性
患有唐氏综合征的儿童发生一种罕见血癌——唐氏综合征髓系白血病(ML-DS)的风险明显增加。在出现白血病之前,许多婴儿会经历一种短暂的癌前状态,通常能自行消退。理解为何部分儿童会进展为真正的白血病而另一些不会,对实现更早的诊断、更温和的治疗乃至可能的预防至关重要。本研究利用强大的单细胞基因学工具,细致观察唐氏综合征中正常血细胞如何逐步转变为白血病细胞。
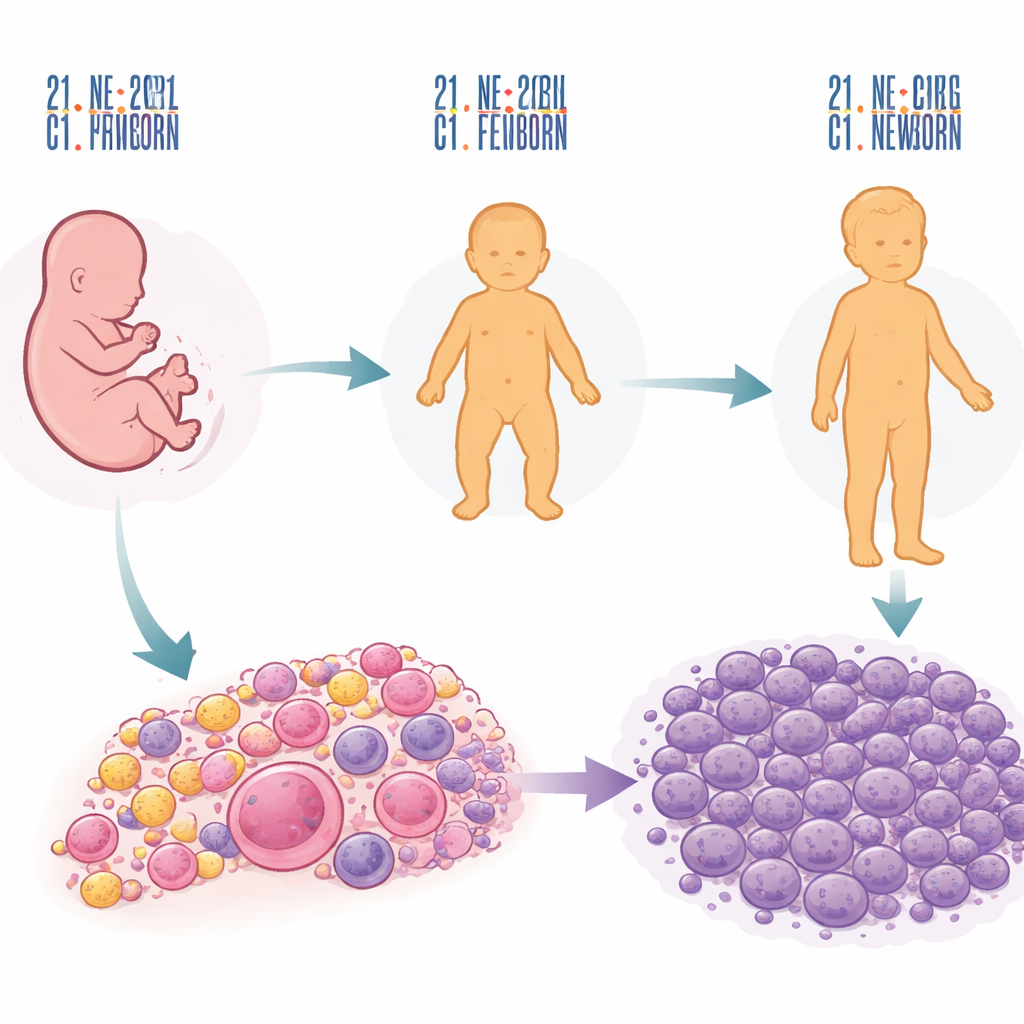
从额外染色体到早期预警阶段
故事始于导致唐氏综合征的额外21号染色体。这一额外染色体在胎儿期微妙地重塑了造血过程,尤其是在生成早期血细胞的肝脏中。通过比较具有正常与异常染色体构型的胎肝样本,研究者发现21号三体使发育中血细胞的比例发生偏移:未来分化为血小板和红细胞的细胞群扩增,而早期 B 细胞减少。其他异常染色体构型也会扰乱血液发育,但方式不同,表明21号染色体的影响具有特异性。然而,仅靠额外染色体本身,只改变了后来定义白血病的少数基因。
一个改变平衡的关键突变
下一步的关键在于名为 GATA1 的基因,该基因通常帮助未成熟血细胞分化为健康的红细胞和血小板。许多唐氏综合征婴儿会获得 GATA1 的突变,产生一种截短的蛋白质形式。这一改变导致一种称为短暂性异常髓样增生(TAM)的现象,即未成熟血细胞短期激增。通过单细胞 RNA 测序,研究团队表明 GATA1 突变同时重编程了数百个基因的活动,使细胞远离红细胞谱系,转向类似巨核细胞和髓系的状态。值得注意的是,完全形成的 ML-DS 中观察到的基因变化中,有超过五分之四在早期的 TAM 阶段就已出现,表明 GATA1 是驱动类白血病程序的主要因素。
从短暂增生到真正白血病
并非所有出现 TAM 的儿童都会发展为白血病,很多病例在不经治疗的情况下自行好转。为弄清促成转变的因素,研究者将 ML-DS 儿童的癌细胞与未进展的 TAM 儿童的细胞进行比较。他们发现一组最终的基因改变,跨 ML-DS 患者共有,并叠加在 GATA1 程序之上。许多这些基因是已知的癌症生长和存活相关基因。有意思的是,这个“ML-DS 模块”在其他儿童血液癌症中也有激活,包括那些与唐氏综合征无关的病例,提示它反映的是一种更普遍的癌症特征而非 ML-DS 独有。随后病情复发或恶化的儿童在早期就已经表现出该模块更强的激活,暗示它可能有助于早期识别高风险病例。
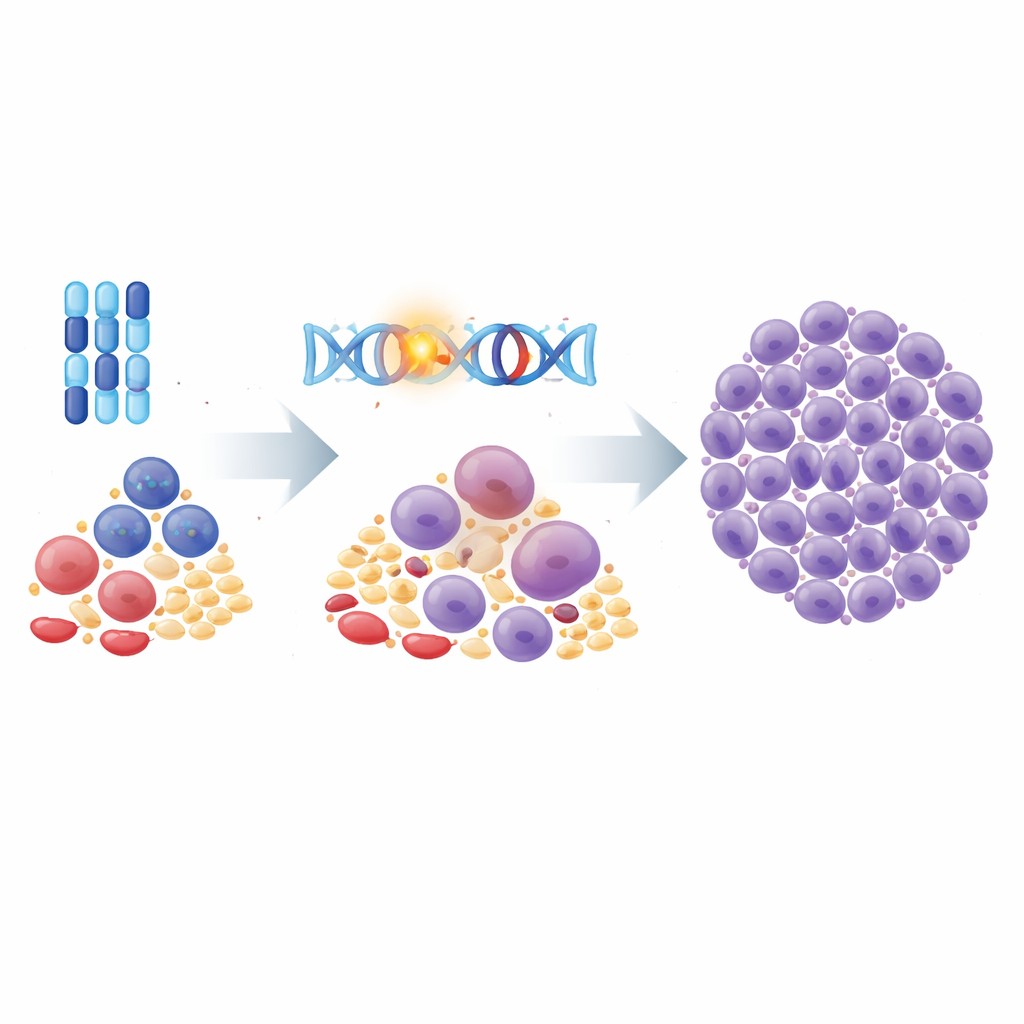
随时间追踪危险克隆
团队难得获得两例特别侵袭性 ML-DS 儿童的多次样本:一例两次复发,另一例从一开始就对治疗耐药。通过将全基因组 DNA 测序与单细胞 RNA 数据结合,他们重建了癌细胞随时间变化的家系树。在一名儿童中,复发细胞形成了从共同祖先并行进化的独立分支,但所有分支都保留了相同的 GATA1 驱动基因程序,并共享可能帮助其在化疗中存活的额外改变。在另一名儿童中,一个带有第17号染色体缺失并影响著名“守护者”基因 TP53 的隐匿子克隆在诊断时就存在,并在治疗后占据主导地位。即便在这些晚期阶段,GATA1 突变的指纹在每个白血病细胞中仍然明显。
这对未来治疗意味着什么
综合而言,该研究表明:尽管额外的21号染色体奠定了基础,GATA1 突变书写了唐氏综合征相关白血病的大部分脚本,而且随着疾病演进和产生耐药,该脚本依然保持。由短暂性增生跃升为真正癌症的最终步骤涉及一个额外的、更为通用的癌症程序,这一程序在多种白血病类型中都能见到。就临床实践而言,这项工作暗示了两个有前景的方向:一是将未来疗法聚焦于 GATA1 驱动的基因网络——它似乎是癌细胞的持续薄弱点;二是利用更广泛的 ML-DS 基因特征来识别哪些短暂病程的婴儿更有可能进展为白血病,从而实现更精准的护理分层。
引用: Trinh, M.K., Schuschel, K., Issa, H. et al. Single cell transcriptional evolution of myeloid leukemia of Down syndrome. Nat Commun 17, 3474 (2026). https://doi.org/10.1038/s41467-026-71707-2
关键词: 唐氏综合征白血病, GATA1 突变, 单细胞 RNA 测序, 短暂性异常髓样增生, 儿科血液癌症