Clear Sky Science · he
התפתחות תעתיקית בתא יחיד של לויקמיה מיולואידית בתסמונת דאון
מדוע המחקר הזה חשוב למשפחות
לילדים עם תסמונת דאון יש סיכון גבוה בהרבה לפתח סרטן דם נדיר הנקרא לויקמיה מיולואידית של תסמונת דאון (ML-DS). לפני הופעת הלויקמיה, רבים מהתינוקות עוברים שלב קודם‑סרטני קצר שברוב המקרים נעלם מעצמו. הבנת הסיבות לכך שחלק מהילדים מתקדמים ללויקמיה מלאה בעוד אחרים לא — היא קריטית לאבחון מוקדם יותר, טיפולים מתונים יותר ואולי אף למניעת סרטן. המחקר משתמש בכלים גנטיים רבי‑עוצמה ברמת תא יחיד כדי לעקוב, בפירוט רב, כיצד תאי דם נורמליים בתסמונת דאון משתנים בהדרגה לתאי לויקמיה.
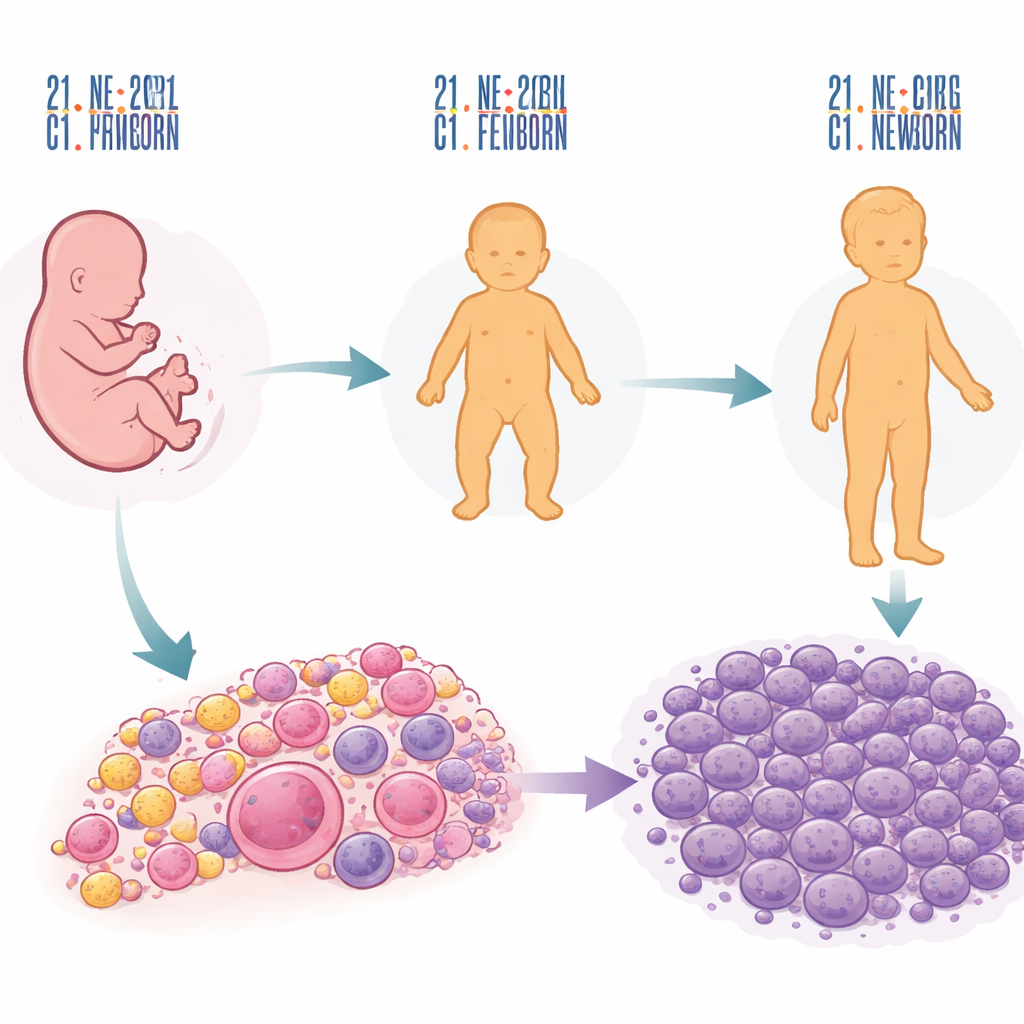
מכרומוזום נוסף עד שלב האזהרה המוקדם
הסיפור מתחיל עם העותק הנוסף של כרומוזום 21 שגורם לתסמונת דאון. הכרומוזום הנוסף מעצב בעדינות את יצירת הדם בעוב, במיוחד בכבד העוברי שבו נוצרים תאי דם מוקדמים. בהשוואת דגימות כבד עוברי עם דפוסי כרומוזומים נורמליים ובלתי‑נורמליים, החוקרים מצאו כי תראיזומיה 21 מזיזת את האיזון של תאי הדם המתפתחים: תאים שעומדים להפוך לטסיות ותאי דם אדומים מתרחבים, בעוד תאי B המוקדמים נדירים יותר. דפוסי כרומוזומים לא שגרתיים אחרים גם הם הפריעו להתפתחות הדם, אך בדרכים שונות, מה שמרמז שההשפעה של כרומוזום 21 היא יחסית ספציפית. עם זאת, לבדו הכרומוזום הנוסף משנה רק חלק קטן מהגנים שיתבררו מאוחר יותר כמאפייני הלויקמיה.
מוטציה מרכזית שמטה את המאזן
הצעד הקריטי הבא כולל את הגן GATA1, שתפקידו לכוון תאים דמויי‑עובר להפוך לתאי דם אדומים וטסיות בריאים. אצל רבים מהתינוקות עם תסמונת דאון מופיעה מוטציה ב‑GATA1 שמייצרת גרסה מקוצרת של החלבון. שינוי זה מוביל למצב שנקרא מיאלופתיה חריגה חולפת (TAM), שבו יש פרץ זמני של תאים גדלים לא בוגרים. באמצעות ריצוף RNA בתא יחיד הראו החוקרים שמוטציית GATA1 משנה בו־זמנית את הפעילות של מאות גנים, ודוחפת תאים הרחק מהתפתחות לתאי דם אדומים וכיוון למצב דמוי מגאקאריוציטים ומיולואידי. באופן מרשים, יותר מארבעה מחמישה מהשינויים הגנטיים שנצפו ב‑ML‑DS המלא כבר קיימים בשלב ה‑TAM המוקדם הזה, מה שמצביע על כך ש‑GATA1 הוא הנהג המרכזי של התוכנית הדמוית־לויקמיה.
מפרץ זמני עד לויקמיה אמיתית
לא כל הילדים עם TAM מפתחים לויקמיה, ורבים מהמקרים נפתרים ללא טיפול. כדי להבין מה משלים את המעבר, השוו החוקרים את תאי הסרטן מילדים עם ML‑DS לתאים מילדים עם TAM שלא התקדמו. הם גילו סט סופי של שינויים גנומיים משותפים לחולי ML‑DS הנבנים על תוכנית GATA1. רבים מהגנים הללו ידועים כלוקחים חלק בצמיחת וסירוגלות סרטן. מעניין כי "מודול ML‑DS" זה היה פעיל גם בסוגי סרטן דם אחרים בילדות, כולל כאלה שאינם קשורים לתסמונת דאון, מה שמרמז שהוא לוכד חתימת סרטן כללית ולא משהו יחידני ל‑ML‑DS. ילדים שמחלותיהם החולפות חזרו מאוחר יותר או החמירו כבר הראו הפעלה חזקה יותר של מודול זה, מרמז שייתכן שניתן להשתמש בו לזיהוי מקרים בסיכון גבוה מוקדם יותר.
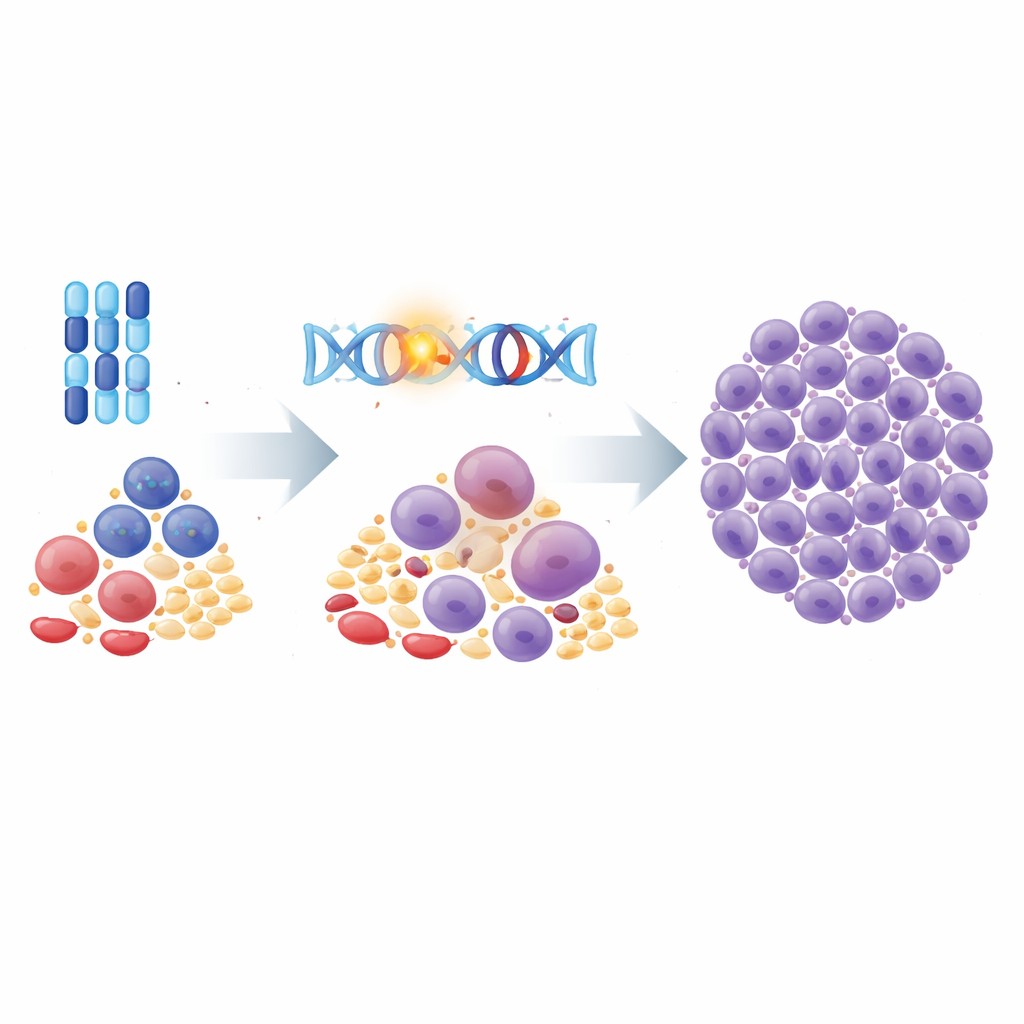
מעקב אחרי שיבוטים מסוכנים לאורך זמן
לצוות היו דגימות נדירות משני ילדים עם ML‑DS תוקפני במיוחד: אחד שחזר פעמיים ואחד שלוקמייתו התנגד לטיפול מלכתחילה. על‑ידי שילוב ריצוף גנום מלא של ה‑DNA עם נתוני RNA בתא יחיד, הם שיקום עצי משפחה של תאי סרטן לאורך זמן. אצל אחד הילדים, תאי ההישנות יצרו ענפים נפרדים שהתפתחו במקביל ממקור משותף, אך כולם שמרו על אותה תוכנית גנטית שנעה בידי GATA1 ושיתפו שינויים נוספים שסביר שעזרו להם לשרוד כימותרפיה. אצל הילד האחר, תת‑שבט מוסתר עם חסר בחלק מכרומוזום 17, שפגע בגן השומר המפורסם TP53, היה קיים כבר באבחון ודומיננטי לאחר הטיפול. גם בשלבים מתקדמים אלה, טביעת האצבע של מוטציית GATA1 נשארה חזקה בכל תא לויקמיה.
מה משמעות הממצאים לטיפול עתידי
לסיכום, המחקר מראה כי בעוד שעותק נוסף של כרומוזום 21 מכין את הבמה, מוטציית GATA1 כותבת את רוב התסריט של הלויקמיה הקשורה לתסמונת דאון, והתסריט הזה נשאר קבוע גם כשהמחלה מתפתחת ומגלה עמידות לטיפול. הקפיצה הסופית מפריחה זמנית לסרטן אמיתי כרוכה בתוכנית סרטן כללית נוספת שנראית במגוון סוגי לויקמיה. במונחים פרקטיים, הממצאים מצביעים על שני כיוונים מבטיחים: ראשית, להתמקד בעתיד בטיפולים שיוחדו לרשת הגנים המונעת ב‑GATA1, שנראית כחולשה עקבית של הסרטן; ושנית, להשתמש בחתימת הגנים הרחבה של ML‑DS כדי לזהות אילו תינוקות עם מחלה חולפת בסיכון הגבוה ביותר להתפתחות לויקמיה, כדי להתאים את הטיפול במדויק יותר.
ציטוט: Trinh, M.K., Schuschel, K., Issa, H. et al. Single cell transcriptional evolution of myeloid leukemia of Down syndrome. Nat Commun 17, 3474 (2026). https://doi.org/10.1038/s41467-026-71707-2
מילות מפתח: לויקמיה בתסמונת דאון, מוטציית GATA1, ריצוף RNA בתא יחיד, מיאלופתיה חריגה חולפת, סרטן דם בילדים