Clear Sky Science · fr
Évolution transcriptionnelle mononucléaire de la leucémie myéloïde chez les personnes trisomiques
Pourquoi cette recherche est importante pour les familles
Les enfants ayant la trisomie 21 présentent un risque beaucoup plus élevé de développer un cancer sanguin rare appelé leucémie myéloïde associée à la trisomie 21 (ML-DS). Avant l’apparition de cette leucémie, de nombreux nourrissons traversent une phase précancéreuse de courte durée qui disparaît souvent spontanément. Comprendre pourquoi certains enfants évoluent vers une leucémie complète alors que d’autres non est crucial pour un diagnostic plus précoce, des traitements moins agressifs et, éventuellement, la prévention du cancer. Cette étude utilise des outils génétiques unicellulaires puissants pour observer, avec une grande précision, comment les cellules sanguines normales chez les personnes trisomiques se transforment progressivement en cellules leucémiques.
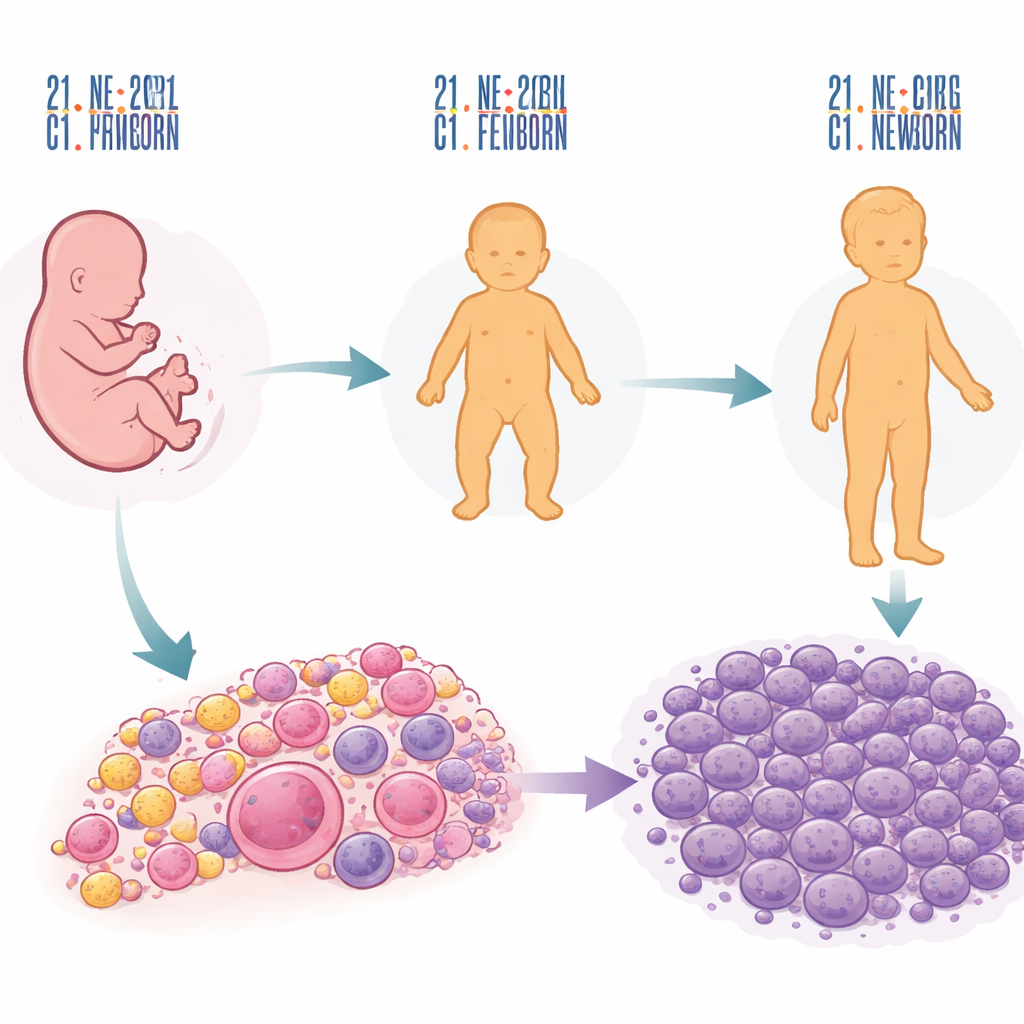
De la copie chromosomique supplémentaire à la phase d’alerte précoce
L’histoire commence avec la copie supplémentaire du chromosome 21 qui cause la trisomie 21. Ce chromosome supplémentaire reconfigure subtilement la formation du sang chez le fœtus, en particulier dans le foie, où se forment les premières cellules sanguines. En comparant des échantillons de foie fœtal avec des patrons chromosomiques normaux et anormaux, les chercheurs ont constaté que la trisomie 21 déplace l’équilibre des cellules sanguines en développement : les lignées destinées aux plaquettes et aux globules rouges s’élargissent, tandis que les premiers lymphocytes B sont réduits. D’autres anomalies chromosomiques ont également perturbé le développement sanguin, mais de manières différentes, ce qui suggère que l’effet du chromosome 21 est assez spécifique. Pris isolément, cependant, le chromosome supplémentaire modifie seulement une petite fraction des gènes qui définiront plus tard la leucémie.
Une mutation clé qui fait basculer l’équilibre
L’étape suivante cruciale implique un gène appelé GATA1, qui, normalement, guide les cellules souches sanguines immatures vers des globules rouges et des plaquettes sains. Beaucoup de nourrissons trisomiques acquièrent une mutation de GATA1 qui produit une version tronquée de la protéine. Ce changement conduit à une condition appelée myélopoïèse anormale transitoire (TAM), une augmentation temporaire de cellules sanguines immatures. Grâce au séquençage ARN unicellulaire, l’équipe a montré que la mutation GATA1 reprogramme l’activité de centaines de gènes simultanément, détournant les cellules du développement érythroïde vers un état proche des mégacaryocytes et des lignées myéloïdes. Fait remarquable, plus de quatre changements génétiques sur cinq observés dans la ML-DS franche sont déjà présents à ce stade précoce de TAM, ce qui montre que GATA1 est le principal moteur du programme de type leucémique.
De la poussée transitoire à la vraie leucémie
Tous les enfants atteints de TAM ne développent pas une leucémie, et de nombreux épisodes se résolvent sans traitement. Pour comprendre ce qui complète la transition, les chercheurs ont comparé les cellules cancéreuses d’enfants atteints de ML-DS aux cellules d’enfants présentant une TAM non évolutive. Ils ont découvert un ensemble final de changements d’expression génique partagé par les patients atteints de ML-DS qui s’ajoute au programme GATA1. Beaucoup de ces gènes sont des acteurs connus de la croissance et de la survie tumorales. Fait intéressant, ce « module ML-DS » était aussi actif dans d’autres cancers sanguins infantiles, y compris ceux non liés à la trisomie 21, ce qui suggère qu’il capture une signature cancéreuse générale plutôt qu’un élément spécifique à la ML-DS. Les enfants dont la maladie supposée transitoire est ensuite réapparue ou s’est aggravée présentaient déjà une activation plus forte de ce module, ce qui laisse penser qu’il pourrait aider à identifier tôt les cas à haut risque.
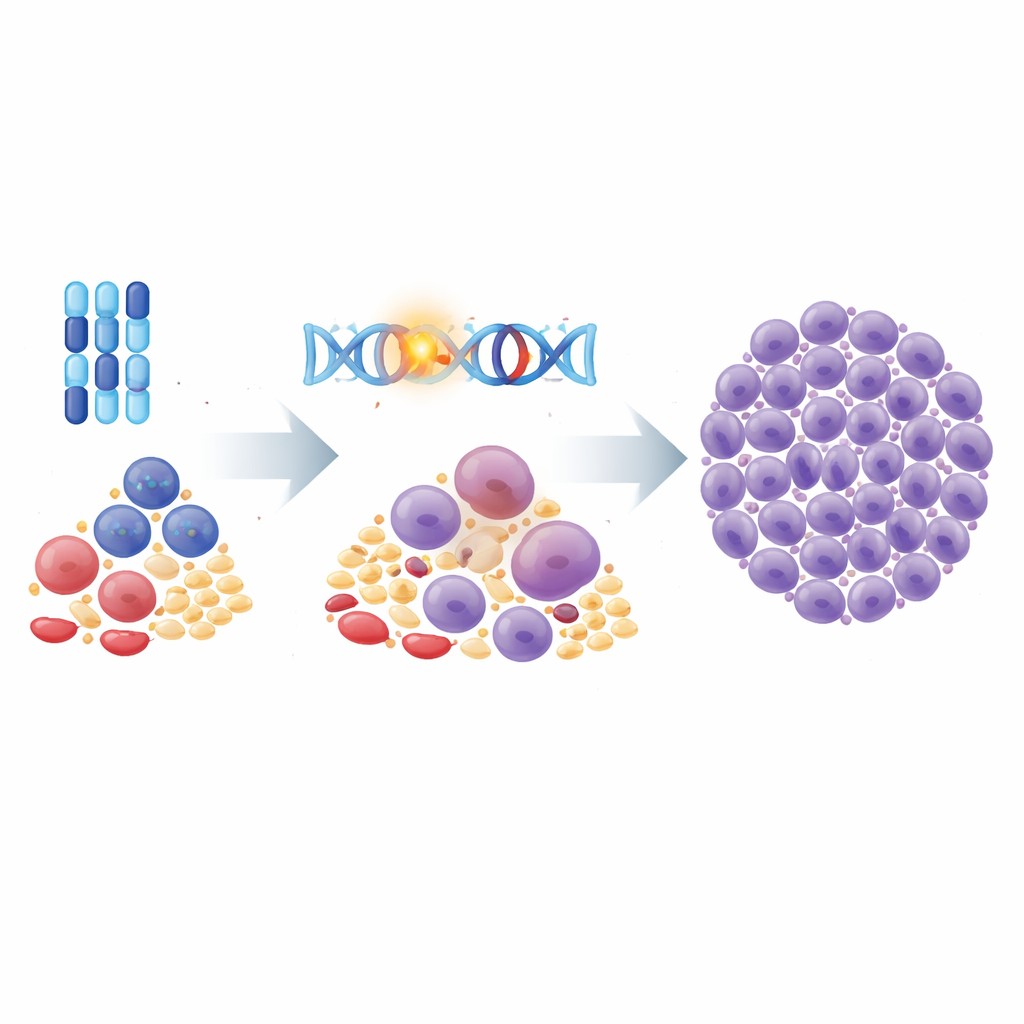
Suivre les clones dangereux au fil du temps
L’équipe a eu un accès rare à des échantillons de deux enfants présentant une ML-DS particulièrement agressive : l’un ayant rechuté deux fois et l’autre dont la leucémie a résisté au traitement dès le départ. En combinant le séquençage du génome complet avec des données ARN unicellulaires, ils ont reconstitué les arbres généalogiques des cellules cancéreuses au fil du temps. Chez un enfant, les cellules de rechute ont formé des branches séparées évoluant en parallèle à partir d’un ancêtre commun, mais elles conservaient toutes le même programme génique piloté par GATA1 et partageaient des altérations supplémentaires qui ont probablement aidé à leur survie face à la chimiothérapie. Chez l’autre enfant, un sous-clone caché avec une perte d’un fragment du chromosome 17, affectant le célèbre gène « gardien » TP53, était présent au diagnostic et a fini par dominer après le traitement. Même à ces stades avancés, l’empreinte de la mutation GATA1 restait forte dans chaque cellule leucémique.
Ce que cela signifie pour les soins futurs
Dans l’ensemble, l’étude montre que, si la copie supplémentaire du chromosome 21 prépare le terrain, la mutation GATA1 écrit la majeure partie du scénario de cette leucémie liée à la trisomie 21, et que ce scénario demeure même lorsque la maladie évolue et résiste au traitement. Le saut final de la surcroissance transitoire au véritable cancer implique un programme cancéreux additionnel, plus général, qui apparaît dans de nombreux types de leucémie. Concrètement, ce travail suggère deux pistes prometteuses : d’une part, cibler à l’avenir le réseau génique piloté par GATA1, qui semble être une vulnérabilité constante de la tumeur ; d’autre part, utiliser la signature génique plus large de la ML-DS pour repérer quels nourrissons atteints d’une maladie transitoire présentent le plus de risque d’évoluer vers une leucémie, afin d’adapter les soins de manière plus précise.
Citation: Trinh, M.K., Schuschel, K., Issa, H. et al. Single cell transcriptional evolution of myeloid leukemia of Down syndrome. Nat Commun 17, 3474 (2026). https://doi.org/10.1038/s41467-026-71707-2
Mots-clés: Leucémie associée à la trisomie 21, mutation GATA1, séquençage ARN unicellulaire, myélopoïèse anormale transitoire, cancer pédiatrique du sang