Clear Sky Science · it
Evoluzione trascrizionale a singola cellula della leucemia mieloide associata alla sindrome di Down
Perché questa ricerca è importante per le famiglie
I bambini con sindrome di Down corrono un rischio molto più elevato di sviluppare una forma rara di cancro del sangue chiamata leucemia mieloide associata alla sindrome di Down (ML-DS). Prima che la leucemia compaia, molti neonati attraversano una fase precancerosa di breve durata che spesso si risolve spontaneamente. Capire perché alcuni bambini progrediscono verso la leucemia completa mentre altri no è cruciale per una diagnosi più precoce, terapie meno invasive e, possibilmente, per prevenire il cancro. Questo studio utilizza potenti strumenti genetici a singola cellula per osservare, con grande dettaglio, come le cellule del sangue normali nella sindrome di Down si trasformano gradualmente in cellule leucemiche.
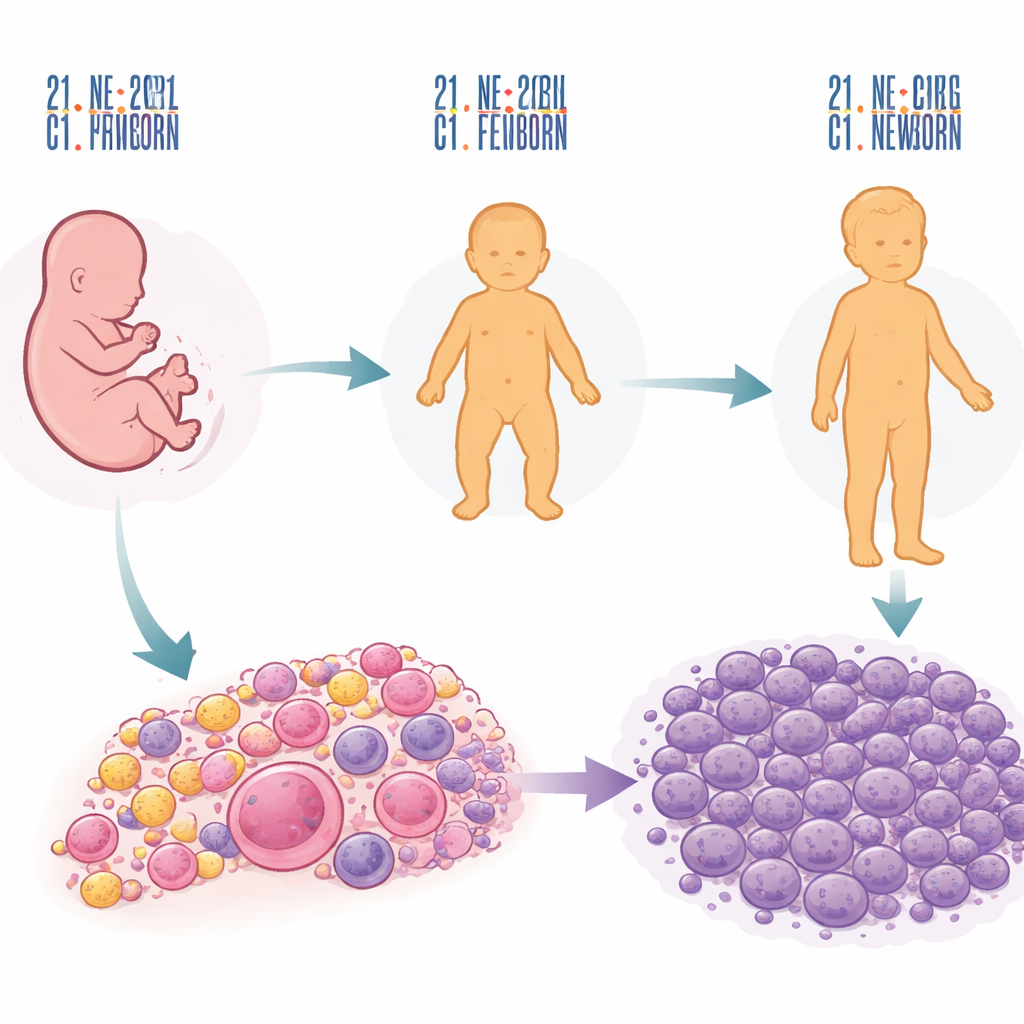
Dalla copia extra del cromosoma alla fase di allerta precoce
La storia inizia con la copia extra del cromosoma 21 che causa la sindrome di Down. Questo cromosoma in più rimodella sottilmente la formazione del sangue nel feto, in particolare nel fegato, dove si generano le prime cellule del sangue. Confrontando campioni di fegato fetale con assetti cromosomici normali e anomali, i ricercatori hanno scoperto che la trisomia 21 sposta l'equilibrio delle cellule ematiche in sviluppo: le cellule destinate a diventare piastrine ed eritrociti si espandono, mentre le prime cellule B risultano ridotte. Altri assetti cromosomici insoliti alteravano anch’essi lo sviluppo del sangue, ma in modi differenti, suggerendo che l'effetto del cromosoma 21 è piuttosto specifico. Da sola, però, la copia extra del cromosoma modifica solo una piccola frazione dei geni che più tardi caratterizzano la leucemia.
Una mutazione chiave che fa pendere la bilancia
Il passo successivo cruciale coinvolge un gene chiamato GATA1, che normalmente guida le cellule ematopoietiche immature verso la differenziazione in eritrociti e piastrine. Molti neonati con sindrome di Down acquisiscono una mutazione in GATA1 che produce una versione accorciata della proteina. Questo cambiamento porta a una condizione chiamata miolopoiesi anomala transitoria (TAM), una temporanea proliferazione di cellule ematiche immature. Utilizzando il sequenziamento dell'RNA a singola cellula, il team ha mostrato che la mutazione in GATA1 riscrive l'attività di centinaia di geni contemporaneamente, allontanando le cellule dalla via degli eritrociti e spingendole verso uno stato simile a megacariociti e mioide. Notevolmente, più di quattro cambiamenti su cinque osservati nella ML-DS conclamata sono già presenti in questa fase precoce di TAM, indicando che GATA1 è il principale motore del programma simile alla leucemia.
Dalla crescita temporanea alla vera leucemia
Non tutti i bambini con TAM sviluppano la leucemia e molti episodi si risolvono senza trattamento. Per capire cosa completa la transizione, i ricercatori hanno confrontato le cellule tumorali di bambini con ML-DS con quelle di bambini con TAM non progressivo. Hanno scoperto un set finale di cambiamenti genici condiviso tra i pazienti con ML-DS che si sovrappone al programma indotto da GATA1. Molti di questi geni sono noti per il loro ruolo nella crescita e nella sopravvivenza tumorale. Interessante, questo “modulo ML-DS” era attivo anche in altri tumori del sangue pediatrici, inclusi quelli non legati alla sindrome di Down, suggerendo che rappresenta una firma oncogenica generale piuttosto che qualcosa di esclusivo per la ML-DS. I bambini la cui malattia apparentemente transitoria è poi ricomparsa o è peggiorata mostravano già una maggiore attivazione di questo modulo, suggerendo che potrebbe aiutare a segnalare i casi ad alto rischio in fase precoce.
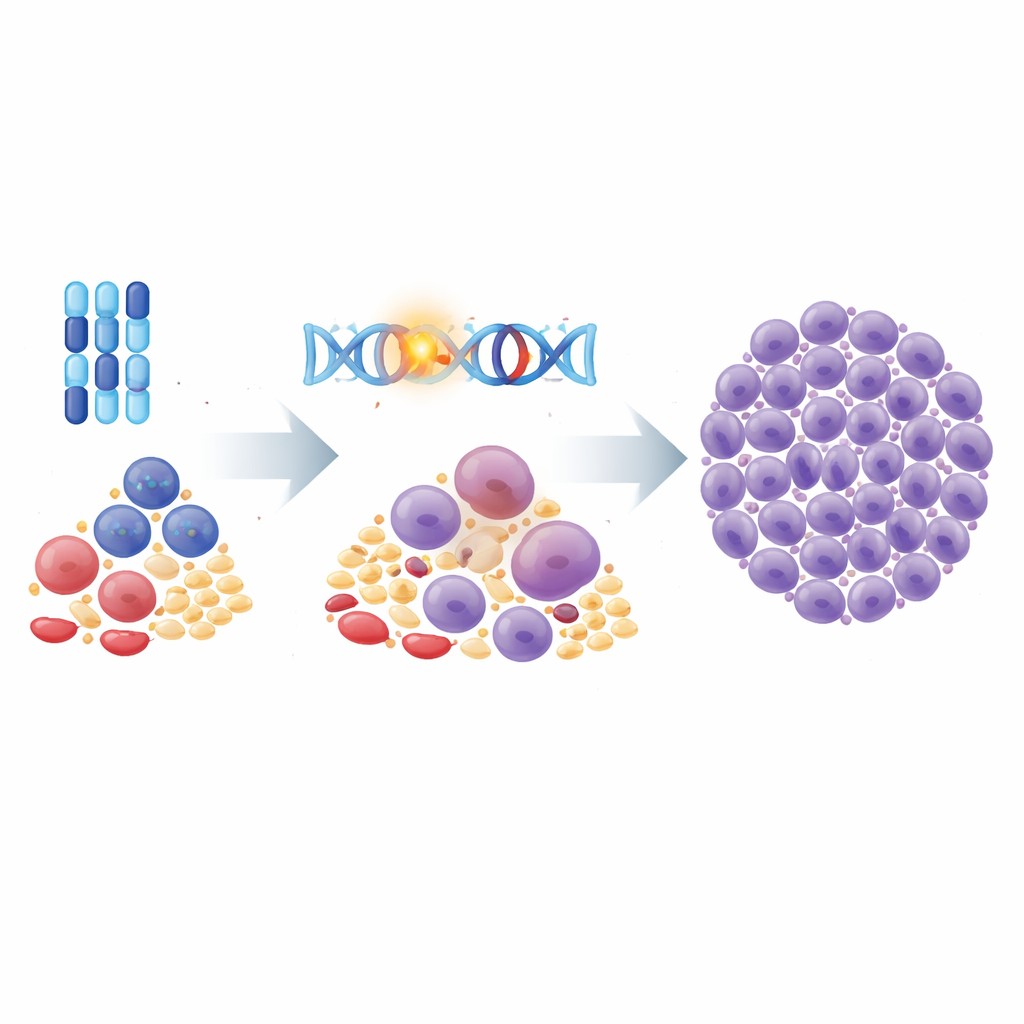
Tracciare i cloni pericolosi nel tempo
Il team ha avuto l'accesso raro a campioni di due bambini con ML-DS particolarmente aggressiva: uno che ha avuto due recidive e uno la cui leucemia è stata resistente al trattamento fin dall'inizio. Combinando il sequenziamento dell'intero genoma con i dati di RNA a singola cellula, hanno ricostruito gli alberi genealogici delle cellule tumorali nel tempo. In un bambino, le cellule di recidiva hanno formato rami separati che si sono evoluti in parallelo da un antenato comune, ma tutte hanno mantenuto lo stesso programma genico guidato da GATA1 e condividevano ulteriori variazioni che probabilmente le hanno aiutate a sopravvivere alla chemioterapia. Nell'altro bambino, un subclone nascosto con una perdita di parte del cromosoma 17, che interessa il noto gene “guardiano” TP53, era presente alla diagnosi e ha poi dominato dopo il trattamento. Anche in questi stadi avanzati, l'impronta della mutazione GATA1 rimaneva forte in ogni cellula leucemica.
Cosa significa per le cure future
Nel complesso, lo studio mostra che sebbene la copia extra del cromosoma 21 prepari il terreno, la mutazione di GATA1 scrive la maggior parte del copione per questa leucemia legata alla sindrome di Down, e quel copione resta stabile anche mentre la malattia evolve e diventa resistente ai trattamenti. Il salto finale dalla crescita transitoria al cancro vero e proprio coinvolge un ulteriore programma oncogenico più generale che ricorre in molti tipi di leucemia. In termini pratici, questo lavoro suggerisce due direzioni promettenti: primo, concentrare le terapie future sulla rete genica guidata da GATA1, che sembra essere una vulnerabilità costante del tumore; secondo, usare la più ampia firma genica ML-DS per identificare quali neonati con malattia transitoria sono a maggior rischio di progredire verso la leucemia, in modo da personalizzare con maggiore precisione l'assistenza.
Citazione: Trinh, M.K., Schuschel, K., Issa, H. et al. Single cell transcriptional evolution of myeloid leukemia of Down syndrome. Nat Commun 17, 3474 (2026). https://doi.org/10.1038/s41467-026-71707-2
Parole chiave: Leucemia nella sindrome di Down, Mutazione GATA1, Sequenziamento dell'RNA a singola cellula, Miolopoiesi anomala transitoria, Cancro del sangue pediatrico