Clear Sky Science · zh
生物工程化耐活性氧益生菌重塑肠道微生物—宿主轴以改善雄性小鼠2型糖尿病
为血糖健康重新想象益生菌
2型糖尿病通常被归咎于糖分、脂肪和缺乏运动,但在肠道深处还有另一个同样重要的参与者:数万亿的微生物,它们帮助消化食物并与我们的代谢对话。本研究探讨是否可以有意重构一种常见益生菌株,使其不仅能在糖尿病时炎症严重、环境恶劣的肠道中存活,而且能积极帮助恢复健康的微生物群并改善血糖控制——至少在小鼠中如此。
为敌对环境打造更强大的肠道盟友
研究人员以备受研究的益生菌株埃希氏菌(Escherichia coli)Nissle 1917为起点,该菌株能缓解肠道炎症,但在肥胖与2型糖尿病所致的高氧化性、化学应激强烈的肠道中表现不佳。为增强其耐受性,研究者反复用逐步增加剂量的过氧化氢——一种模拟糖尿病肠道慢性氧化应激的活性氧分子——处理细菌。经过十轮选择,他们获得了一株新菌株,称为REcN,能耐受显著更高水平的氧化应激。遗传与生化检测显示,REcN启动了整套抗氧化防御网络,包括能解毒活性分子的酶以及增强的细胞能量与氧化还原平衡处理系统。
工程化微生物如何处理应激与营养
深入研究表明,REcN重构了其代谢途径。它更有效地通过核心能量通路燃烧脂肪和碳水化合物,并表现出关键管理电子流动的酶更强的活性,从而减少有害副产物的形成。该菌株还以受控方式产生更多硫化氢,在此情境下充当额外的化学屏障以抵御氧化损伤。在细胞培养实验中,REcN培养上清能减少脂肪细胞内的脂滴并抑制迅速分解淀粉和糖的消化酶活性,这暗示该微生物可能减缓餐后血糖激增并促使机体燃烧脂肪而非储存。
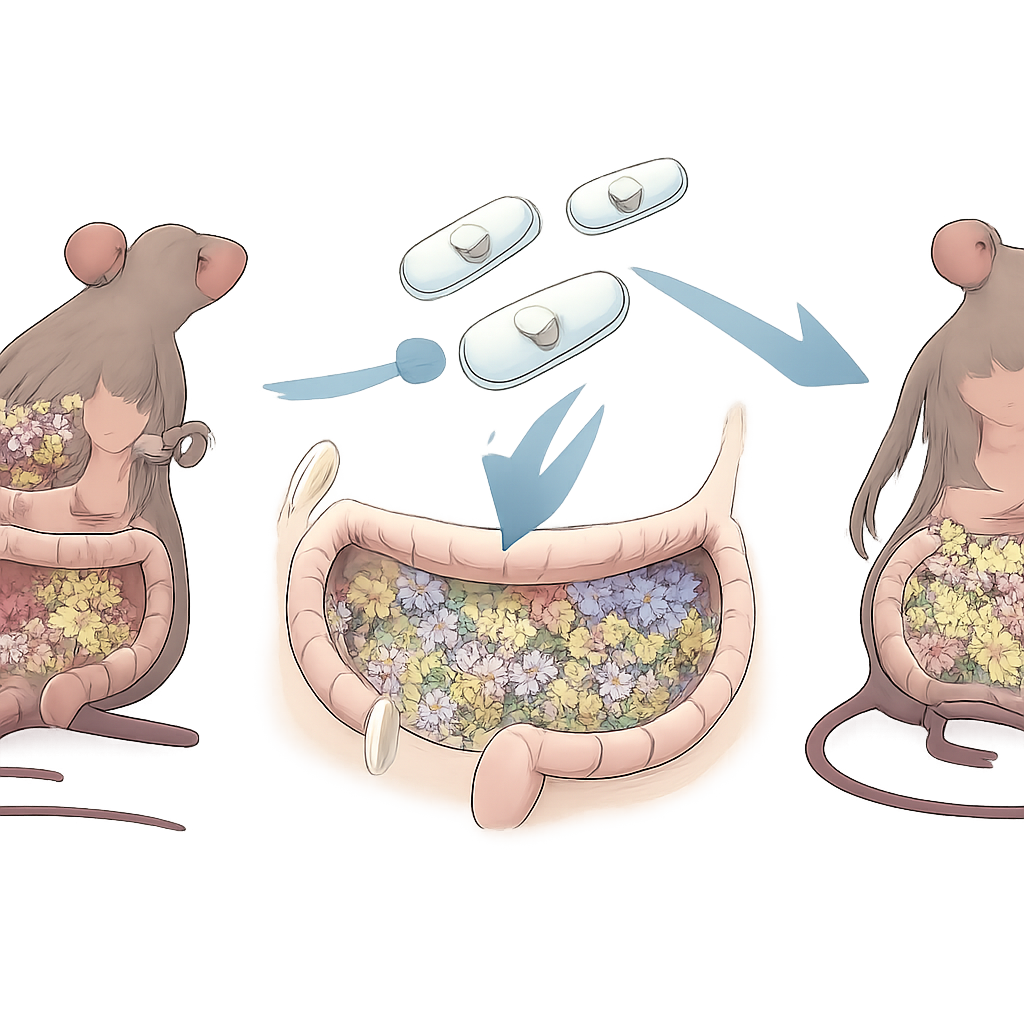
为旅程装甲并供能益生菌
为了确保这株升级后的细菌能通过胃和小肠,科学家用一种植物来源的糖链——果聚糖寡糖(fructooligosaccharides)为REcN包覆一层,然后用一层碳酸钙薄壳使其矿化,生成REcN‑F/Ca。电子显微镜显示每个细胞周围都有平滑的保护壳。在模拟消化液中,这种包被帮助更多细菌存活并保持中和高反应性自由基的能力。矿化外壳在酸性胃类液体中迅速溶解,但在模拟小肠和发炎的结肠条件下溶解较慢,从而在细菌最需要的部位释放它们。给予小鼠后,包被菌株比未改造对照更好地定植肠道并将免疫细胞引导向较少炎症的状态。
扭转小鼠的肥胖、血糖和肠道生态
关键测试在饲以高脂饮食导致肥胖和类2型糖尿病症状的雄性小鼠中进行。与未处理动物相比,接受REcN‑F/Ca的小鼠体重增长明显更少,腹部脂肪减少,空腹血糖和胰岛素敏感性改善。它们对突发葡萄糖负荷的反应更接近正常,相比之下,高脂喂养小鼠的胰岛素分泌受损。在显微镜下,它们的脂肪组织中炎性免疫细胞和脂滴更少,结肠显示出更少的氧化损伤。在基因层面,处理组上调了由一个称为PPARα的主调控因子控制的通路活性,该因子促进脂肪燃烧并抑制炎症。当该通路被化学抑制时,工程化益生菌的大部分益处消失,表明PPARα是微生物与宿主代谢之间的关键联结点。
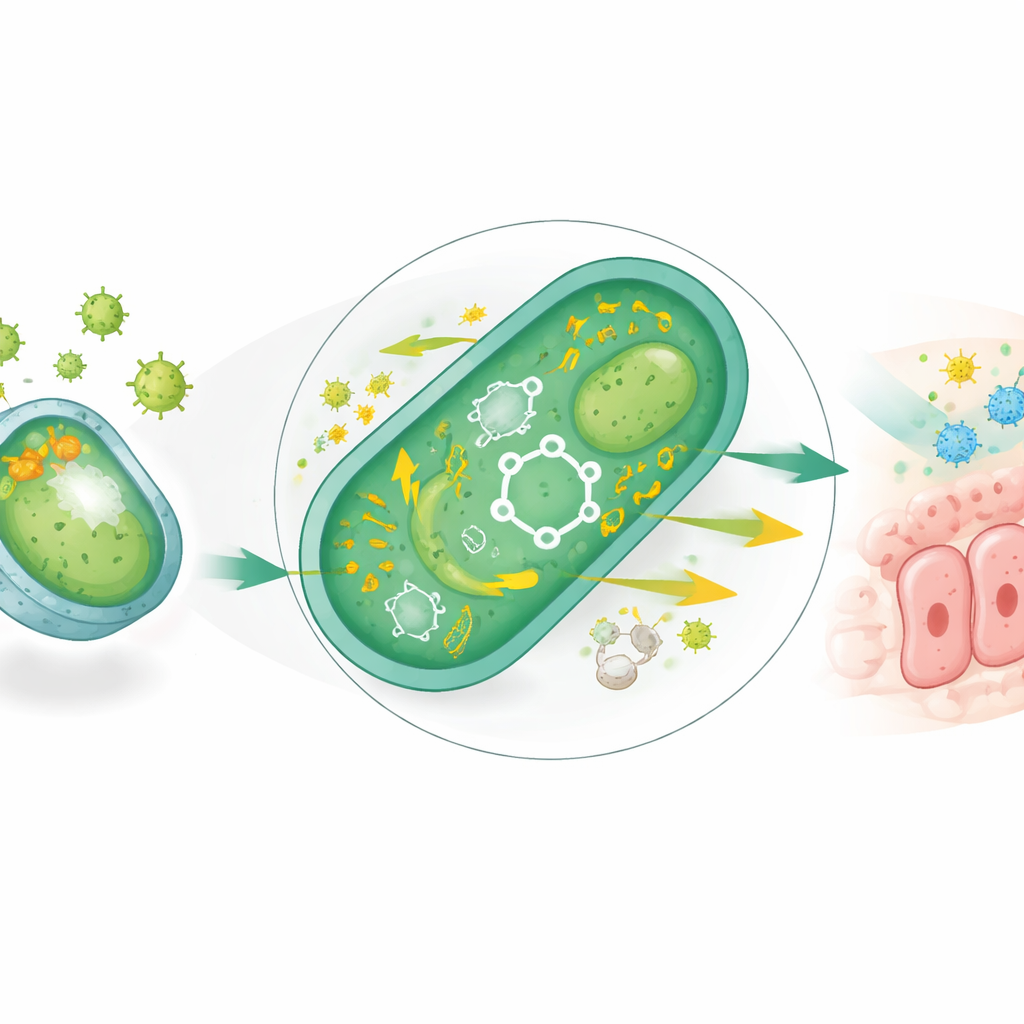
重建更健康的微生物邻里
该工程化益生菌还重塑了更广泛的肠道群落。高脂喂养剥夺了小鼠肠道的微生物多样性,并耗竭了产生短链脂肪酸的细菌——这些小分子滋养肠道上皮并有助于调节免疫与血糖控制。REcN‑F/Ca部分恢复了多样性,并显著富集了如Lachnospiraceae科和属Blautia等家族,这些群体以产生有益的丁酸而闻名,并在人类研究中与更佳的代谢健康相关。粪便化学物质测定证实,关键短链脂肪酸在高脂饮食下下降后,在处理组中回升至接近正常水平。
这对未来糖尿病护理意味着什么
综合来看,这项工作表明可以“训练”益生菌在肥胖与糖尿病的应激性肠道环境中存活,并设计一种简便的包被将其以活菌形式递送到结肠。在小鼠中,这种生物工程化微生物同时纠正了代谢疾病的多个标志:它中和过量的活性分子、将肠道生态向有益物种转变、激活宿主有利于脂肪燃烧的通路,并缓解炎症与胰岛素抵抗。尽管在将此类方法用于人类之前仍需许多步骤——包括长期安全性、用量以及在两性中的研究——但本研究为下一代益生菌指出了一条路径:它们不只是求生,而是积极与我们的身体合作,从内部重新平衡代谢。
引用: Mao, C., Jin, W., Dou, L. et al. Bioengineered ROS-tolerant probiotic reshapes gut microbiota-host axis to ameliorate type 2 diabetes in male mice. Nat Commun 17, 3339 (2026). https://doi.org/10.1038/s41467-026-70138-3
关键词: 工程化益生菌, 肠道微生物组, 2型糖尿病, 氧化应激, 短链脂肪酸