Clear Sky Science · ru
Биоинженерный пробиотик, устойчивый к ROS, перестраивает ось микробиота–хозяин, улучшая состояние при сахарном диабете 2 типа у самцов мышей
Переосмысление «дружелюбных» бактерий для контроля уровня сахара
Сахарный диабет 2 типа обычно связывают с избыточным потреблением сахара, жиров и недостатком физической активности, но глубоко в кишечнике важную роль играет еще один фактор: триллионы микробов, которые помогают переваривать пищу и взаимодействуют с нашим метаболизмом. В этом исследовании изучали, можно ли целенаправленно перепрограммировать одну известную пробиотическую штамм, чтобы он не только выживал в суровой, воспаленной среде кишечника при диабете, но и активно способствовал восстановлению здоровой микробиоты и улучшению контроля гликемии — по крайней мере у мышей.
Укрепленный союзник для враждебной среды
Исследователи начали с Escherichia coli Nissle 1917, хорошо изученного пробиотика, который может успокаивать кишечное воспаление, но с трудом переносит сильно окислительную, химически напряженную среду при ожирении и сахарном диабете 2 типа. Чтобы сделать штамм более устойчивым, его многократно подвергали повышающимся дозам перекиси водорода — реактивного кислородного соединения, имитирующего хронический окислительный стресс в диабетическом кишечнике. После десяти раундов отбора они получили новый штамм, названный REcN, который мог переносить значительно более высокие уровни окислительного стресса. Генетические и биохимические тесты показали, что у REcN активировались целые сети антиоксидантной защиты, включая ферменты, детоксифицирующие реактивные молекулы, и усиленную систему управления энергетическим и редокс-гомеостазом клетки.
Как инженерный микроб справляется со стрессом и питанием
Глубже анализ показал, что у REcN перестроен метаболизм. Он эффективнее окислял жиры и углеводы по основным энергетическим путям и демонстрировал повышенную активность ключевых ферментов, управляющих переносом электронов и уменьшающих образование вредных побочных продуктов. Штамм также вырабатывал больше сероводорода в контролируемой форме, что в данном контексте выступало дополнительным химическим щитом против окислительного повреждения. В экспериментах с клеточными культурами фильтрат из культур REcN снижал количество жировых капель в адипоцитах и подавлял активность пищеварительных ферментов, которые быстро расщепляют крахмал и сахара, что наводит на мысль, что микроб может замедлять послеаппетитные всплески глюкозы и стимулировать сжигание жира вместо его отложения.
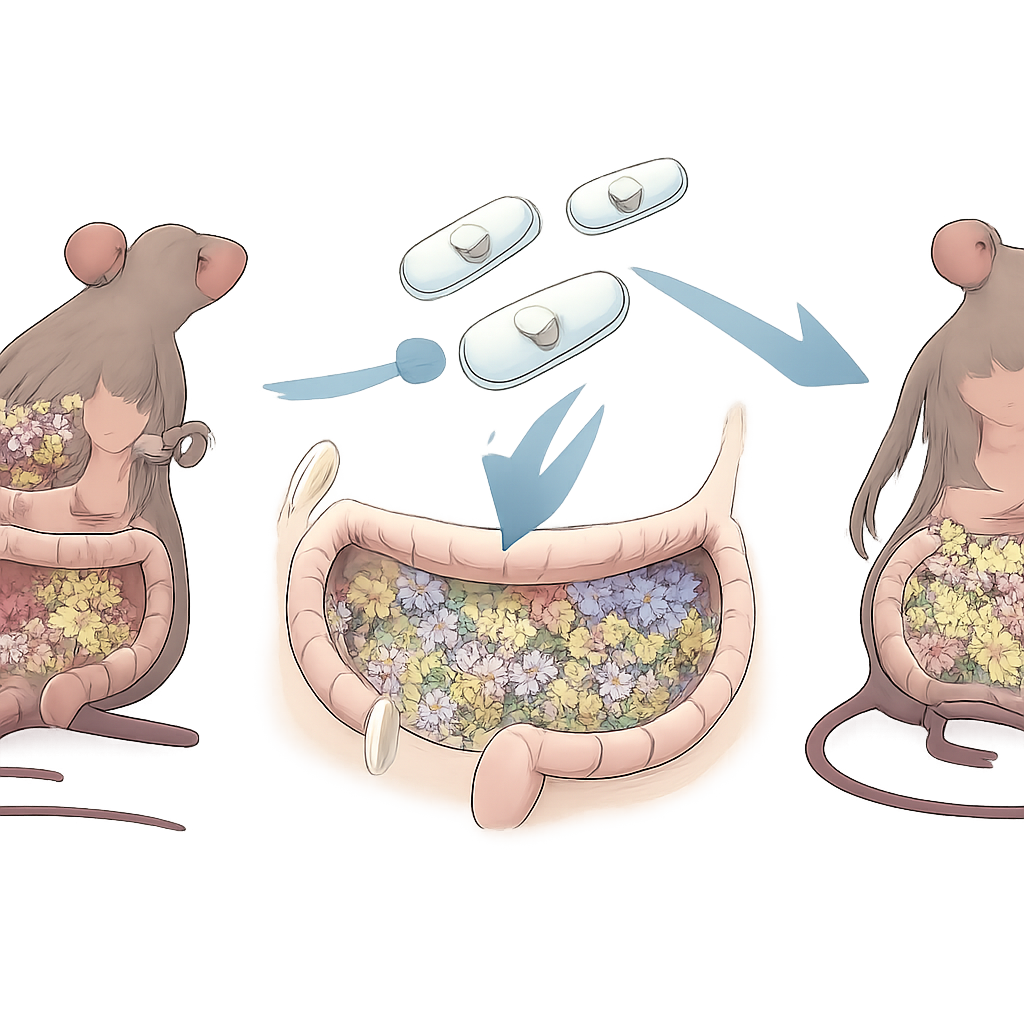
Бронирование и питание пробиотика для пути
Чтобы гарантировать выживание улучшенного штамма в пути через желудок и тонкую кишку, ученые покрыли REcN слоем растительных сахарных цепочек — фруктолигосахаридов — а затем минерализовали тонкой оболочкой из карбоната кальция, получив REcN‑F/Ca. Электронная микроскопия показала гладкую защитную оболочку вокруг каждой клетки. В моделируемых пищеварительных средах такое покрытие помогало значительно большему числу бактерий выживать и сохранять способность нейтрализовать высокореактивные радикалы. Минеральная оболочка быстро растворялась в кислой среде, имитирующей желудок, но медленнее — в условиях, соответствующих кишечнику и воспаленному отделу толстой кишки, высвобождая бактерии там, где они наиболее нужны. При введении мышам покрытый штамм лучше колонизировал кишечник, чем немодифицированный, и склонял иммунные клетки к менее воспалительному состоянию.
Изменение ожирения, уровня сахара и экологии кишечника у мышей
Ключевое испытание проводили на самцах мышей, получавших высокожировую диету, вызывающую ожирение и симптомы, похожие на сахарный диабет 2 типа. По сравнению с нелечеными животными мыши, получавшие REcN‑F/Ca, прибавляли в весе значительно меньше, имели меньше абдоминального жира и демонстрировали улучшенные показатели натощак глюкозы и чувствительности к инсулину. Их реакция на внезапный глюкозный шок была более нормальной, в отличие от мышей на ВЖД, у которых секреция инсулина была нарушена. В жировых тканях у них наблюдалось меньше воспалительных иммунных клеток и меньше жировых капель, а в толстой кишке — меньше окислительных повреждений. На уровне экспрессии генов у обработанных мышей усилилась активность путей, контролируемых главным регулятором PPARα, который способствует сжиганию жира и подавляет воспаление. Когда этот путь химически блокировали, преимущества инженерного пробиотика в значительной мере исчезали, что указывает на PPARα как на ключевую связь между микробом и метаболизмом хозяина.
Восстановление более здорового микробного окружения
Инженерный пробиотик также перестроил более широкое сообщество кишечника. Высокожировая диета лишила кишечник мышей микробного разнообразия и истощила бактерии, продуцирующие короткоцепочечные жирные кислоты — небольшие молекулы, питающие эпителий кишечника и участвующие в регуляции иммунитета и контроля глюкозы. REcN‑F/Ca частично восстановил разнообразие и существенно обогатил семейства, такие как Lachnospiraceae, и род Blautia, известные производством полезной масляной кислоты (бутирата) и связью в исследованиях человека с лучшим метаболическим здоровьем. Измерения фекальных метаболитов подтвердили, что уровни ключевых короткоцепочечных жирных кислот, которые падали на ВЖД, у обработанных мышей восстановились почти до нормальных значений.
Что это может значить для будущего лечения диабета
В целом работа показывает, что возможно «обучить» пробиотик выживанию в стрессовой среде кишечника при ожирении и диабете и разработать простое покрытие, доставляющее его живым до толстой кишки. У мышей этот биоинженерный микроб одновременно устранил избыток реактивных молекул, сместил экосистему кишечника в сторону полезных видов, активировал пути хозяина, способствующие сжиганию жира, и снизил воспаление и инсулинорезистентность. Хотя до испытаний на людях еще далеко — требуются исследования долгосрочной безопасности, дозирования и исследования на самцах и самках — это исследование очерчивает путь к пробиотикам следующего поколения, которые не просто выживают: они активно сотрудничают с нашим организмом, восстанавливая метаболический баланс изнутри.
Цитирование: Mao, C., Jin, W., Dou, L. et al. Bioengineered ROS-tolerant probiotic reshapes gut microbiota-host axis to ameliorate type 2 diabetes in male mice. Nat Commun 17, 3339 (2026). https://doi.org/10.1038/s41467-026-70138-3
Ключевые слова: инженерные пробиотики, кишечный микробиом, сахарный диабет 2 типа, окислительный стресс, короткоцепочечные жирные кислоты