Clear Sky Science · nl
Bio-gemanipuleerde ROS-tolerante probiotic herstructureert de darmmicrobiota-gastheeras om type 2-diabetes bij mannelijke muizen te verbeteren
Het opnieuw bedenken van vriendelijke bacteriën voor bloedsuikergezondheid
Type 2 diabetes wordt doorgaans toegeschreven aan suiker, vet en gebrek aan beweging, maar diep in de darm speelt een andere factor even belangrijk: biljoenen microben die helpen bij de spijsvertering en communiceren met onze stofwisseling. Deze studie onderzoekt of we een bekende probiotische stam gericht kunnen herontwerpen zodat deze niet alleen overleeft in de zware, ontstoken darmen bij diabetes, maar ook actief bijdraagt aan het herstel van een gezond microbioom en verbetering van de bloedsuikercontrole — althans bij muizen.
Een steviger darmbondgenoot voor een vijandige omgeving
De onderzoekers begonnen met Escherichia coli Nissle 1917, een goed bestudeerde probiotica die darmontsteking kan kalmeren maar moeite heeft in de sterk oxiderende, chemisch stressvolle darmen van obesitas en type 2 diabetes. Om de stam te versterken, werden de bacteriën herhaaldelijk blootgesteld aan toenemende doses waterstofperoxide, een reactieve zuurstofverbinding die de chronische oxidatieve stress in een diabetesdarm nabootst. Na tien selectieronden verkregen ze een nieuwe stam, genaamd REcN, die veel hogere niveaus van oxidatieve stress kon verdragen. Genetische en biochemische tests toonden aan dat REcN volledige netwerken van antioxidantverdedigingen had geactiveerd, waaronder enzymen die reactieve moleculen ontgiften en een verbeterd systeem voor het omgaan met cellulaire energie en redoxbalans.
Hoe de gemodificeerde microbe met stress en voeding omgaat
Dieper gravend ontdekte het team dat REcN zijn metabolisme had herbedraad. Het verbrandde vetten en koolhydraten efficiënter via kernenergiepaden en vertoonde sterkere activiteit van sleutelenzymen die elektronen beheren en de vorming van schadelijke bijproducten verminderen. De stam produceerde ook meer waterstofsulfide op een gecontroleerde manier, wat in deze context fungeerde als een extra chemisch schild tegen oxidatieve schade. In celkweekexperimenten verminderde het vloeistofmedium van REcN-kweken vetdruppels in vetcellen en dempte het de activiteit van verteringsenzymen die zetmeel en suikers snel afbreken, wat suggereert dat de microbe pieken in de bloedglucose na maaltijden zou kunnen vertragen en het lichaam eerder zou aansporen vet te verbranden dan op te slaan.
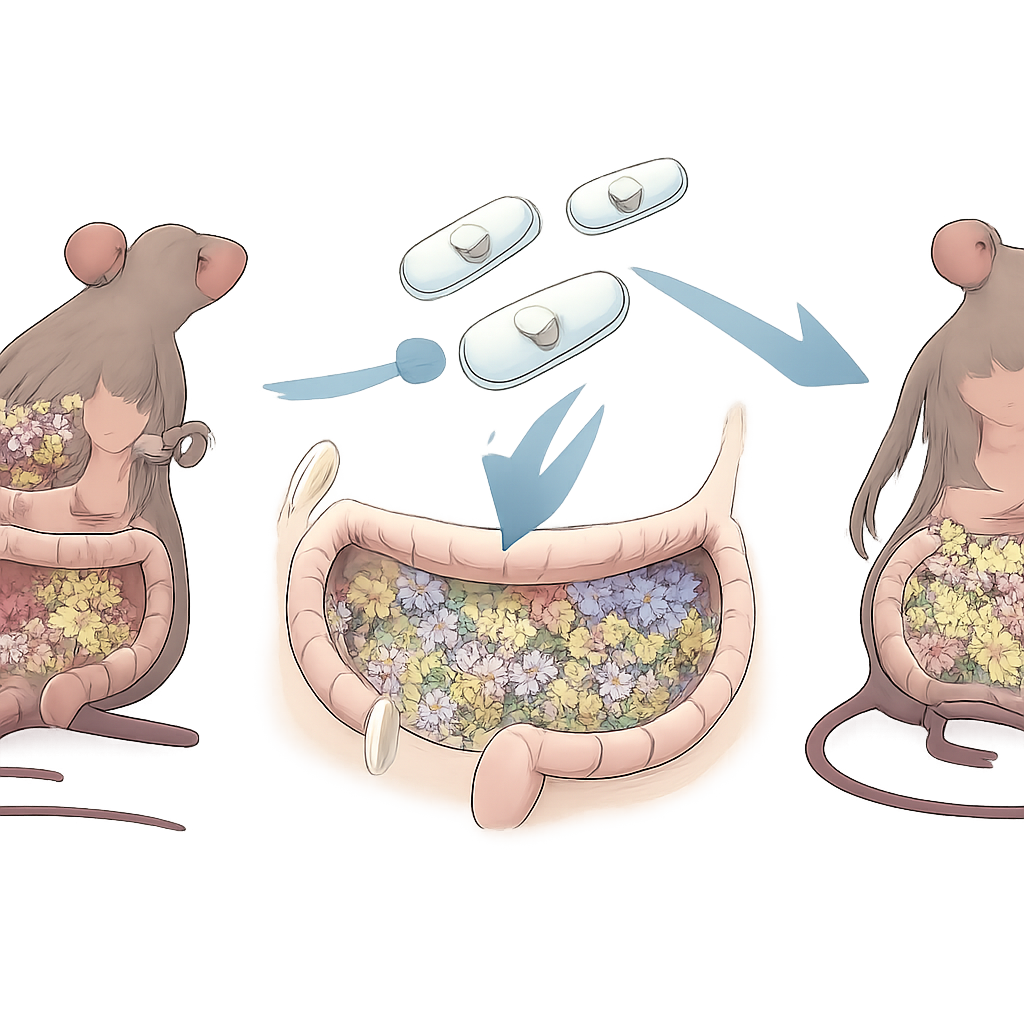
De probiotic beschermen en voeden voor de reis
Om te verzekeren dat deze verbeterde bacterie de reis door de maag en dunne darm overleefde, coatten de wetenschappers REcN met een laag plantaardige suikerketens genaamd fructo-oligosacchariden en mineraliseerden die vervolgens met een dunne schaal van calciumcarbonaat, waarmee REcN‑F/Ca ontstond. Elektronenmicroscopie toonde een gladde, beschermende schaal rond elke cel. In gesimuleerde spijsverteringsvloeistoffen hielp deze coating veel meer bacteriën te overleven en hun vermogen te behouden om zeer reactieve radicalen te neutraliseren. De mineralschil loste snel op in zuurgevoelige maagachtige vloeistof maar langzamer in omstandigheden die de darm en ontstoken colon nabootsen, waardoor de bacteriën vrijkwamen waar ze het meest nodig zijn. Bij toediening aan muizen koloniseerde de gecoate stam de darm beter dan de ongemodificeerde variant en stuwde immuuncellen in een minder inflammatoire richting.
Het keren van obesitas, bloedsuiker en darmiologie bij muizen
De cruciale test vond plaats bij mannelijke muizen die een vetrijke voeding kregen die obesitas en diabetes-achtige symptomen veroorzaakte. Vergeleken met onbehandelde dieren kregen muizen die REcN‑F/Ca ontvingen veel minder gewichtstoename, hadden ze minder buikvet en toonden ze verbeterde nuchtere bloedsuiker en insulinegevoeligheid. Hun lichamen reageerden normaler op een plotselinge glucosetolerantietest, in tegenstelling tot de vetrijke-gevoede muizen wiens insulinesecretie tekortschoot. Onder de microscoop bevatten hun vetweefsels minder inflammatoire immuuncellen en minder vetdruppels, en hun colonen vertoonden minder oxidatieve schade. Op geniveau verhoogden de behandelde muizen de activiteit van paden die worden gereguleerd door een hoofdregelaar genaamd PPARα, die vetverbranding bevordert en ontsteking dempt. Toen dit pad chemisch werd geblokkeerd, verdwenen de voordelen van de gemodificeerde probiotica grotendeels, wat suggereert dat PPARα een belangrijke schakel is tussen microbe en gastheerstofwisseling.
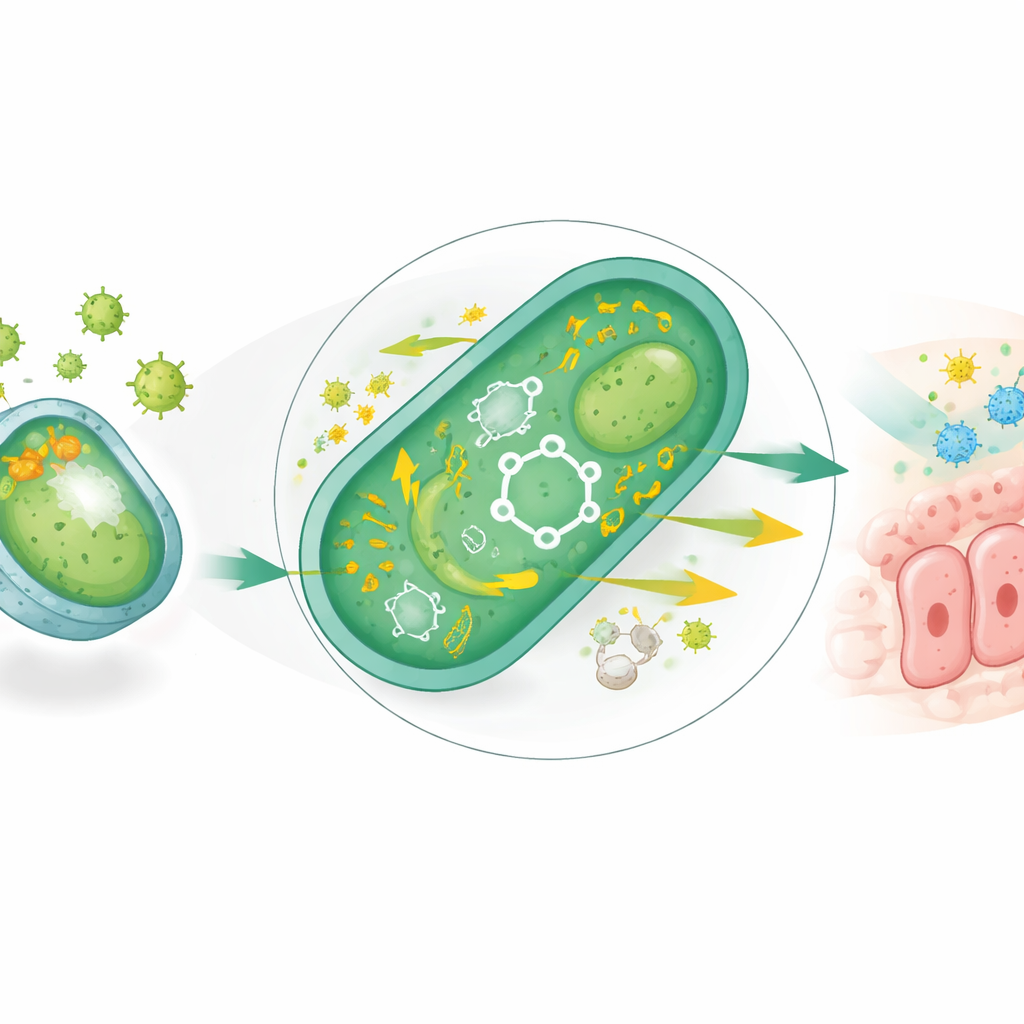
Het herbouwen van een gezondere microbiele omgeving
De gemodificeerde probiotica hervormde ook de bredere darmgemeenschap. Vetrijke voeding had de darm van de muizen ontdaan van microbiële diversiteit en bacteriën uitgeput die korteketenvetzuren produceren — kleine moleculen die de darmslijmvlies voeden en helpen bij de regulatie van immuniteit en glucosecontrole. REcN‑F/Ca herstelde gedeeltelijk de diversiteit en verrijkte sterk families zoals Lachnospiraceae en het geslacht Blautia, beide bekend om het genereren van het gunstige vetzuur boterzuur en verbonden in humane studies met betere metabole gezondheid. Metingen van fecale chemicaliën bevestigden dat niveaus van belangrijke korteketenvetzuren, die onder het vetrijke dieet waren gedaald, in de behandelde muizen weer tot bijna normale waarden herstelden.
Wat dit zou kunnen betekenen voor toekomstige diabeteszorg
Samengevat laat het werk zien dat het mogelijk is een probiotica te "trainen" om te gedijen in de stressvolle darmomgeving van obesitas en diabetes en een eenvoudige coating te ontwerpen die het levend naar de colon brengt. Bij muizen corrigeerde deze bio-gemanipuleerde microbe meerdere kenmerken van metabole ziekte tegelijk: het neutraliseerde overtollige reactieve moleculen, verschuifde het darmecosysteem naar gunstige soorten, activeerde gastheerwegen die vetverbranding bevorderen en verminderde ontsteking en insulineresistentie. Hoewel veel stappen nog nodig zijn voordat een dergelijke benadering bij mensen kan worden getest — inclusief langetermijnveiligheid, dosering en studies in beide geslachten — schetst deze studie een route naar next-generation probiotica die meer doen dan alleen overleven: ze werken actief samen met ons lichaam om de stofwisseling van binnenuit te herbouwen.
Bronvermelding: Mao, C., Jin, W., Dou, L. et al. Bioengineered ROS-tolerant probiotic reshapes gut microbiota-host axis to ameliorate type 2 diabetes in male mice. Nat Commun 17, 3339 (2026). https://doi.org/10.1038/s41467-026-70138-3
Trefwoorden: gemodificeerde probiotica, darmmicrobioom, type 2 diabetes, oxidatieve stress, korteketenvetzuren