Clear Sky Science · de
Bioengineering-RNS-tolerantes Probiotikum formt die Darmmikrobiota-Host-Achse neu, um Typ-2-Diabetes bei Männchen zu bessern
Freundliche Bakterien neu gedacht für Blutzuckergesundheit
Typ-2-Diabetes wird meist Zucker, Fett und Bewegungsmangel zugeschrieben, doch tief im Darm spielt ein anderer Akteur eine ebenso wichtige Rolle: Billionen von Mikroben, die bei der Verdauung helfen und mit unserem Stoffwechsel kommunizieren. Diese Studie untersucht, ob sich ein bekanntes Probiotikum absichtlich so umgestalten lässt, dass es nicht nur in den harschen, entzündeten Därmen von Diabetes überlebt, sondern aktiv dazu beiträgt, ein gesundes Mikrobiom wiederherzustellen und die Blutzuckerregulation zu verbessern – zumindest bei Mäusen.
Ein robusterer Darmhelfer für eine feindliche Umgebung
Die Forschenden begannen mit Escherichia coli Nissle 1917, einem gut untersuchten Probiotikum, das Darmentzündungen dämpfen kann, aber in den stark oxidativen, chemisch belasteten Därmen von Adipositas und Typ-2-Diabetes Schwierigkeiten hat. Um es widerstandsfähiger zu machen, setzten sie die Bakterien wiederholt steigenden Dosen von Wasserstoffperoxid aus, einem reaktiven Sauerstoffmolekül, das den chronischen oxidativen Stress eines diabetischen Darms nachahmt. Nach zehn Selektionsrunden gewannen sie einen neuen Stamm, genannt REcN, der deutlich höhere Oxidationsbelastungen tolerierte. Genetische und biochemische Tests zeigten, dass REcN ganze Netzwerke antioxidativer Abwehrmechanismen hochgefahren hatte, einschließlich Enzymen, die reaktive Moleküle entgiften, und einem verstärkten System zur Handhabung von zellulärer Energie und Redox-Balance.
Wie das entwickelte Mikroben-Stamm Stress und Nährstoffe bewältigt
Bei tieferer Untersuchung zeigte sich, dass REcN seinen Stoffwechsel umverdrahtet hatte. Er verbrennt Fette und Kohlenhydrate effizienter über zentrale Energiewege und zeigte eine stärkere Aktivität wichtiger Enzyme, die Elektronen verwalten und die Bildung schädlicher Nebenprodukte reduzieren. Der Stamm produzierte außerdem gesteuert mehr Schwefelwasserstoff, der hier als zusätzlicher chemischer Schutz gegen oxidativen Schaden wirkte. In Zellkulturen reduzierte das Kulturmedium von REcN Fetttropfen in Fettzellen und dämpfte die Aktivität von Verdauungsenzymen, die Stärke und Zucker rasch abbauen, was darauf hindeutet, dass das Mikrobenprodukt Blutzuckerspitzen nach Mahlzeiten verlangsamen und den Körper dazu anregen könnte, eher Fett zu verbrennen als zu speichern.
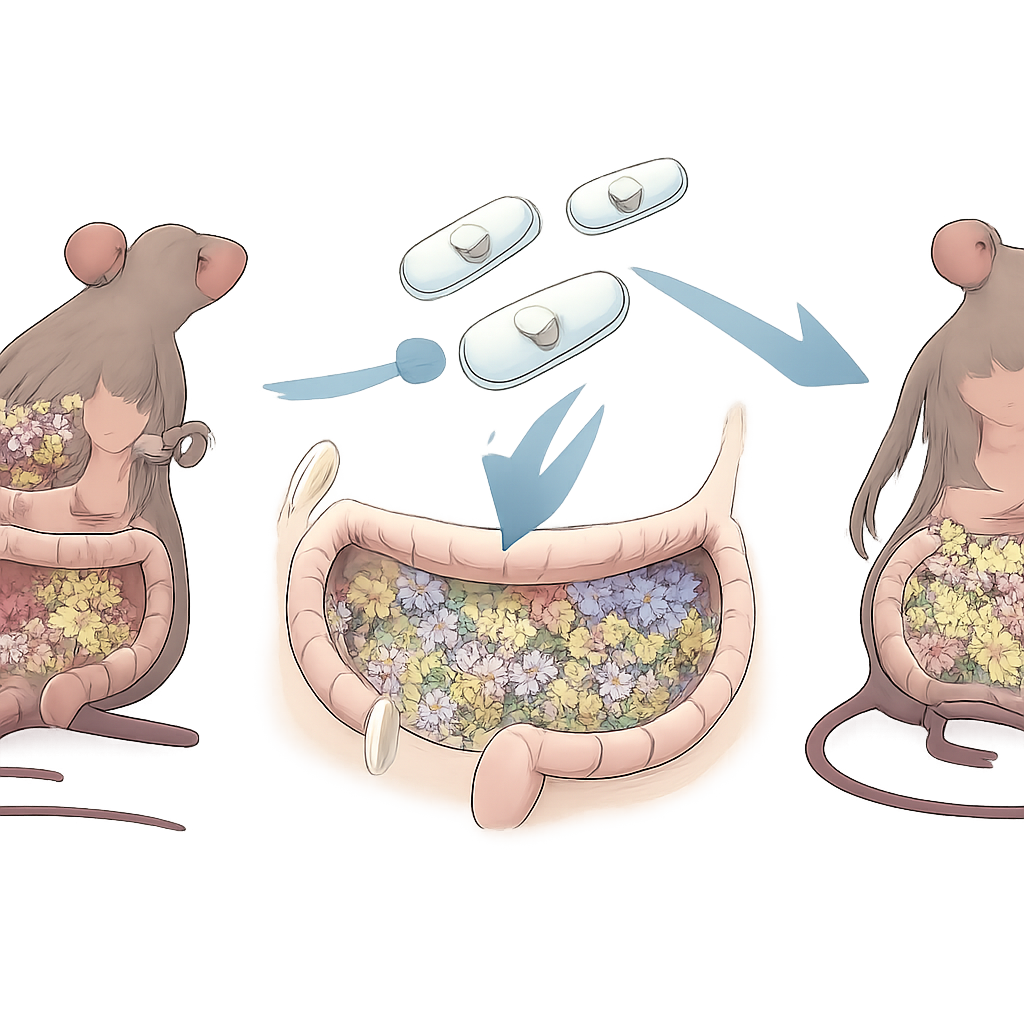
Das Probiotikum schützen und ernähren für die Reise
Um sicherzustellen, dass dieses verbesserte Bakterium die Passage durch Magen und Dünndarm überlebt, beschichteten die Wissenschaftler REcN mit einer Schicht pflanzlicher Zuckerketten, sogenannter Fructooligosaccharide, und mineralisierten es anschließend mit einer dünnen Schale aus Calciumcarbonat, wodurch REcN‑F/Ca entstand. Elektronenmikroskopie zeigte eine glatte, schützende Hülle um jede Zelle. In simulierten Verdauungsflüssigkeiten half diese Beschichtung deutlich mehr Bakterien, lebensfähig zu bleiben und ihre Fähigkeit zur Neutralisierung hochreaktiver Radikale zu bewahren. Die Mineralschale löste sich schnell in magensaftähnlicher Säure, aber langsamer in Bedingungen, die den Darm und den entzündeten Dickdarm nachahmen, und setzte die Bakterien dort frei, wo sie am meisten gebraucht werden. Bei Verabreichung an Mäuse kolonisierte der beschichtete Stamm den Darm besser als sein unveränderter Gegenpart und lenkte Immunzellen in einen weniger entzündlichen Zustand.
Wende bei Adipositas, Blutzucker und Darmökologie in Mäusen
Der entscheidende Test erfolgte an männlichen Mäusen, die mit einer fettreichen Ernährung gefüttert wurden, die Adipositas und typ-2-diabetesähnliche Symptome hervorrief. Im Vergleich zu unbehandelten Tieren nahmen Mäuse, die REcN‑F/Ca erhielten, deutlich weniger zu, hatten weniger Bauchfett und zeigten verbesserte Nüchternblutzuckerwerte sowie Insulinsensitivität. Ihr Körper reagierte normaler auf eine plötzliche Glukosebelastung, im Gegensatz zu den fettreich gefütterten Mäusen, bei denen die Insulinsekretion schwächelte. Unter dem Mikroskop fanden sich in ihrem Fettgewebe weniger entzündliche Immunzellen und weniger Fetttropfen, und ihre Kolons wiesen weniger oxidative Schäden auf. Auf Genebene erhöhten die behandelten Mäuse die Aktivität von Wegen, die von einem Masterregulator namens PPARα gesteuert werden, der Fettverbrennung fördert und Entzündungen dämpft. Wurde dieser Weg chemisch blockiert, verschwanden die Vorteile des gentechnisch veränderten Probiotikums größtenteils, was darauf hindeutet, dass PPARα eine Schlüsselrolle zwischen Mikrobe und Wirtsstoffwechsel spielt.
Wiederaufbau einer gesünderen mikrobiellen Nachbarschaft
Das entwickelte Probiotikum veränderte auch die breitere Darmgemeinschaft. Die fettreiche Ernährung hatte die mikrobiellen Vielfalt der Mäusedärme reduziert und Bakterien dezimiert, die kurzkettige Fettsäuren produzieren – kleine Moleküle, die die Darmschleimhaut nähren und zur Regulation von Immunität und Glukose beitragen. REcN‑F/Ca stellte teilweise die Diversität wieder her und reicherte stark Familien wie Lachnospiraceae und die Gattung Blautia an, die beide für die Produktion der vorteilhaften Fettsäure Butyrat bekannt sind und in Humanstudien mit besserer metabolischer Gesundheit in Verbindung gebracht werden. Messungen von Stuhlmetaboliten bestätigten, dass die Konzentrationen wichtiger kurzkettiger Fettsäuren, die unter der fettreichen Diät eingebrochen waren, bei den behandelten Mäusen wieder nahezu normal waren.
Was dies für die zukünftige Diabetesbehandlung bedeuten könnte
Zusammengefasst zeigt die Arbeit, dass es möglich ist, ein Probiotikum so zu „trainieren“, dass es in der stressgeprägten Darmumgebung von Adipositas und Diabetes gedeiht, und eine einfache Beschichtung zu entwerfen, die es lebend in den Dickdarm bringt. Bei Mäusen korrigierte dieses bioengineerte Mikrobenprodukt gleichzeitig mehrere Kennzeichen metabolischer Erkrankungen: Es neutralisierte überschüssige reaktive Moleküle, verschob das Darmökosystem zugunsten nützlicher Arten, aktivierte Wirtswege, die Fettverbrennung fördern, und milderte Entzündungen sowie Insulinresistenz. Obwohl viele Schritte nötig sind, bevor ein solcher Ansatz am Menschen getestet werden kann – einschließlich Langzeitsicherheit, Dosierung und Studien in beiden Geschlechtern – skizziert diese Studie einen Weg zu neuartigen Probiotika, die mehr tun als überleben: Sie arbeiten aktiv mit unserem Körper zusammen, um den Stoffwechsel von innen heraus wieder ins Gleichgewicht zu bringen.
Zitation: Mao, C., Jin, W., Dou, L. et al. Bioengineered ROS-tolerant probiotic reshapes gut microbiota-host axis to ameliorate type 2 diabetes in male mice. Nat Commun 17, 3339 (2026). https://doi.org/10.1038/s41467-026-70138-3
Schlüsselwörter: künstlich veränderte Probiotika, Darmmikrobiom, Typ-2-Diabetes, oxidativer Stress, kurzkettige Fettsäuren