Clear Sky Science · zh
L-天冬酰胺酶诱导的肿瘤代谢适应揭示了B细胞淋巴瘤对PARP1/2抑制剂的脆弱性
将癌症的“燃料短缺”转化为新的薄弱点
肿瘤科医生长期以来使用一种名为L-天冬酰胺酶的酶药,通过掐断某些血液癌症所需的关键养分来迫使其死亡。然而,许多肿瘤最终学会适应这种“节食”并重新生长,导致患者可用的治疗选项减少。本研究提出了一个简单但重要的问题:癌细胞究竟做了什么来逃避这种饥饿状态,能否利用现有药物将这一逃生路径反过来作为致命弱点?
一种“饥饿药”如何对抗血液癌症
L-天冬酰胺酶通过清除血液中的氨基酸天冬酰胺来起作用。一些白血病和淋巴瘤细胞自身无法合成足够的天冬酰胺,因此当血液供应减少时,它们便衰弱并死亡。在B细胞淋巴瘤的小鼠模型中,研究人员证实该药物起初能强力延缓肿瘤生长。然而即便持续用药,肿瘤最终还是复发。重要的是,药物在血液中仍然有效,这意味着癌症并非简单地“熬过”了治疗——而是以更微妙的方式进行了适应。
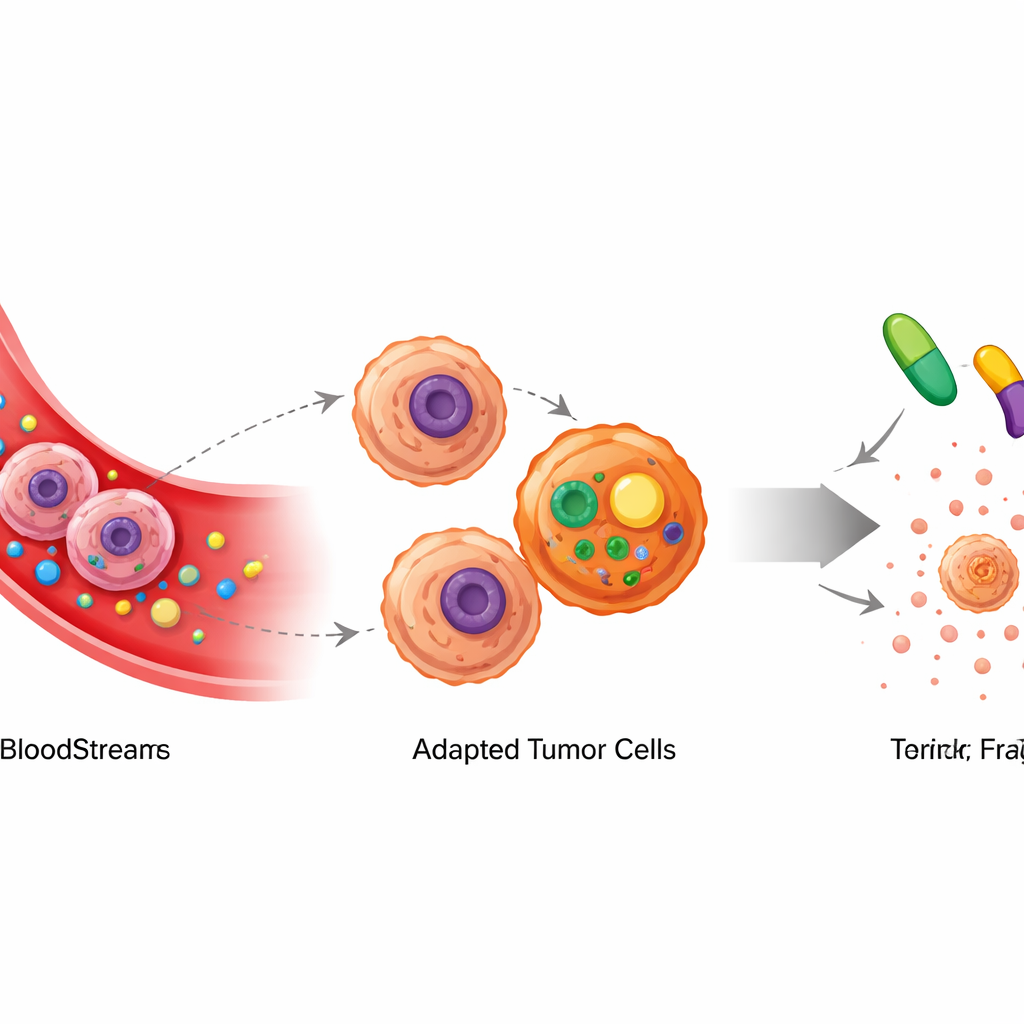
代谢绕道:合成新的构建模块
为揭示肿瘤如何适应,团队对来自受治与未受治小鼠的癌细胞内数百种小分子进行了精确测量。他们观察到在接受L-天冬酰胺酶处理的肿瘤中,两种相关氨基酸——丝氨酸和甘氨酸——显著升高。借助标记营养物作为示踪剂,研究显示癌细胞并非只是从外部摄入更多这类氨基酸,而是重构其内部代谢,将葡萄糖转化为这些氨基酸。此代谢绕道中的关键酶PHGDH活性增强,并且对肿瘤在低天冬酰胺环境下恢复生长至关重要。
内部应对应激与DNA损伤
为什么丝氨酸生成的增强如此重要?研究表明,天冬酰胺缺乏会导致活性氧(ROS)激增——这些化学性强的副产物会损害DNA。丝氨酸和甘氨酸是合成谷胱甘肽的关键原料,谷胱甘肽是细胞主要的抗氧化剂之一。通过提高PHGDH驱动的丝氨酸生成,淋巴瘤细胞强化了其抗氧化防线,控制了氧化应激并减少了DNA损伤。当用专门的抑制剂或通过沉默PHGDH基因阻断其功能时,癌细胞积累了更多氧化应激,受到更严重的DNA损伤,并且在体外细胞培养和小鼠体内的L-天冬酰胺酶治疗期间恢复能力大幅下降。
暴露出的对DNA修复的依赖
天冬酰胺饥饿引起的DNA损伤不仅是副作用——它揭示了一种新的脆弱性。承受这种应激的细胞激活了以PARP1和PARP2酶活性升高为标志的修复程序,这些酶帮助修复断裂的DNA链。作者推测,如果肿瘤细胞已经高度依赖这一修复途径以存活L-天冬酰胺酶诱导的损伤,那么阻断PARP可能会将它们推向崩溃的边缘。他们将已获批的PARP抑制剂奥拉帕利(Olaparib,常用于某些乳腺癌和卵巢癌)与L-天冬酰胺酶联合使用进行测试。在淋巴瘤细胞和小鼠体内,这一组合诱导的肿瘤细胞死亡远多于任何单药,并且更长时间延缓了疾病进展。值得注意的是,同样的药物组合也抑制了一个无已知DNA修复缺陷的结直肠癌模型的生长,表明这一策略可能超出传统PARP敏感肿瘤的适用范围。
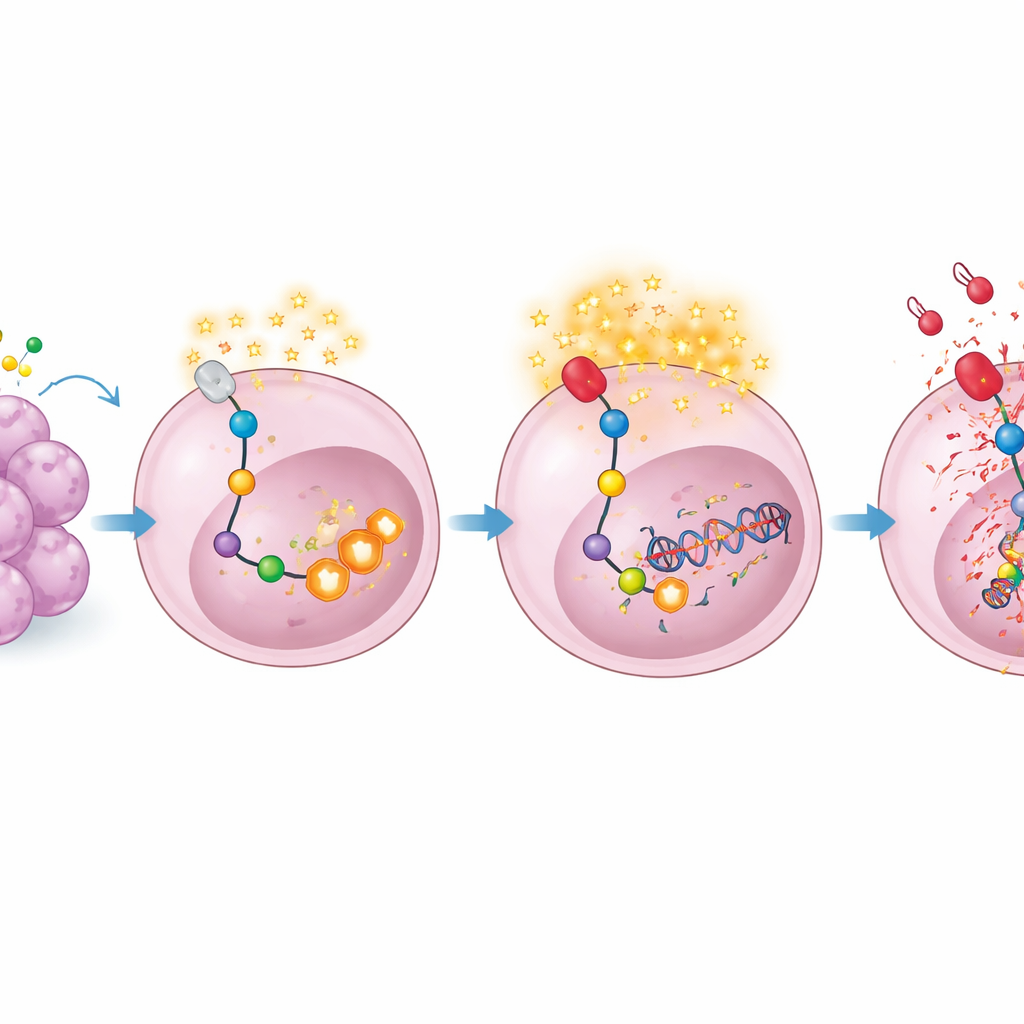
为更聪明的组合疗法打开大门
这项工作显示,当L-天冬酰胺酶将肿瘤逼入代谢困境时,肿瘤通过重编程代谢来减轻氧化应激并修复由此产生的DNA损伤。这种快速的适应依赖于PHGDH驱动的丝氨酸生成以及PARP介导的DNA修复。通过加入如奥拉帕利这样的PARP抑制剂,医生可能阻断这一生命线,将肿瘤生长的短暂放缓转变为更持久的反应。从实际角度看,该研究为在侵袭性B细胞淋巴瘤——以及可能的其他癌种——中联合使用L-天冬酰胺酶和PARP抑制剂提供了明确且有生物学依据的试验理由,而这些药物已在临床使用中。
引用: Aussel, A., Nemazanyy, I., Vandenberghe, A. et al. Tumor metabolic adaptation induced by L-asparaginase reveals a vulnerability to PARP1/2 inhibitor in B-cell lymphomas. Nat Commun 17, 3305 (2026). https://doi.org/10.1038/s41467-026-70066-2
关键词: L-天冬酰胺酶, B细胞淋巴瘤, 肿瘤代谢, PARP抑制剂, 丝氨酸生物合成