Clear Sky Science · ru
Метаболическая адаптация опухоли, вызванная L-аспарагиназой, выявляет уязвимость к ингибитору PARP1/2 при В-клеточных лимфомах
Превращение дефицита топлива у рака в новую слабость
Онкологи давно используют ферментный препарат L-аспарагиназу, чтобы лишать некоторые кровяные раки ключевого нутриента и заставлять их погибать. Однако многие опухоли со временем учатся переживать такую «диету» и снова растут, оставляя пациентам меньше вариантов лечения. В этом исследовании ставится простой, но важный вопрос: что именно делают раковые клетки, чтобы избежать голодания, и можно ли этот путь спасения обратить против них с помощью уже имеющихся лекарств?
Как препарат голодания борется с кровяными раками
L-аспарагиназа действует, очищая кровь от аминокислоты аспарагина. Некоторые клетки лейкемии и лимфомы не способны самостоятельно синтезировать достаточно аспарагина, поэтому при снижении его уровня в крови они ослабевают и погибают. На мышиных моделях В-клеточных лимфом исследователи подтвердили, что препарат первоначально может сильно замедлять рост опухоли. Тем не менее при продолжительном лечении опухоли в конечном счёте возвращались. Важно, что препарат по-прежнему был активен в плазме крови, что означает: опухоль не просто «перепасла» терапию — она адаптировалась более тонким способом.
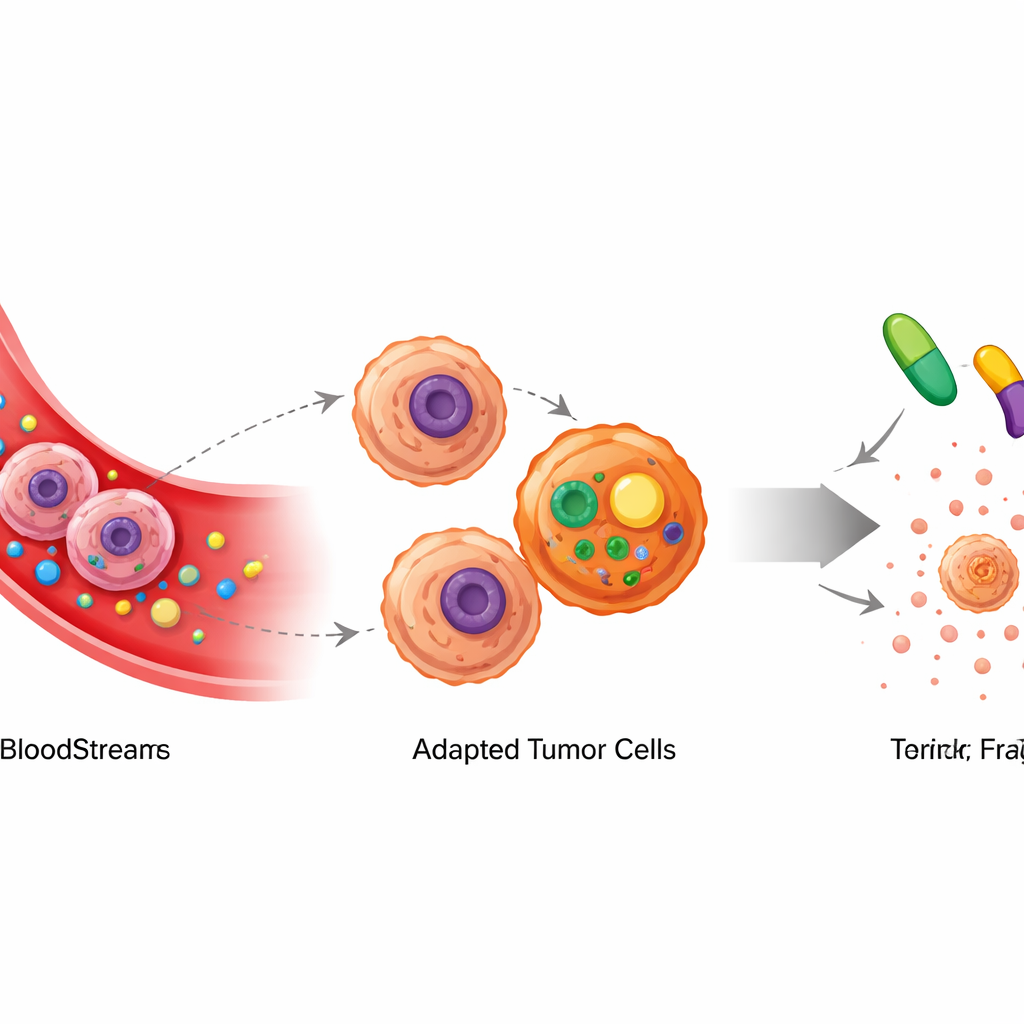
Метаболическая объездная: синтез новых строительных блоков
Чтобы выяснить, как опухоли адаптировались, команда внимательно измерила сотни малых молекул внутри раковых клеток, взятых у леченных и нелеченных мышей. Они обнаружили резкое повышение уровней двух родственных аминокислот — серина и глицина — в опухолях, подвергшихся воздействию L-аспарагиназы. С помощью меченых питательных веществ в качестве трассеров показали, что раковые клетки не просто забирали больше этих аминокислот из окружения — они перестроили свою внутреннюю химию, чтобы синтезировать их из глюкозы. Ключевой фермент в этой объездной, PHGDH, стал более активным и оказался необходимым для возобновленного роста клеток в условиях дефицита аспарагина.
Борьба со стрессом и повреждением ДНК изнутри
Почему увеличение производства серина так важно? Исследование показывает, что голодание по аспарагину вызывает всплеск реактивных форм кислорода — химически агрессивных побочных продуктов, которые могут повреждать ДНК. Серин и глицин являются ключевыми компонентами для синтеза глутатиона, одного из главных антиоксидантов клетки. Увеличив производство серина за счёт активности PHGDH, лимфомные клетки усиливали свою антиоксидантную защиту, сдерживали окислительный стресс и ограничивали повреждение ДНК. Когда PHGDH блокировали — либо с помощью специфического ингибитора, либо подавляя ген — раковые клетки накапливали больше окислительного стресса, терпели более серьёзные повреждения ДНК и значительно хуже восстанавливались во время лечения L-аспарагиназой как в культурах клеток, так и у мышей.
Обнажённая зависимость от репарации ДНК
Повреждение ДНК при голодании по аспарагину оказалось не просто побочным эффектом — оно выявило новую уязвимость. Клетки под этим стрессом активировали программу репарации, характеризующуюся повышенной активностью ферментов PARP1 и PARP2, которые помогают ремонтировать разрывы ДНК. Авторы предположили, что если опухолевые клетки стали сильно зависимы от этого пути репарации для выживания при повреждении, вызванном L-аспарагиназой, то блокада PARP может добить их. Они протестировали одобренный ингибитор PARP Олапариб, который обычно применяется при некоторых раках груди и яичников, вместе с L-аспарагиназой. В лимфомных клетках и у мышей сочетание вызвало гораздо более массовую гибель опухолевых клеток и дольше замедляло заболевание, чем каждый препарат в отдельности. Примечательно, что та же пара лекарств также сдерживала рост модели колоректального рака без известных дефектов репарации ДНК, что указывает на то, что подход может работать и за пределами классически PARP-чувствительных опухолей.
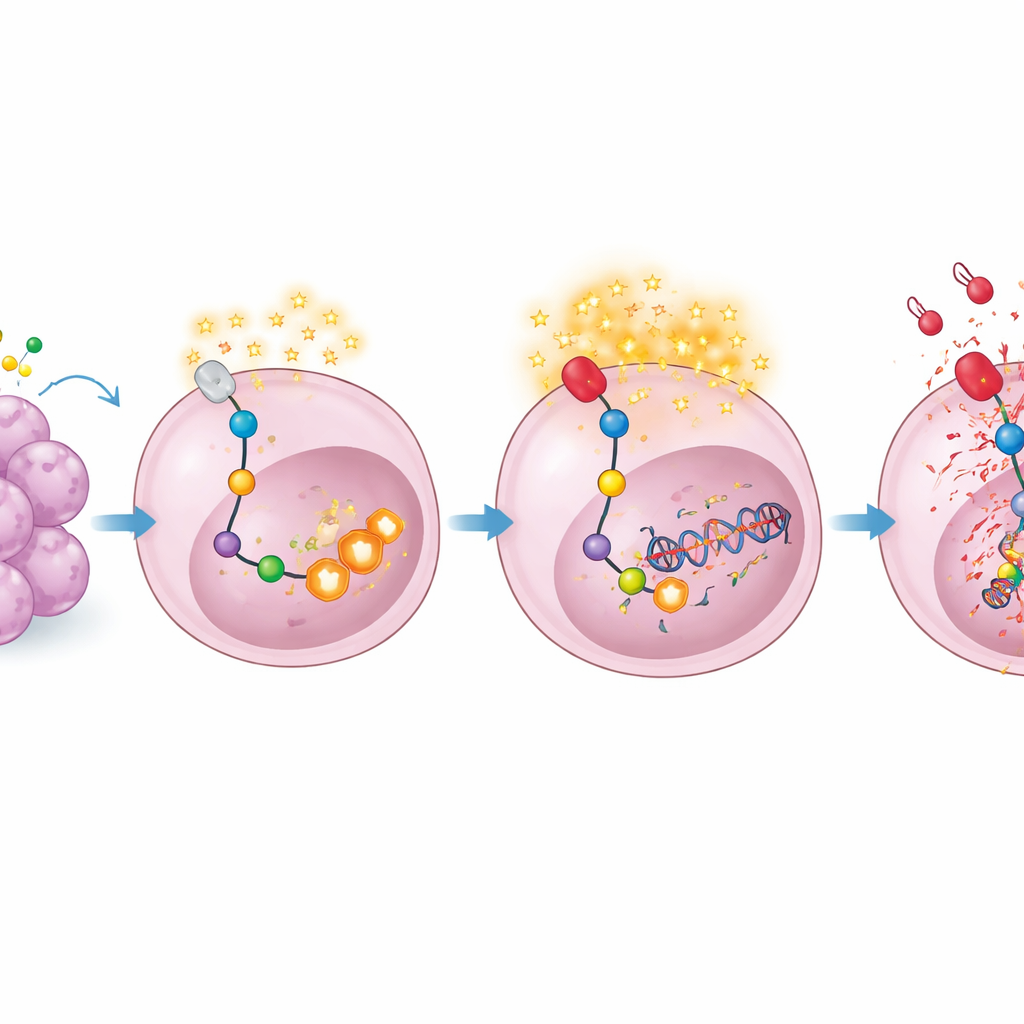
Открывая путь к более разумным комбинациям
Эта работа показывает, что когда L-аспарагиназа загоняет опухоли в метаболический угол, они реагируют перестройкой химии — чтобы смягчить окислительный стресс и ремонтировать вызванные им повреждения ДНК. Быстрая адаптация опирается на производство серина, управляемое PHGDH, и на PARP-зависимую репарацию ДНК. Добавляя ингибитор PARP, такой как Олапариб, клиницисты могут блокировать эту спасительную ниточку и превратить временное замедление роста опухоли в более стойкий ответ. С практической точки зрения исследование даёт чёткое биологически обоснованное обоснование для испытаний сочетания L-аспарагиназы и ингибиторов PARP при агрессивных В-клеточных лимфомах — и, возможно, при других раках — с использованием препаратов, уже применяемых в клинике.
Цитирование: Aussel, A., Nemazanyy, I., Vandenberghe, A. et al. Tumor metabolic adaptation induced by L-asparaginase reveals a vulnerability to PARP1/2 inhibitor in B-cell lymphomas. Nat Commun 17, 3305 (2026). https://doi.org/10.1038/s41467-026-70066-2
Ключевые слова: L-аспарагиназа, В-клеточная лимфома, метаболизм опухоли, ингибитор PARP, биосинтез серина