Clear Sky Science · pt
Adaptação metabólica tumoral induzida por L-asparaginase revela vulnerabilidade a inibidor de PARP1/2 em linfomas de células B
Transformando a escassez de combustível do câncer em uma nova fraqueza
Médicos oncologistas usam há muito uma enzima medicamentosa chamada L-asparaginase para privar certos cânceres do sangue de um nutriente-chave e forçá-los a morrer. Ainda assim, muitos tumores acabam aprendendo a conviver com essa “dieta” imposta e voltam a crescer, deixando os pacientes com menos opções de tratamento. Este estudo faz uma pergunta simples, porém importante: o que exatamente as células cancerosas fazem para escapar dessa privação, e esse próprio caminho de fuga pode ser usado contra elas com medicamentos já existentes?
Como um medicamento de privação combate cânceres sanguíneos
A L-asparaginase age eliminando o aminoácido asparagina da corrente sanguínea. Algumas células de leucemia e linfoma não conseguem produzir asparagina suficiente por conta própria, então quando o suprimento no sangue fica baixo, elas falham e morrem. Em modelos murinos de linfomas de células B, os pesquisadores confirmaram que esse medicamento pode retardar fortemente o crescimento tumoral a princípio. Mesmo com tratamento contínuo, porém, os tumores eventualmente reapareceram. Importante: o fármaco ainda estava ativo no sangue, o que significa que o câncer não havia simplesmente “esperado” o tratamento passar — havia se adaptado de forma mais sutil.
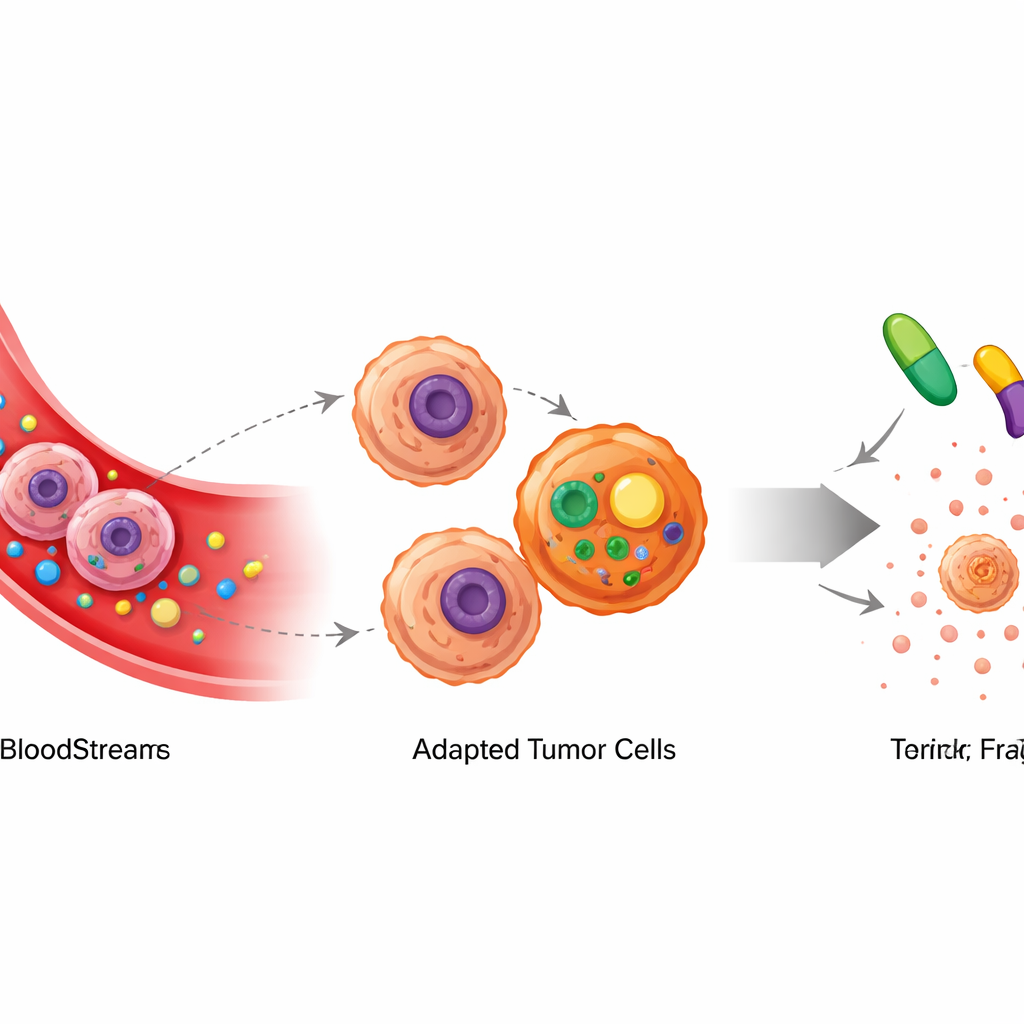
Desvio metabólico: produzindo novos blocos de construção
Para descobrir como os tumores se adaptaram, a equipe mediu cuidadosamente centenas de pequenas moléculas dentro de células cancerosas retiradas de camundongos tratados e não tratados. Eles observaram um aumento marcante em dois aminoácidos relacionados, serina e glicina, em tumores expostos à L-asparaginase. Usando nutrientes marcados como traçadores, mostraram que as células cancerosas não estavam apenas captando mais desses aminoácidos do ambiente — estavam reconstruindo sua química interna para fabricá-los a partir da glicose. Uma enzima-chave nesse desvio, chamada PHGDH, tornou-se mais ativa e foi essencial para o novo crescimento das células em condições pobres em asparagina.
Combatendo o estresse e o dano ao DNA de dentro
Por que esse aumento na produção de serina importa tanto? O estudo mostra que a privação de asparagina cria uma explosão de espécies reativas de oxigênio — subprodutos quimicamente agressivos que podem danificar o DNA. Serina e glicina são ingredientes cruciais para fabricar glutationa, um dos principais antioxidantes da célula. Ao aumentar a produção de serina dirigida pela PHGDH, as células do linfoma reforçaram sua barreira antioxidante, mantiveram o estresse oxidativo sob controle e limitaram o dano ao DNA. Quando a PHGDH foi bloqueada, seja com um inibidor específico ou silenciando seu gene, as células cancerosas acumularam mais estresse oxidativo, sofreram maior dano ao DNA e ficaram muito menos capazes de se recuperar durante o tratamento com L-asparaginase, tanto em culturas celulares quanto em camundongos.
Dependência exposta na reparação do DNA
O dano ao DNA causado pela privação de asparagina revelou-se mais do que um efeito colateral — expôs uma nova vulnerabilidade. Células sob esse estresse ativaram um programa de reparo marcado por aumento da atividade das enzimas PARP1 e PARP2, que ajudam a consertar quebras nas fitas de DNA. Os autores raciocinaram que, se as células tumorais se tornaram fortemente dependentes dessa via de reparo para sobreviver ao dano induzido pela L-asparaginase, então bloquear a PARP poderia levá-las ao colapso. Testaram o medicamento aprovado que bloca PARP, Olaparibe, comumente usado em alguns cânceres de mama e ovário, juntamente com L-asparaginase. Em células de linfoma e em camundongos, a combinação desencadeou muito mais morte celular tumoral e retardou a progressão da doença por muito mais tempo do que qualquer um dos fármacos isolados. Notavelmente, a mesma combinação também prejudicou o crescimento de um modelo de câncer colorretal que não apresentava defeitos de reparo de DNA conhecidos, sugerindo que essa abordagem pode funcionar além dos tumores classicamente sensíveis a PARP.
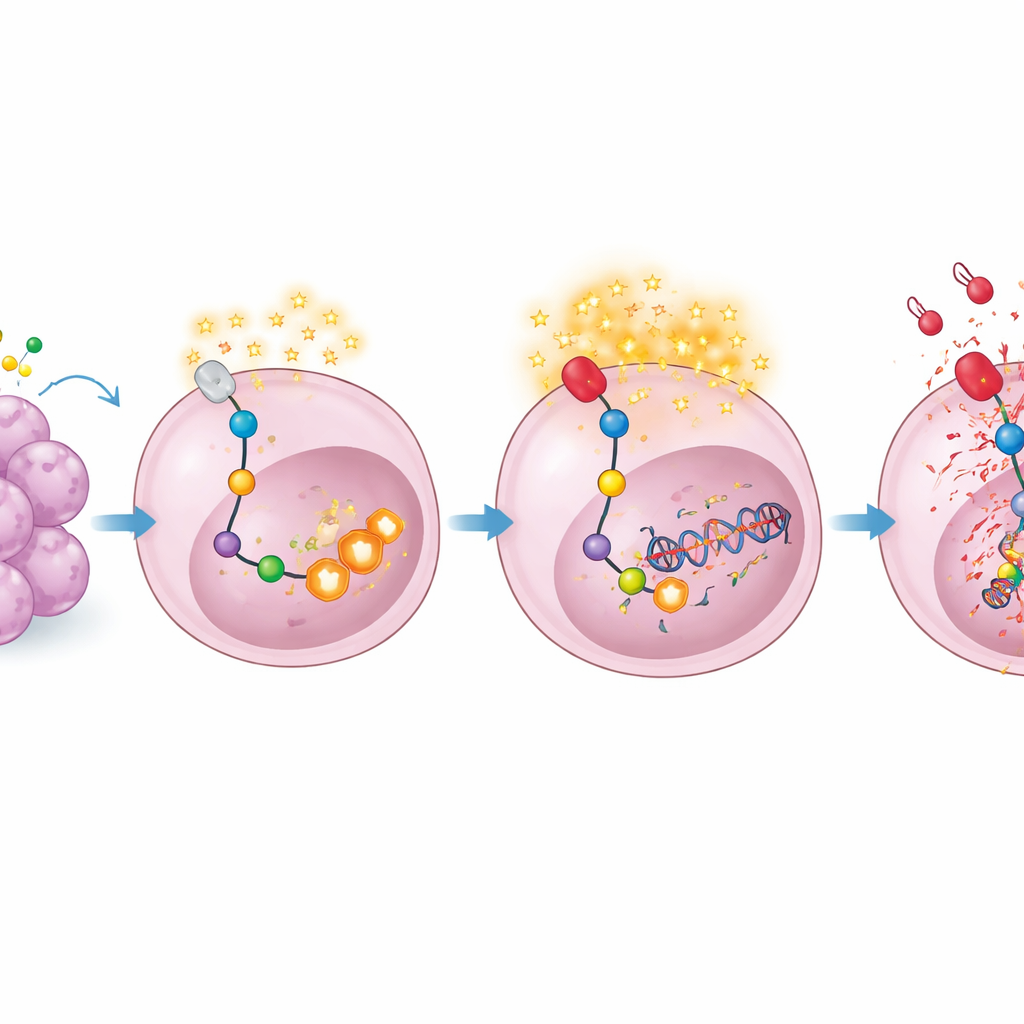
Abrindo a porta para combinações mais inteligentes
Este trabalho revela que, quando a L-asparaginase encurrala metabolicamente os tumores, eles respondem reprogramando sua química para atenuar o estresse oxidativo e reparar o dano ao DNA decorrente. Essa adaptação rápida depende da produção de serina dirigida por PHGDH e da reparação do DNA mediada por PARP. Ao adicionar um inibidor de PARP como o Olaparibe, os médicos podem bloquear essa tábua de salvação e transformar uma desaceleração temporária do crescimento tumoral em uma resposta mais duradoura. Em termos práticos, o estudo apresenta um argumento claro e biologicamente fundamentado para testar L-asparaginase e inibidores de PARP em combinação em linfomas agressivos de células B — e possivelmente em outros cânceres — usando fármacos que já estão em uso clínico.
Citação: Aussel, A., Nemazanyy, I., Vandenberghe, A. et al. Tumor metabolic adaptation induced by L-asparaginase reveals a vulnerability to PARP1/2 inhibitor in B-cell lymphomas. Nat Commun 17, 3305 (2026). https://doi.org/10.1038/s41467-026-70066-2
Palavras-chave: L-asparaginase, Linfoma de células B, metabolismo tumoral, inibidor de PARP, biossíntese de serina