Clear Sky Science · sv
Tumors metaboliska anpassning som induceras av L-asparaginase avslöjar en sårbarhet för PARP1/2-hämmare i B-cellslymfom
Att göra cancerens bränslebrist till en ny svaghet
Onkologer har länge använt ett enzymläkemedel kallat L-asparaginase för att svälta vissa blodcancerformer på en nyckelnäringsämne och tvinga dem till celldöd. Ändå lär sig många tumörer så småningom att överleva denna påtvingade ”diet” och växer tillbaka, vilket lämnar patienterna med färre behandlingsalternativ. Denna studie ställer en enkel men viktig fråga: vad gör cancercellerna exakt för att undkomma denna svält, och kan just den flyktvägen vändas mot dem med redan tillgängliga läkemedel?
Hur ett svältningsläkemedel bekämpar blodcancer
L-asparaginase verkar genom att rensa aminosyran asparagin ur blodomloppet. Vissa leukemi- och lymfomceller kan inte producera tillräckligt med asparagin själva, så när tillgången i blodet blir låg försvagas de och dör. I musmodeller av B-cellslymfom bekräftade forskarna att detta läkemedel initialt kan kraftigt fördröja tumörtillväxt. Även vid fortsatt behandling återkom dock tumörerna så småningom. Viktigt är att läkemedlet fortfarande var aktivt i blodet, vilket betyder att cancern inte bara hade ”väntat ut” behandlingen — den hade anpassat sig på ett mer subtilt sätt.
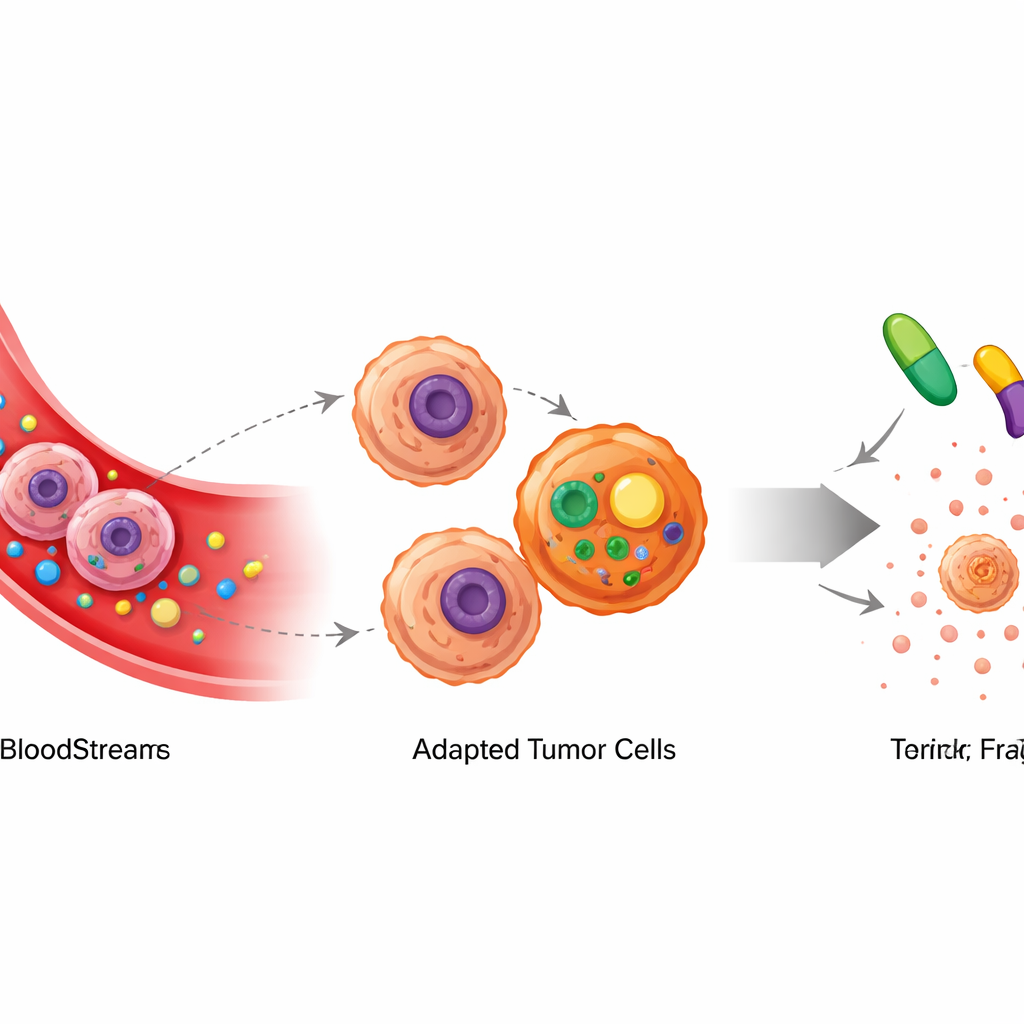
Metabolisk omväg: att bygga nya byggstenar
För att ta reda på hur tumörerna anpassade sig mätte teamet noggrant hundratals små molekyler i cancerceller tagna från behandlade och obehandlade möss. De observerade en markant ökning av två besläktade aminosyror, serin och glycin, i tumörer exponerade för L-asparaginase. Genom att använda märkta näringsämnen som spårämnen visade de att cancercellerna inte bara tog upp mer av dessa aminosyror från omgivningen — de byggde om sin interna kemi för att tillverka dem från glukos. Ett nyckelenzym i denna omväg, kallat PHGDH, blev mer aktivt och var avgörande för cellernas återupptagna tillväxt under asparagin-snåla förhållanden.
Kämpa mot stress och DNA-skada inifrån
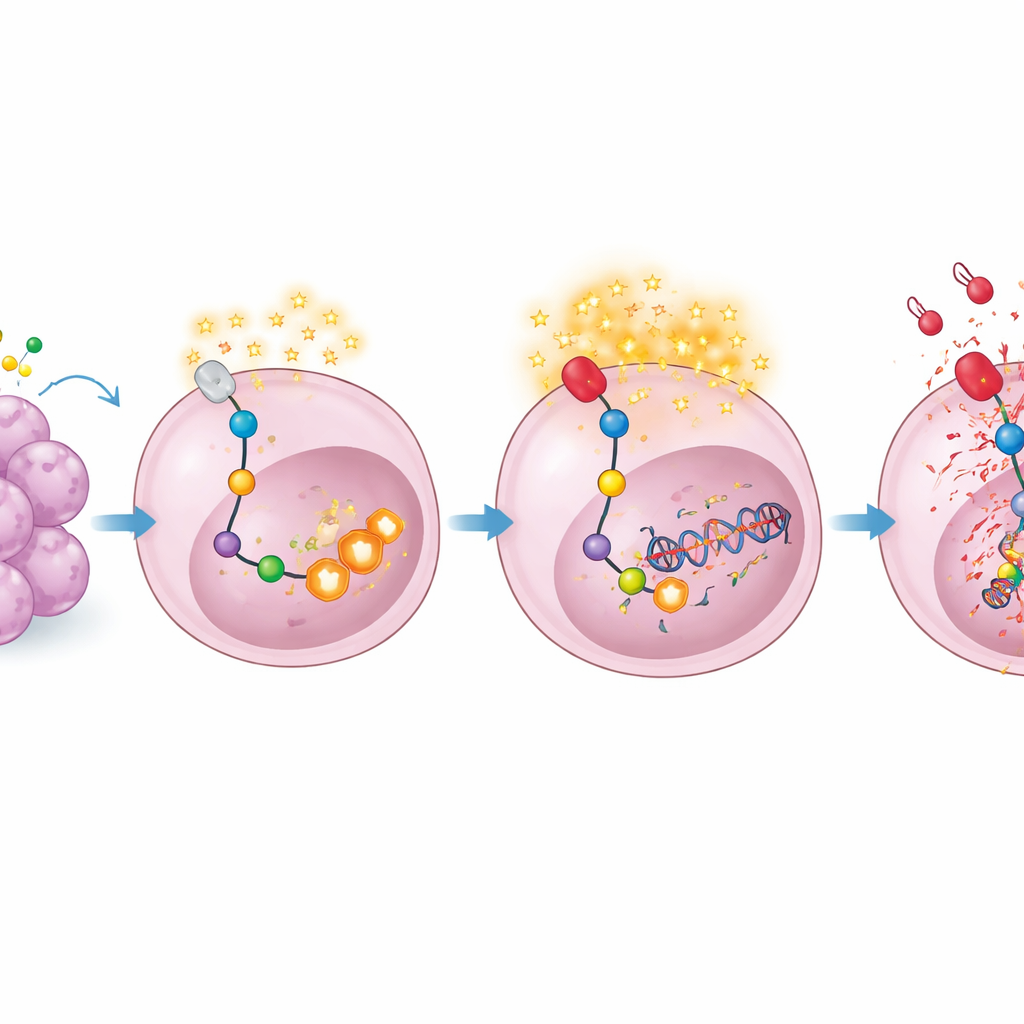
Varför spelar denna ökade serinproduktion så stor roll? Studien visar att asparaginbrist skapar en våg av reaktiva syreradikaler — kemiskt aggressiva biprodukter som kan skada DNA. Serin och glycin är viktiga ingredienser för att tillverka glutathion, en av cellens huvudantioxidanter. Genom att öka PHGDH-driven serinproduktion stärkte lymfomcellerna sitt antioxidativa skydd, höll oxidativ stress i schack och begränsade DNA-skador. När PHGDH blockerades, antingen med en specialiserad hämmare eller genom att tysta dess gen, samlades mer oxidativ stress i cancercellerna, de drabbades av större DNA-skador och återhämtade sig betydligt sämre under L-asparaginase-behandling både i cellkulturer och i möss.
Exponerat beroende av DNA-reparation
DNA-skadorna som följde av asparaginbrist visade sig vara mer än en bieffekt — de avslöjade en ny sårbarhet. Celler under denna stress aktiverade ett reparationsprogram kännetecknat av ökad aktivitet hos enzymerna PARP1 och PARP2, som hjälper till att laga brutna DNA-strängar. Författarna resonerade att om tumörceller blivit starkt beroende av denna reparationsväg för att överleva L-asparaginase-inducerad skada, så skulle blockering av PARP kunna få dem att tippa över kanten. De testade den godkända PARP-hämmande substansen Olaparib, som används vid vissa bröst- och äggstockscancerformer, tillsammans med L-asparaginase. I lymfomceller och i möss gav kombinationen betydligt mer tumörcelldöd och fördröjde sjukdomen mycket längre än något av läkemedlen ensamt. Anmärkningsvärt är att samma läkemedelspair även hindrade tillväxten i en kolorektalcancermodell utan kända DNA-reparationsdefekter, vilket tyder på att detta tillvägagångssätt kan fungera utöver de klassiska PARP-känsliga tumörerna.
Öppnar dörren för smartare kombinationer
Denna studie visar att när L-asparaginase tvingar tumörer in i ett metabolt hörn svarar de genom att omkoppla sin kemi för att dämpa oxidativ stress och reparera den därav följande DNA-skadan. Denna snabba anpassning beror på PHGDH-driven serinproduktion och på PARP-medierad DNA-reparation. Genom att lägga till en PARP-hämmare såsom Olaparib kan läkare kanske blockera denna livlina och förvandla en tillfällig inbromsning av tumörtillväxt till en mer varaktig respons. I praktiska termer lägger studien fram ett tydligt, biologiskt grundat argument för att testa L-asparaginase och PARP-hämmare tillsammans vid aggressiva B-cellslymfom — och möjligen även vid andra cancerformer — med läkemedel som redan används i kliniken.
Citering: Aussel, A., Nemazanyy, I., Vandenberghe, A. et al. Tumor metabolic adaptation induced by L-asparaginase reveals a vulnerability to PARP1/2 inhibitor in B-cell lymphomas. Nat Commun 17, 3305 (2026). https://doi.org/10.1038/s41467-026-70066-2
Nyckelord: L-asparaginase, B-cellslymfom, tumörmetabolism, PARP-hämmare, serinbiosyntes