Clear Sky Science · zh
含端粒重复的RNA G-四链体触发由ZBP1介导的细胞死亡
细胞如何决定何时自我终结
我们的细胞内置警报系统,能感知严重异常并触发可控的自我毁灭程序。这一过程有助于阻止受损或癌前细胞演变成肿瘤,也能抵御感染。这里描述的研究揭示了一种令人意外的方式:一种特定的细胞感受器识别位于染色体末端的遗传物质中的异常结构,并据此决定细胞是否应当死亡。
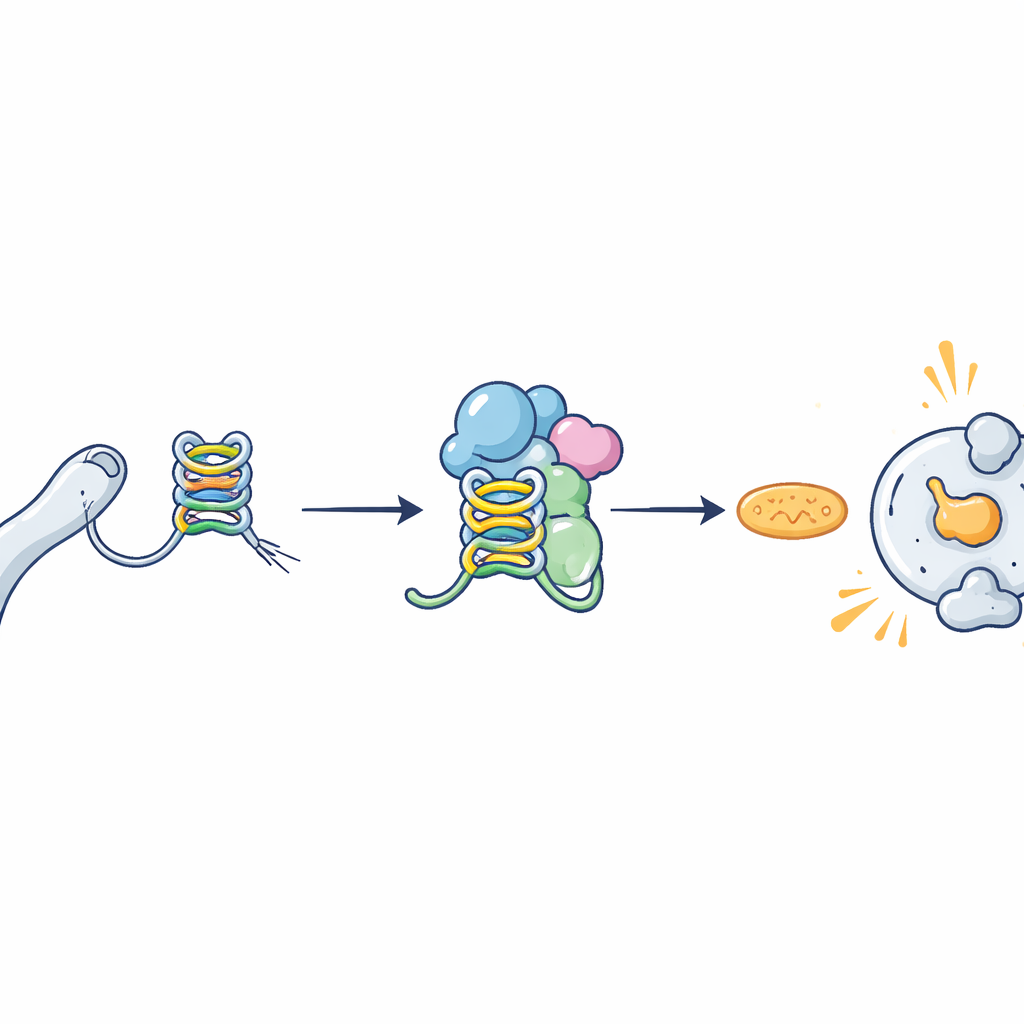
染色体末端的奇异形状
人类染色体末端有被称为端粒的保护帽,由重复的DNA序列构成。这些区域会被抄录成称为TERRA的RNA分子。由于富含鸟嘌呤,TERRA链可以折叠成紧凑的层叠状结构,称为G‑四链体,而不是保持简单的线性链。这些不寻常的折叠越来越被视为细胞内的重要调控元件,且与癌症、脑部疾病和病毒感染有关。研究人员想知道,TERRA中的这种G‑四链体形状是否正是解释细胞死亡感受蛋白ZBP1如何识别受损端粒的缺失环节。
细胞的结构形状感受器
ZBP1是先天免疫系统的一部分,是机体对危险的第一道防线。它巡逻细胞,寻找异常的遗传物质,激活时可引发炎症反应和程序性细胞死亡。较短的ZBP1变体ZBP1‑S最近被证明能特异性响应TERRA并帮助清除处于危机中的细胞。然而,ZBP1‑S感知TERRA的具体特征尚不清楚。通过生化实验和结构建模,作者发现ZBP1的两个区域,称为Zα结构域,可以紧密且直接结合TERRA的G‑四链体形式,但不能结合无法折叠成这些形状的突变TERRA。仅携带其中一个Zα结构域(Zα2)的ZBP1‑S仍能以高亲和力识别TERRA G‑四链体,尤其在多个G‑四链体单元堆叠在一起时。
从结合到致命决定
识别危险物质只是第一步;ZBP1还必须组装成更大的复合体以发出强烈的死亡信号。团队证明,当细胞内存在能形成G‑四链体的正常TERRA时,ZBP1‑S分子会聚集成长丝状结构,这是激活的标志。无法形成G‑四链体的突变TERRA则不能诱导这种聚集。在工程化表达ZBP1‑S的乳腺癌及其他细胞系中,能形成G‑四链体的TERRA开启了抗病毒和炎症基因并导致大量细胞死亡。这些效应依赖于ZBP1‑S的Zα2区域及线粒体上的下游伙伴MAVS,MAVS负责转导死亡信号。
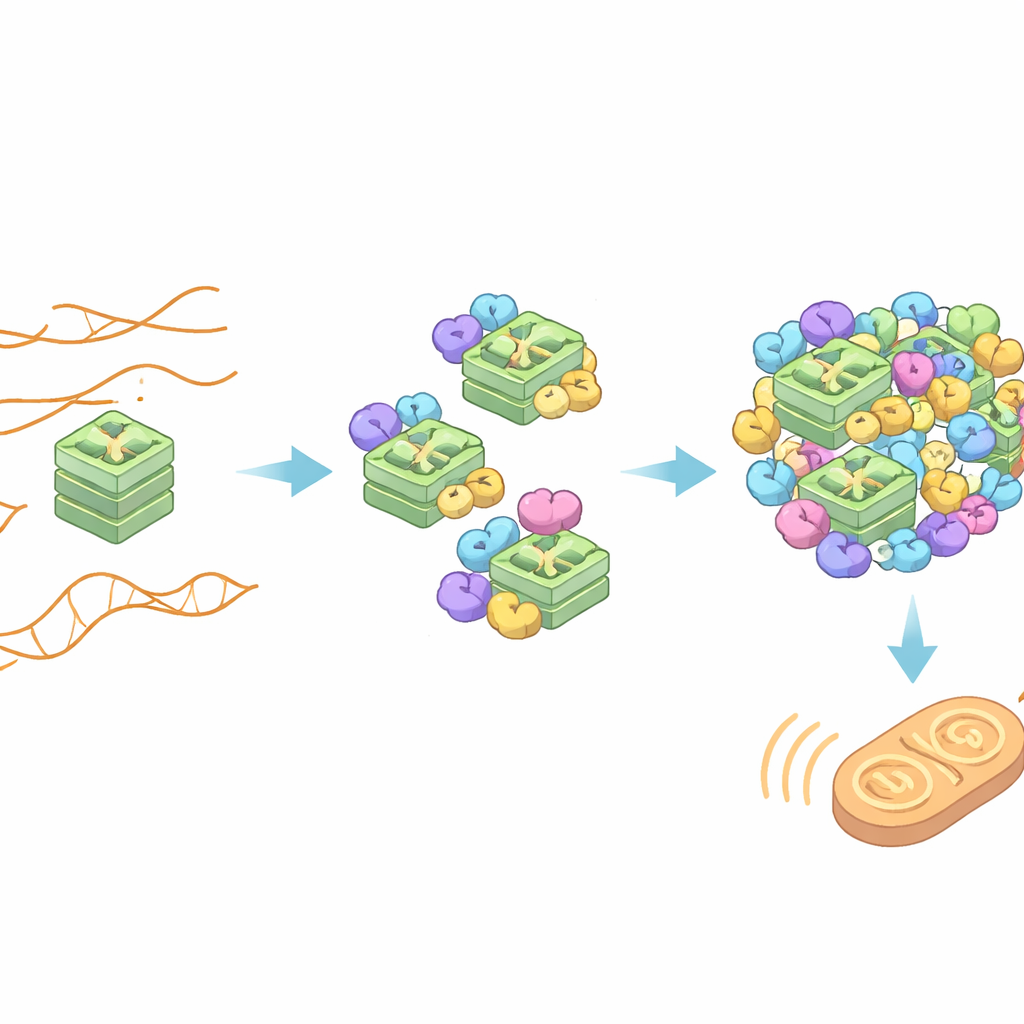
可抑制警报的小分子
既然ZBP1‑S的激活依赖于TERRA G‑四链体,坐落在这些结构上的化合物或许能阻断两者相互作用。研究人员测试了若干已知的G‑四链体结合化合物。其中两种,PDS和TMPyP4,在试管实验和活细胞中有效地与ZBP1‑S竞争结合TERRA G‑四链体。存在这些化合物时,ZBP1‑S未能聚集,炎症基因活性下降,死亡细胞减少。其他G‑四链体药物效果则差得多,表明化合物与折叠RNA形状的具体结合方式决定了其是否能干扰ZBP1–TERRA的相互作用。
更广泛的意义与未来可能性
这项工作表明ZBP1‑S并非仅感知一般的类病毒物质;相反,它对端粒RNA中G‑四链体的三维形状具有特异性。通过锁定这些紧凑折叠,ZBP1‑S组装成大规模簇,通过线粒体发出信号,清除可能走向癌变的细胞。与此同时,经过谨慎选择的小分子可以通过屏蔽G‑四链体结构来抑制该通路。对于非专业读者来说,关键结论是:细胞的生死抉择可能取决于其遗传物质中的细微扭结和结状结构——这些形状未来可能被药物靶向,用以促进危险细胞的清除或防止有害的炎症性细胞死亡。
引用: Qin, G., Zhao, C., Gao, C. et al. Telomeric repeat-containing RNA G-quadruplexes trigger ZBP1-mediated cell death. Nat Commun 17, 3076 (2026). https://doi.org/10.1038/s41467-026-69989-7
关键词: 先天免疫, 端粒, G-四链体RNA, 程序性细胞死亡, 癌症预防