Clear Sky Science · de
Telomeric repeat-containing RNA G-quadruplexes trigger ZBP1-mediated cell death
Wie Zellen entscheiden, sich selbst zu zerstören
Unsere Zellen verfügen über eingebaute Alarmsysteme, die erkennen können, wenn etwas ernsthaft schiefgelaufen ist, und dann eine kontrollierte Form der Selbstzerstörung auslösen. Dieser Prozess hilft, beschädigte oder präkanzeröse Zellen daran zu hindern, zu Tumoren zu werden, und er bekämpft außerdem Infektionen. Die hier beschriebene Studie enthüllt eine überraschende Art, wie ein bestimmter zellulärer Sensor ungewöhnliche Formen genetischen Materials an den Enden der Chromosomen erkennt und diese Information nutzt, um zu entscheiden, wann eine Zelle sterben sollte.
Merkwürdige Strukturen an Chromosomenenden
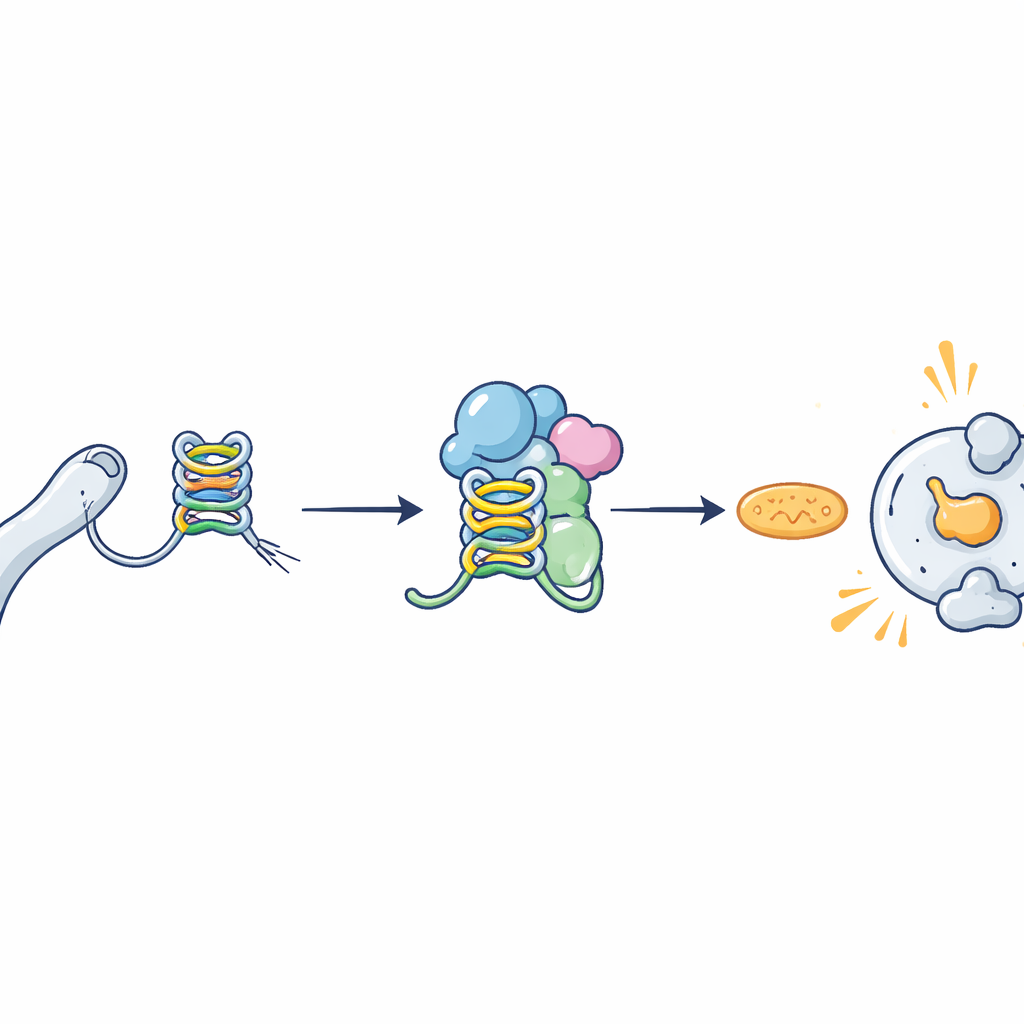
Menschliche Chromosomen enden in schützenden Kappen, den Telomeren, die aus wiederholten DNA‑Sequenzen bestehen. Diese Bereiche werden in RNA‑Moleküle namens TERRA kopiert. Weil sie reich an der Baustein‑Guanin sind, können TERRA‑Stränge kompakte, gestapelte Formen bilden, sogenannte G‑Quadruplexe, anstatt als einfache Stränge vorzuliegen. Diese ungewöhnlichen Faltungen werden zunehmend als wichtige Steuerungselemente in Zellen erkannt und mit Krebs, Erkrankungen des Gehirns und Virusinfektionen in Verbindung gebracht. Die Forscher fragten, ob solche G‑Quadruplex‑Formen in TERRA das fehlende Puzzlestück sein könnten, das erklärt, wie das zelltodauslösende Sensorprotein ZBP1 gestörte Telomere erkennt.
Der strukturelle Formensensor der Zelle
ZBP1 ist Teil der angeborenen Immunität, der ersten Verteidigungslinie des Körpers gegen Gefahren. Es patrouilliert in Zellen auf der Suche nach abnormalem genetischem Material und kann, wenn es aktiviert wird, Entzündungsreaktionen und programmierten Zelltod auslösen. Eine kürzere Version dieses Proteins, ZBP1‑S, wurde kürzlich gezeigt, dass sie spezifisch auf TERRA reagiert und dabei hilft, Zellen in der Krise zu entfernen. Welches genaue Merkmal von TERRA ZBP1‑S jedoch wahrnahm, blieb unklar. Durch biochemische Tests und Strukturmodellierung fanden die Autoren heraus, dass zwei Regionen von ZBP1, die sogenannten Zα‑Domänen, stark und direkt an G‑Quadruplex‑Formen von TERRA binden, jedoch nicht an mutierte TERRA, die sich nicht zu diesen Formen falten kann. ZBP1‑S, das nur eine dieser Domänen (Zα2) trägt, erkannte TERRA‑G‑Quadruplexe weiterhin mit hoher Affinität, insbesondere wenn mehrere G‑Quadruplex‑Einheiten gestapelt vorlagen.
Vom Binden zur tödlichen Entscheidung
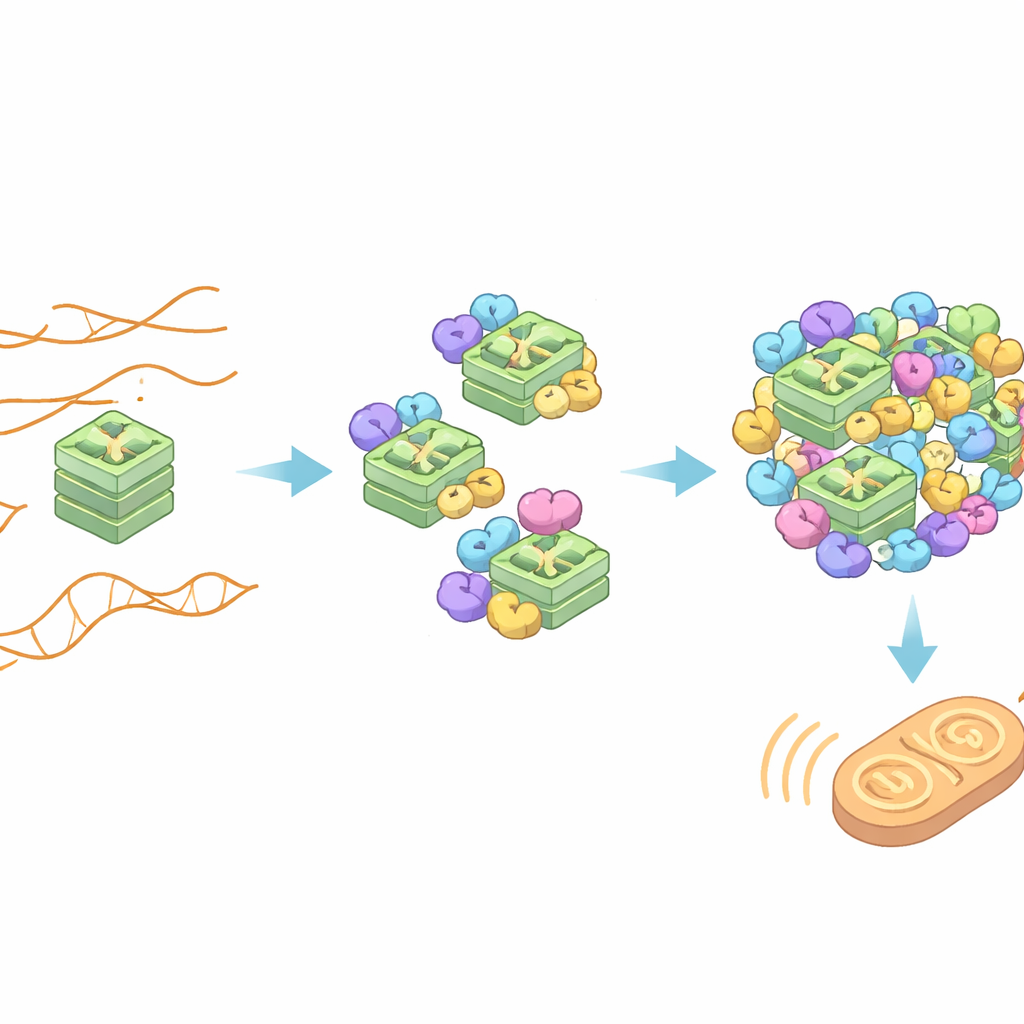
Das Erkennen gefährlichen Materials ist nur der erste Schritt; ZBP1 muss sich auch zu größeren Komplexen zusammenlagern, um ein starkes Todessignal zu senden. Das Team zeigte, dass, wenn normale TERRA, die G‑Quadruplexe bilden kann, in Zellen vorhanden war, sich ZBP1‑S‑Moleküle zu langen filamentartigen Strukturen zusammenlagerten, ein Zeichen der Aktivierung. Mutierte TERRA, die keine G‑Quadruplexe bilden konnten, induzierten diese Clusterbildung nicht. In Brustkrebs‑ und anderen Zelllinien, die so verändert wurden, dass sie ZBP1‑S produzieren, schaltete das Vorhandensein TERRA‑bildender G‑Quadruplexe antivirale und entzündliche Gene ein und führte zu erheblichem Zelltod. Diese Effekte hingen sowohl von der Zα2‑Region von ZBP1‑S als auch von einem nachgeschalteten Partner an den Mitochondrien namens MAVS ab, der das Todessignal weiterleitet.
Kleine Moleküle, die den Alarm dämpfen können
Wenn die Aktivierung von ZBP1‑S von TERRA‑G‑Quadruplexen abhängt, könnten Chemikalien, die sich an diese Strukturen anlagern, die Wechselwirkung blockieren. Die Forscher testeten mehrere bekannte G‑Quadruplex‑bindende Verbindungen. Zwei davon, PDS und TMPyP4, konkurrierten in Reagenzglas‑Experimenten und in lebenden Zellen effektiv mit ZBP1‑S um den Zugang zu TERRA‑G‑Quadruplexen. In Gegenwart dieser Verbindungen bildete ZBP1‑S keine Cluster mehr, die Aktivität entzündlicher Gene ging zurück und weniger Zellen starben. Andere G‑Quadruplex‑Wirkstoffe waren deutlich weniger wirksam, was darauf hindeutet, dass die genaue Art und Weise, wie eine Verbindung die gefaltete RNA‑Form greift, bestimmt, ob sie die ZBP1–TERRA‑Partnerschaft stören kann.
Weiterreichende Implikationen und zukünftige Möglichkeiten
Diese Arbeit zeigt, dass ZBP1‑S nicht einfach generisches, viralähnliches Material wahrnimmt; vielmehr ist es auf die dreidimensionale Form von G‑Quadruplexen in telomerer RNA abgestimmt. Indem es sich an diese kompakten Faltungen heftet, bildet ZBP1‑S große Cluster, die über Mitochondrien Signale aussenden, um Zellen zu töten, die sich möglicherweise auf dem Weg zu Krebs befinden. Zugleich können sorgfältig ausgewählte kleine Moleküle diesen Pfad abschwächen, indem sie die G‑Quadruplex‑Strukturen vor ZBP1‑S abschirmen. Für eine allgemeine Leserschaft ist die Kernbotschaft: Die Entscheidung einer Zelle zu leben oder zu sterben kann von subtilen Drehungen und Verschlingungen ihres genetischen Materials abhängen — und diese Strukturen könnten eines Tages mit Medikamenten gezielt genutzt werden, um entweder die Entfernung gefährlicher Zellen zu fördern oder schädlichen entzündlichen Zelltod zu verhindern.
Zitation: Qin, G., Zhao, C., Gao, C. et al. Telomeric repeat-containing RNA G-quadruplexes trigger ZBP1-mediated cell death. Nat Commun 17, 3076 (2026). https://doi.org/10.1038/s41467-026-69989-7
Schlüsselwörter: angeborene Immunität, Telomere, G‑Quadruplex‑RNA, programmierter Zelltod, Krebsprävention