Clear Sky Science · it
I G-quadruplex dell'RNA contenente ripetizioni telomeriche attivano la morte cellulare mediata da ZBP1
Come le cellule decidono quando autodistruggersi
Le nostre cellule possiedono sistemi di allarme incorporati in grado di rilevare quando qualcosa è andato gravemente storto e quindi di innescare una forma controllata di autodistruzione. Questo processo aiuta a prevenire che cellule danneggiate o precancerose si trasformino in tumori e contribuisce anche a combattere le infezioni. Lo studio descritto qui svela un modo sorprendente in cui un particolare sensore cellulare riconosce forme insolite del materiale genetico alle estremità dei cromosomi e utilizza questa informazione per decidere quando una cellula debba morire.
Forme strane alle estremità dei cromosomi
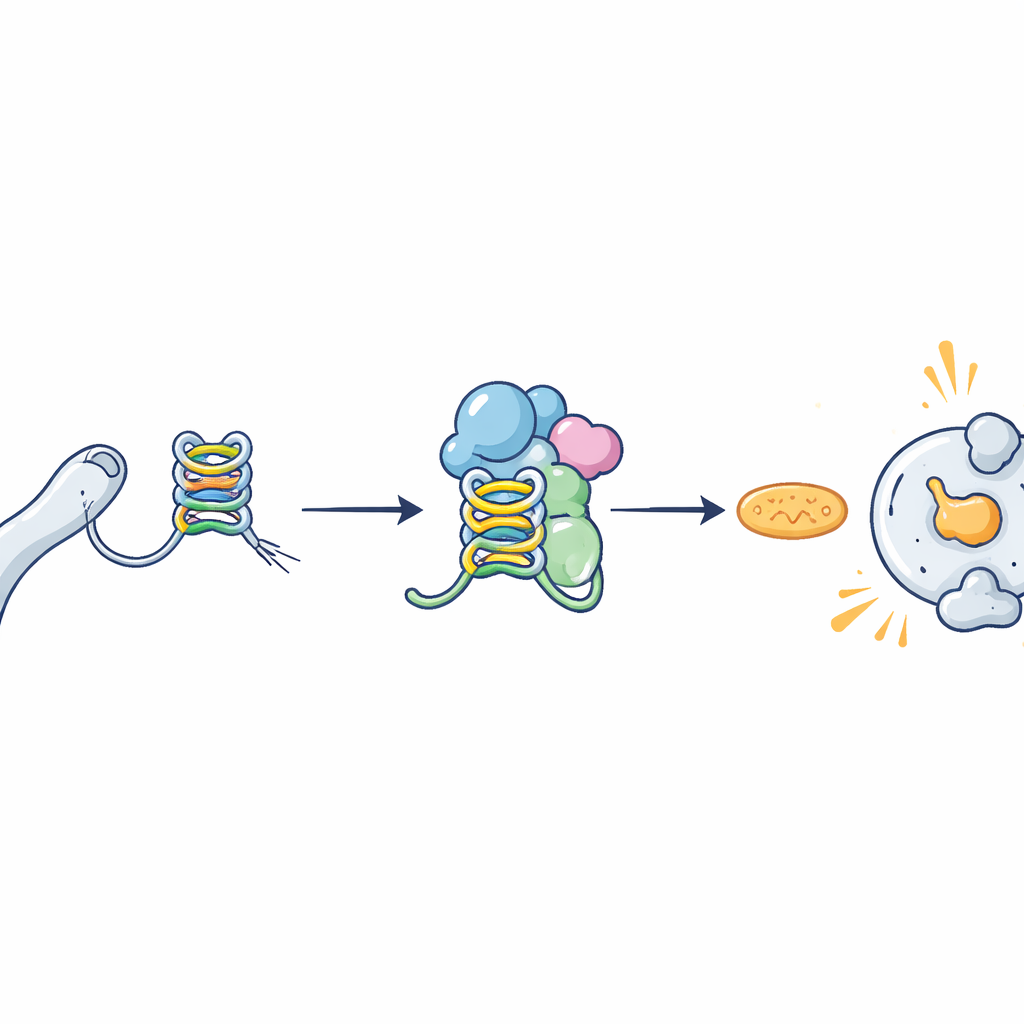
I cromosomi umani terminano con cappucci protettivi chiamati telomeri, costituiti da sequenze di DNA ripetute. Queste regioni vengono trascritte in molecole di RNA note come TERRA. Poiché sono ricche dell'nucleobase guanina, le catene di TERRA possono ripiegarsi in forme compatte e impilate chiamate G-quadruplex invece di rimanere semplici filamenti. Questi ripiegamenti insoliti sono sempre più riconosciuti come elementi di controllo importanti nelle cellule e sono stati collegati al cancro, a disturbi cerebrali e a infezioni virali. I ricercatori si sono chiesti se tali G-quadruplex nella TERRA potessero essere il tassello mancante che spiega come una proteina sensore della morte cellulare chiamata ZBP1 riconosce telomeri in difficoltà.
Il sensore strutturale della cellula
ZBP1 fa parte del sistema immunitario innato, la prima linea di difesa dell’organismo contro i pericoli. Pattuglia le cellule alla ricerca di materiale genetico anomalo e, quando attivata, può scatenare risposte infiammatorie e la morte cellulare programmata. Una versione più corta di questa proteina, ZBP1-S, era stata recentemente dimostrata rispondere in modo specifico alla TERRA e contribuire a eliminare le cellule in crisi. Tuttavia, la caratteristica esatta della TERRA che ZBP1-S riconosceva rimaneva poco chiara. Attraverso test biochimici e modellizzazione strutturale, gli autori hanno scoperto che due regioni di ZBP1, chiamate domini Zα, si legano saldamente e direttamente alle forme a G-quadruplex della TERRA ma non alla TERRA mutata che non può ripiegarsi in queste strutture. ZBP1-S, che porta solo uno di questi domini (Zα2), riconosce comunque le TERRA a G-quadruplex con alta affinità, in particolare quando più unità di G-quadruplex sono impilate tra loro.
Dal legame alla decisione letale
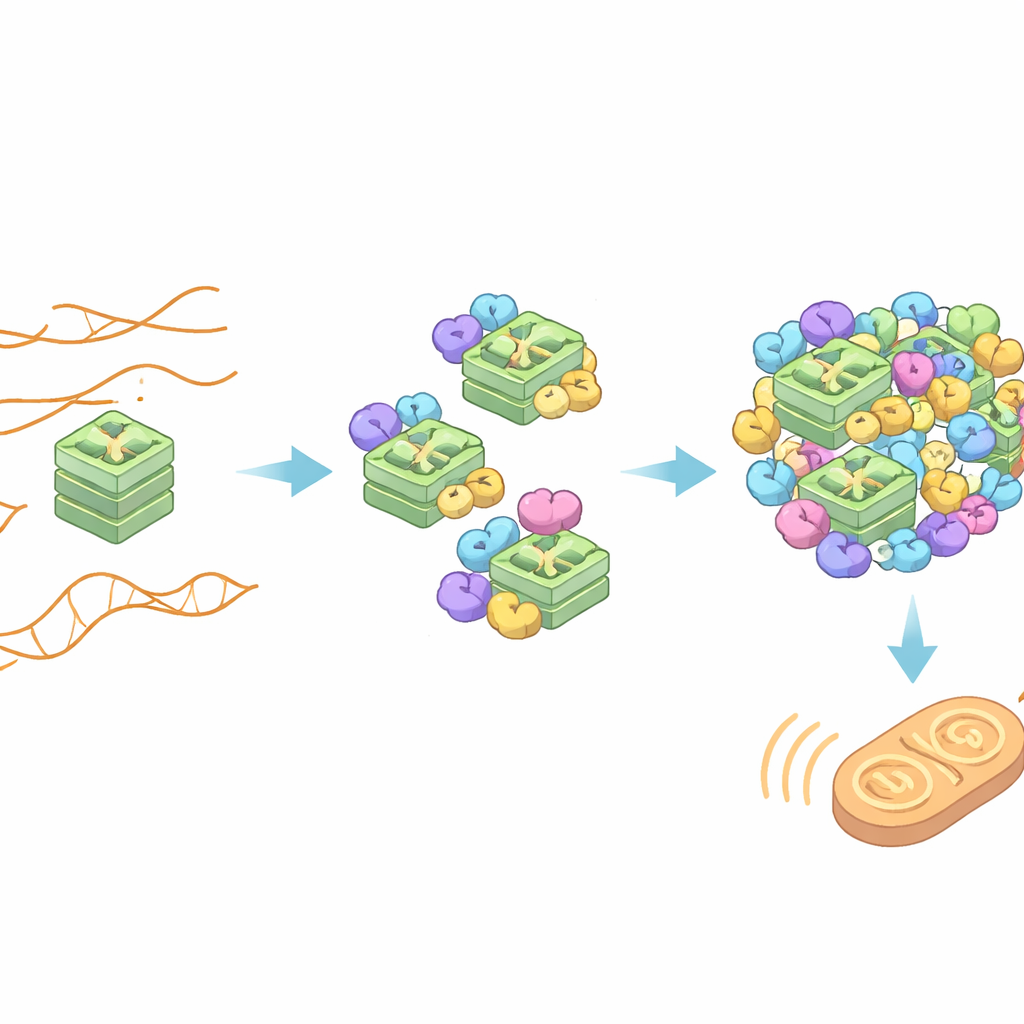
Riconoscere materiale pericoloso è solo il primo passo; ZBP1 deve anche assemblarsi in complessi più grandi per inviare un segnale di morte potente. Il gruppo ha mostrato che quando nelle cellule era presente TERRA normale in grado di formare G-quadruplex, le molecole di ZBP1-S si raggruppavano in lunghe strutture filamentose, segno di attivazione. La TERRA mutata incapace di formare G-quadruplex non riusciva a indurre questo clustering. In linee cellulari di carcinoma mammario e in altre linee ingegnerizzate per esprimere ZBP1-S, la presenza di TERRA capace di formare G-quadruplex attivava geni antivirali e infiammatori e portava a una morte cellulare significativa. Questi effetti dipendevano sia dalla regione Zα2 di ZBP1-S sia da un partner a valle localizzato sui mitocondri chiamato MAVS, che trasmette il segnale di morte.
Piccole molecole che possono abbassare l’allarme
Se l’attivazione di ZBP1-S dipende dai G-quadruplex della TERRA, allora molecole che si legano a queste strutture potrebbero bloccare l’interazione. I ricercatori hanno testato diversi composti noti per legarsi ai G-quadruplex. Due di essi, PDS e TMPyP4, hanno efficacemente competuto con ZBP1-S per l’accesso ai G-quadruplex della TERRA sia in esperimenti in provetta sia in cellule viventi. Quando questi composti erano presenti, ZBP1-S non riusciva a raggrupparsi, l’attività dei geni infiammatori diminuiva e meno cellule morivano. Altri farmaci per G-quadruplex si sono rivelati molto meno efficaci, suggerendo che il modo preciso in cui un composto afferra la struttura dell’RNA ripiegato determina se può interferire con la partnership ZBP1–TERRA.
Implicazioni più ampie e possibili sviluppi futuri
Questo lavoro rivela che ZBP1-S non si limita a riconoscere materiale generico di tipo virale; è invece tarato sulla forma tridimensionale dei G-quadruplex nell’RNA telomerico. Agganciandosi a questi ripiegamenti compatti, ZBP1-S si assemblea in grandi agglomerati che segnalano attraverso i mitocondri per eliminare cellule potenzialmente sulla via del cancro. Allo stesso tempo, piccole molecole scelte con cura possono attenuare questa via schermando le strutture a G-quadruplex da ZBP1-S. Per il lettore non specialistico, il messaggio chiave è che la decisione della cellula di vivere o morire può dipendere da sottili torsioni e nodi nel suo materiale genetico — e che queste forme potrebbero un giorno essere bersagliate con farmaci per favorire la rimozione di cellule pericolose o prevenire una morte cellulare infiammatoria dannosa.
Citazione: Qin, G., Zhao, C., Gao, C. et al. Telomeric repeat-containing RNA G-quadruplexes trigger ZBP1-mediated cell death. Nat Commun 17, 3076 (2026). https://doi.org/10.1038/s41467-026-69989-7
Parole chiave: immunità innata, telomeri, RNA a G-quadruplex, morte cellulare programmata, prevenzione del cancro