Clear Sky Science · fr
Les ARN télomériques contenant des répétitions et leurs G-quadruplex déclenchent la mort cellulaire médiée par ZBP1
Comment les cellules décident quand s’autodétruire
Nos cellules possèdent des systèmes d’alerte intégrés capables de détecter qu’un problème grave est survenu, puis de déclencher une forme contrôlée d’autodestruction. Ce processus empêche des cellules endommagées ou précancéreuses d’évoluer en tumeurs et contribue également à lutter contre les infections. L’étude présentée ici révèle une façon surprenante par laquelle un détecteur cellulaire particulier reconnaît des formes inhabituelles de matière génétique aux extrémités des chromosomes et utilise cette information pour décider quand une cellule doit mourir.
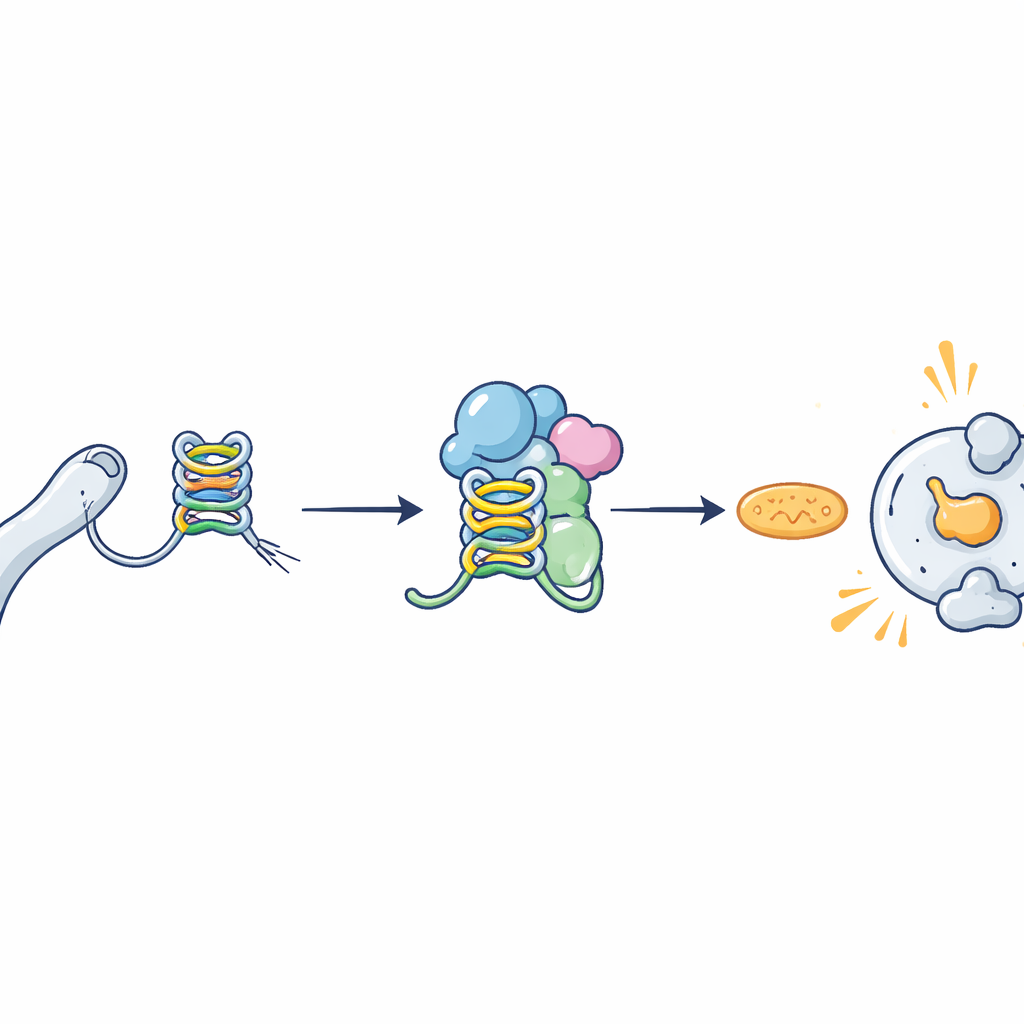
Des formes étranges aux extrémités des chromosomes
Les chromosomes humains se terminent par des coiffes protectrices appelées télomères, constituées de séquences d’ADN répétées. Ces régions sont transcrites en molécules d’ARN connues sous le nom de TERRA. Parce qu’elles sont riches en guanine, les chaînes de TERRA peuvent se replier en formes compactes et empilées appelées G-quadruplex plutôt que de rester de simples brins. Ces replis inhabituels sont de plus en plus reconnus comme des éléments de contrôle importants dans la cellule et ont été associés au cancer, aux troubles cérébraux et aux infections virales. Les chercheurs se sont demandé si ces structures en G-quadruplex de la TERRA pourraient être la pièce manquante expliquant comment une protéine détectrice de mort cellulaire appelée ZBP1 reconnaît des télomères en détresse.
Le détecteur de formes structurelles de la cellule
ZBP1 fait partie du système immunitaire inné, la première ligne de défense de l’organisme contre le danger. Il patrouille dans les cellules à la recherche de matériel génétique anormal et, une fois activé, peut déclencher des réponses inflammatoires et la mort cellulaire programmée. Une version plus courte de cette protéine, ZBP1-S, avait récemment été montrée comme répondant spécifiquement à la TERRA et contribuant à l’élimination des cellules en crise. Toutefois, la caractéristique exacte de la TERRA que ZBP1-S détectait restait inconnue. Grâce à des tests biochimiques et à la modélisation structurelle, les auteurs ont découvert que deux régions de ZBP1, appelées domaines Zα, se lient fermement et directement aux formes G-quadruplex de la TERRA mais pas à des TERRA mutées incapables de se plier en ces structures. ZBP1-S, qui ne porte que l’un de ces domaines (Zα2), reconnaissait néanmoins les G-quadruplex de la TERRA avec une forte affinité, en particulier lorsque plusieurs unités G-quadruplex étaient empilées les unes sur les autres.
Du lien à la décision létale
Reconnaître du matériel dangereux n’est que la première étape ; ZBP1 doit aussi s’assembler en complexes plus grands pour envoyer un signal de mort efficace. L’équipe a montré que lorsque la TERRA normale, capable de former des G-quadruplex, était présente dans les cellules, les molécules de ZBP1-S se regroupaient en longues structures filamenteuses, signe d’activation. La TERRA mutante incapable de former des G-quadruplex n’induisait pas ce regroupement. Dans des lignées cellulaires mammaires et d’autres lignées modifiées pour produire ZBP1-S, la présence de TERRA formant des G-quadruplex a activé des gènes antiviraux et inflammatoires et entraîné une mort cellulaire significative. Ces effets dépendaient à la fois de la région Zα2 de ZBP1-S et d’un partenaire en aval localisé sur les mitochondries, MAVS, qui relaie le signal de mort.
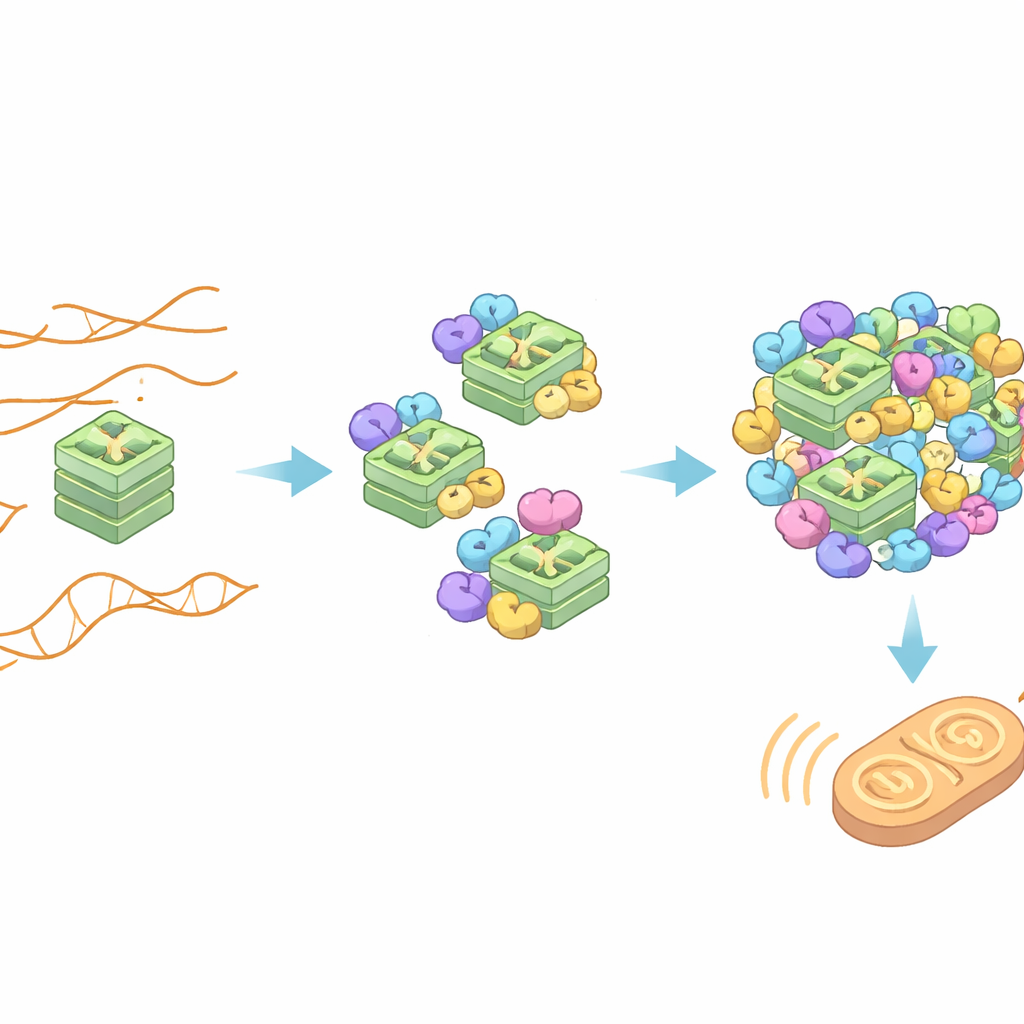
Petites molécules capables d’abaisser l’alarme
Si l’activation de ZBP1-S dépend des G-quadruplex de la TERRA, des composés chimiques qui se fixent sur ces structures pourraient bloquer l’interaction. Les chercheurs ont testé plusieurs composés connus pour se lier aux G-quadruplex. Deux d’entre eux, PDS et TMPyP4, ont efficacement concurrencé ZBP1-S pour l’accès aux G-quadruplex de la TERRA dans des expériences in vitro et dans des cellules vivantes. En présence de ces composés, ZBP1-S n’a pas pu se regrouper, l’activité des gènes inflammatoires a diminué et moins de cellules sont mortes. D’autres médicaments ciblant les G-quadruplex se sont révélés bien moins efficaces, ce qui suggère que la manière précise dont un composé agrippe la forme repliée de l’ARN détermine s’il peut ou non perturber le partenariat ZBP1–TERRA.
Implications plus larges et perspectives
Ce travail révèle que ZBP1-S ne se contente pas de détecter du matériel à caractère viral générique ; il est accordé à la forme tridimensionnelle des G-quadruplex dans l’ARN télomérique. En s’accrochant à ces replis compacts, ZBP1-S s’assemble en grands agrégats qui signalent via les mitochondries pour éliminer des cellules susceptibles d’évoluer vers le cancer. Parallèlement, des petites molécules choisies avec soin peuvent atténuer cette voie en protégeant les structures en G-quadruplex de ZBP1-S. Pour un lecteur non spécialiste, le message principal est que la décision d’une cellule de vivre ou de mourir peut dépendre de torsions et de nœuds subtils dans son matériel génétique — et que ces formes pourraient un jour être ciblées par des médicaments pour favoriser l’élimination de cellules dangereuses ou empêcher une mort cellulaire inflammatoire nuisible.
Citation: Qin, G., Zhao, C., Gao, C. et al. Telomeric repeat-containing RNA G-quadruplexes trigger ZBP1-mediated cell death. Nat Commun 17, 3076 (2026). https://doi.org/10.1038/s41467-026-69989-7
Mots-clés: immunité innée, télomères, ARN en G-quadruplex, mort cellulaire programmée, prévention du cancer