Clear Sky Science · zh
用于糖尿病伤口中线粒体ROS调控的巨噬细胞—线粒体混合细胞外囊泡
为什么难愈合的糖尿病伤口很重要
对许多糖尿病患者而言,脚上的一个小水疱或划伤可能演变为难以愈合的慢性创面,最终出现感染、住院甚至截肢。这些难治溃疡由伤口内免疫细胞中失控的炎症驱动。在这项研究中,科学家们构建了一种高度靶向的“纳米囊泡”——一种微小的、类细胞的囊泡——能够直接潜入这些免疫细胞的能量工厂(线粒体),在不完全抑制其功能的情况下平息有害化学反应,从而在糖尿病小鼠中加速愈合。
当愈合停滞而非前进
正常的伤口愈合按一个有序顺序进行:短暂炎症、组织再生和长期重塑。在糖尿病中,第一阶段常常停滞。巨噬细胞——负责清除碎屑并协调修复的免疫细胞——持续处于攻击性的炎症状态,而无法切换到有利于再生的修复模式。一个主要原因是线粒体产生过量的活性氧(ROS)。过多的反应性氧会损伤线粒体DNA、脂质和蛋白质,破坏细胞稳态,阻止巨噬细胞转向有利于修复的抗炎表型。
会“等到麻烦出现”才起作用的智能抗氧化剂
简单地用抗氧化剂填充伤口并不能解决问题;这既会削弱有害信号,也会抑制有益信号,而且往往无法到达线粒体。研究人员设计了一种天然抗氧化物咖啡酸苯乙酯(caffeic acid phenethyl ester)的“前药”版本。该前药在化学上被锁定为稳定的惰性形式,只有在遇到高水平氧化剂(如受损线粒体内的情况)时才被激活。通过精细的化学修饰,将抗氧化剂与一个反应性键和一段疏油尾连接,使分子在水中保持稳定,同时倾向于嵌入脂质膜。实验表明,该前药在温和条件下保持完整,但在暴露于较高氧化水平时会断裂并释放强效抗氧化剂,近似模拟了受胁迫线粒体内的环境。
瞄准免疫“动力工厂”的微小混合外壳
为了将这种智能货物准确送达所需位置,团队用真实生物膜构建了人工细胞外囊泡。他们提取并纯化了巨噬细胞的外膜和它们线粒体的膜,然后将这些膜融合成混合外壳。由于这些膜携带与原始细胞和细胞器相同的蛋白质,所得到的囊泡能够识别巨噬细胞及其线粒体,就像钥匙与锁配对一样。实验显示,当这些装载药物的混合囊泡接触巨噬细胞时,会通过自然的摄取途径被吞噬,随后与线粒体膜融合。在囊泡内部,高氧化剂环境剪断了前药上的化学锁,精确在过量损伤发生处释放活性抗氧化剂。 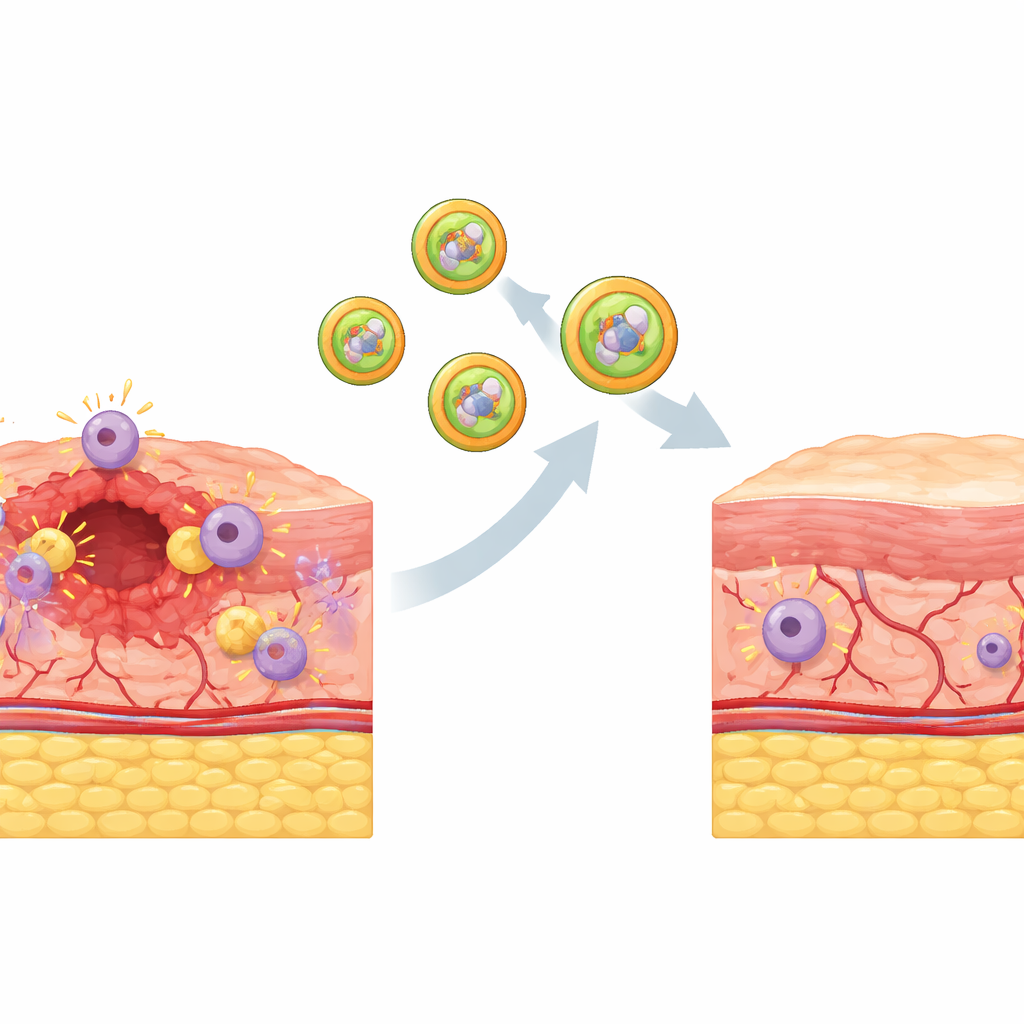
重塑免疫细胞并拯救受损组织
在细胞培养中,这种靶向系统显著降低了有害的线粒体氧化物水平,减少了线粒体内脂质损伤,恢复了其产生能量所需的膜电位,并改善了ATP产生。电子显微镜显示,原本肿胀、形态异常的线粒体在处理后恢复为瘦长且组织良好的结构。这些内部修复对细胞行为产生了重大影响:巨噬细胞从炎症型表型向非炎症、促进修复的状态转变,相关的促炎基因和标志物下调,而与抚慰和组织修复相关的基因上调。 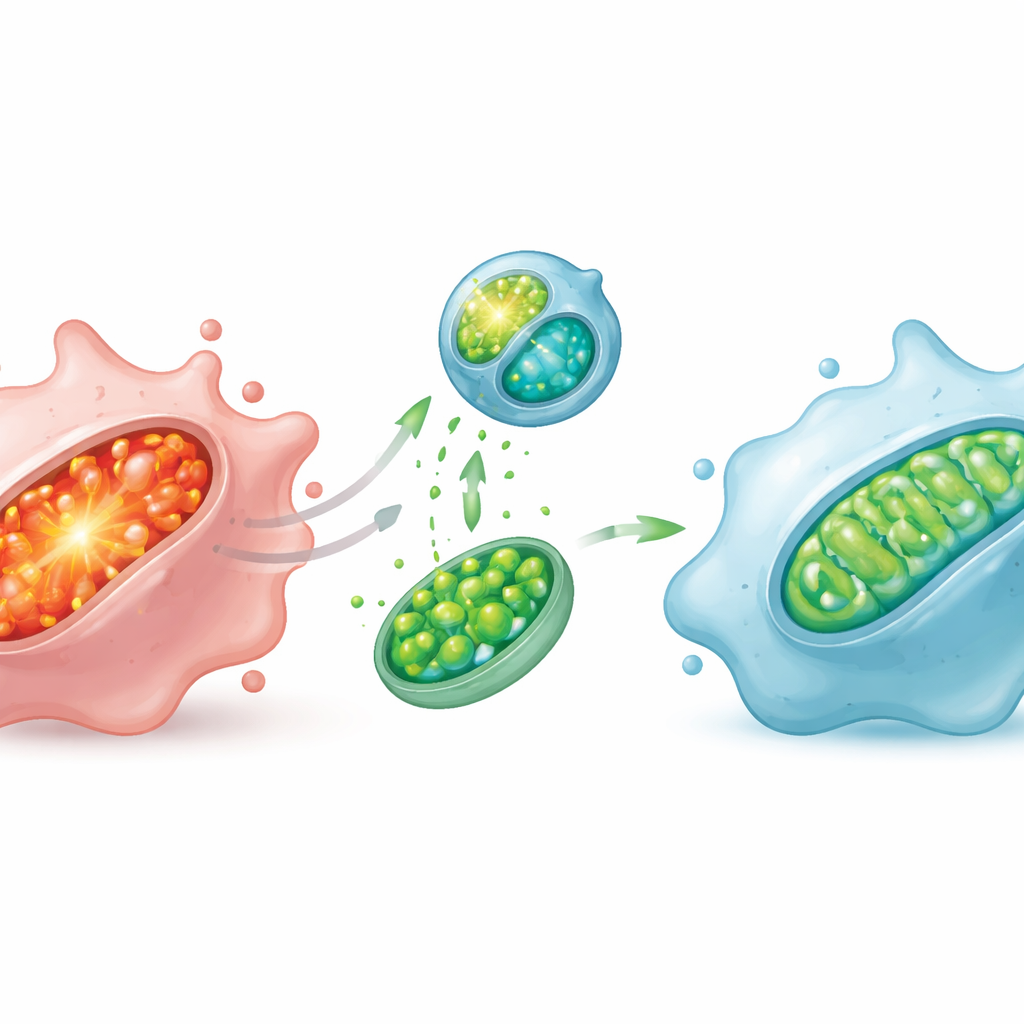
帮助糖尿病动物伤口闭合
当研究人员将混合囊泡注射到糖尿病小鼠全层伤口周围的皮下时,这些颗粒在受损组织中扩散,并主要被巨噬细胞及其线粒体摄取。数天内,线粒体氧化剂水平下降,炎性信号减弱,修复型巨噬细胞数量增加。与几种对照处理(包括游离药物、不含前药的囊泡和其他基于膜的颗粒)相比,混合囊泡导致伤口闭合更快,表皮再生更早,新生血管更多且胶原纤维更致密、排列更好。接受新系统处理的伤口在外观和功能上更接近愈合良好的健康皮肤。
这对未来护理的意义
该研究表明,不仅可以阻断活性氧,还可以通过将生物启发的靶向策略与按需化学反应相结合,在正确的时间和地点对其进行调控。通过定位至巨噬细胞线粒体并仅在高应激条件下释放抗氧化剂,这些混合囊泡恢复了平衡,而不仅仅是压制信号。在糖尿病小鼠中,这种精确控制缓解了慢性炎症并启动了正常修复,指向一类潜在用于糖尿病伤口及其他与线粒体失衡相关的炎性疾病的新疗法。
引用: Fan, L., Zhang, C., Xu, Z. et al. Hybrid macrophage-mitochondria extracellular vesicles for mitochondrial ROS regulation in diabetic wounds. Nat Commun 17, 3285 (2026). https://doi.org/10.1038/s41467-026-69383-3
关键词: 糖尿病伤口愈合, 巨噬细胞线粒体, 纳米囊泡, 氧化应激, 靶向抗氧化剂