Clear Sky Science · it
Vescicole extracellulari ibride macrofagi-mitocondri per la regolazione del ROS mitocondriale nelle ferite diabetiche
Perché le ferite diabetiche ostinate sono importanti
Per molte persone con diabete, una piccola vescica o un graffio sul piede può trasformarsi in una ferita cronica che rifiuta di guarire, talvolta sfociando in infezione, ricovero o persino amputazione. Queste piaghe difficili da trattare sono alimentate da un’infiammazione incontrollata all’interno delle cellule immunitarie presenti nella ferita. In questo studio, i ricercatori hanno costruito una “nanovesicola” altamente mirata — una piccola bolla simile a una cellula — che si infiltra direttamente nelle centrali energetiche di queste cellule immunitarie per calmare la chimica dannosa senza spegnerla completamente, accelerando la guarigione in topi diabetici.
Quando la guarigione si blocca invece di procedere
La guarigione normale di una ferita segue una sequenza ordinata: infiammazione breve, rigenerazione dei tessuti e rimodellamento a lungo termine. Nel diabete, quella prima fase spesso si blocca. I macrofagi — le cellule immunitarie che rimuovono i detriti e coordinano la riparazione — rimangono bloccati in uno stato aggressivo e guidato dall’infiammazione invece di passare a una modalità rigenerativa e di supporto. Un colpevole principale sono le specie reattive dell’ossigeno in eccesso prodotte dai mitocondri, le piccole centrali energetiche dentro le cellule. Un eccesso di questi ossidanti danneggia il DNA mitocondriale, i lipidi e le proteine, destabilizzando la cellula e impedendo ai macrofagi di trasformarsi in uno stato anti‑infiammatorio favorevole alla riparazione.
Un antiossidante intelligente che aspetta il guaio
Semplicemente somministrare inondazioni di antiossidanti nelle ferite non ha risolto il problema; questo approccio può attenuare segnali sia negativi sia positivi e non raggiunge i mitocondri. I ricercatori hanno quindi progettato una versione “pro‑farmaco” di un antiossidante naturale chiamato estere fenetile dell’acido caffeico. Questo pro‑farmaco è chimicamente bloccato in una forma stabile e inattiva che si attiva solo quando incontra livelli elevati di ossidanti, come quelli presenti nei mitocondri danneggiati. Una chimica accurata ha legato l’antiossidante a un legame reattivo e a una coda lipofila, rendendo la molecola stabile in acqua ma incline a inserirsi nelle membrane grasse. I test hanno mostrato che questo pro‑farmaco rimaneva intatto in condizioni miti ma si scindeva e rilasciava potenti antiossidanti quando esposto a livelli più alti di ossidanti, imitando da vicino quanto avviene all’interno dei mitocondri stressati.
Gusci ibridi minuscoli che mirano alle centrali immunitarie
Per consegnare questo carico intelligente esattamente dove serviva, il team ha costruito vescicole extracellulari artificiali a partire da membrane biologiche reali. Hanno isolato e purificato le membrane esterne dei macrofagi e dei loro mitocondri, quindi le hanno fuse in involucri ibridi. Poiché queste membrane portano le stesse proteine delle cellule e degli organelli originari, le vescicole risultanti possono riconoscere i macrofagi e poi i loro mitocondri, come una chiave che si abbina a una serratura. Gli esperimenti hanno mostrato che quando queste vescicole ibride cariche di farmaco entravano in contatto con i macrofagi, venivano internalizzate tramite vie naturali di assorbimento e poi fuse con le membrane mitocondriali. All’interno, l’ambiente ad alta ossidazione rompeva il blocco chimico sul pro‑farmaco, rilasciando l’antiossidante attivo proprio nel punto di origine del danno in eccesso. 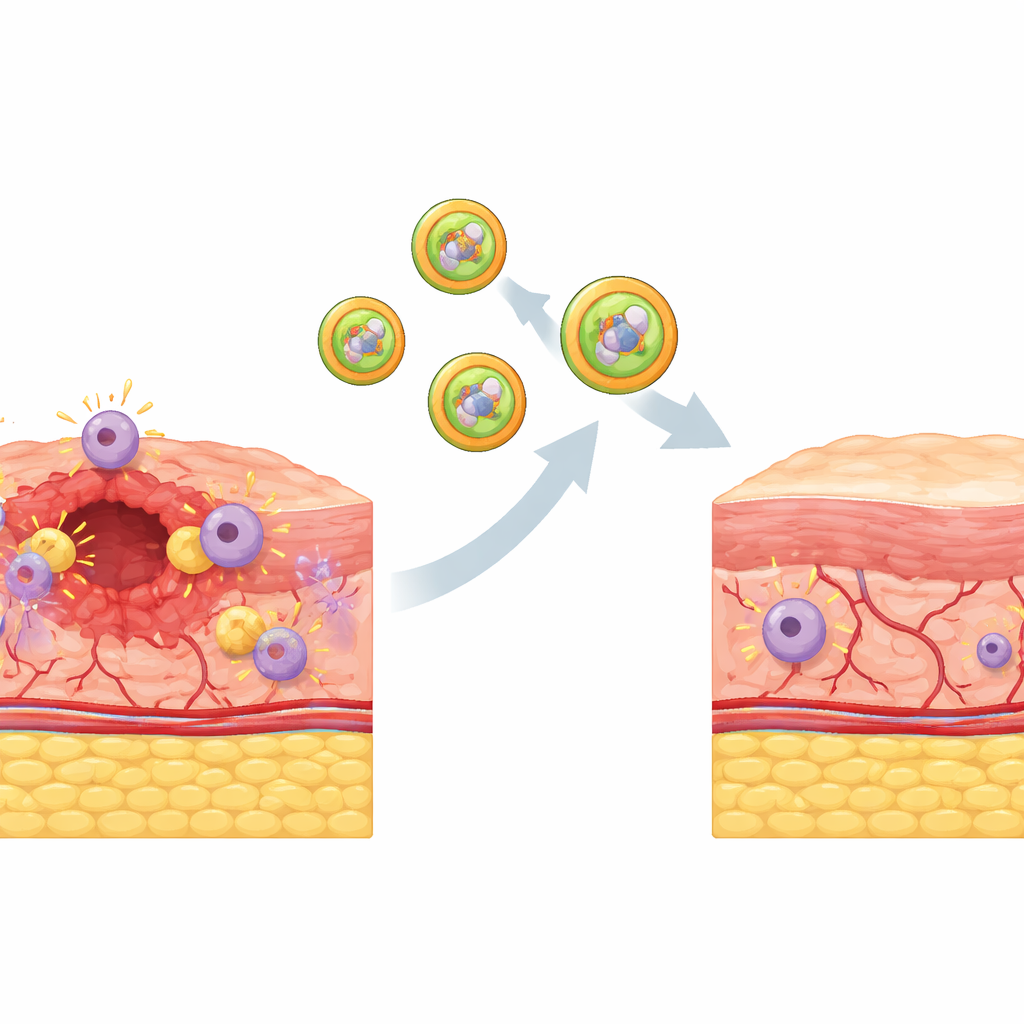
Rimodellare le cellule immunitarie e salvare il tessuto danneggiato
nelle colture cellulari, questo sistema mirato ha ridotto drasticamente gli ossidanti mitocondriali dannosi, limitato il danno lipidico all’interno dei mitocondri, ripristinato il potenziale elettrico necessario per produrre energia e migliorato la produzione di ATP. La microscopia elettronica ha rivelato che mitocondri gonfi e deformi sono tornati a strutture sottili e ben organizzate una volta trattati. Queste riparazioni interne hanno avuto conseguenze importanti sul comportamento cellulare: i macrofagi si sono spostati lontano da un profilo infiammatorio, abbassando l’espressione di geni e marker associati alla modalità aggressiva e aumentando quelli legati a uno stato calmante e di riparazione tissutale. 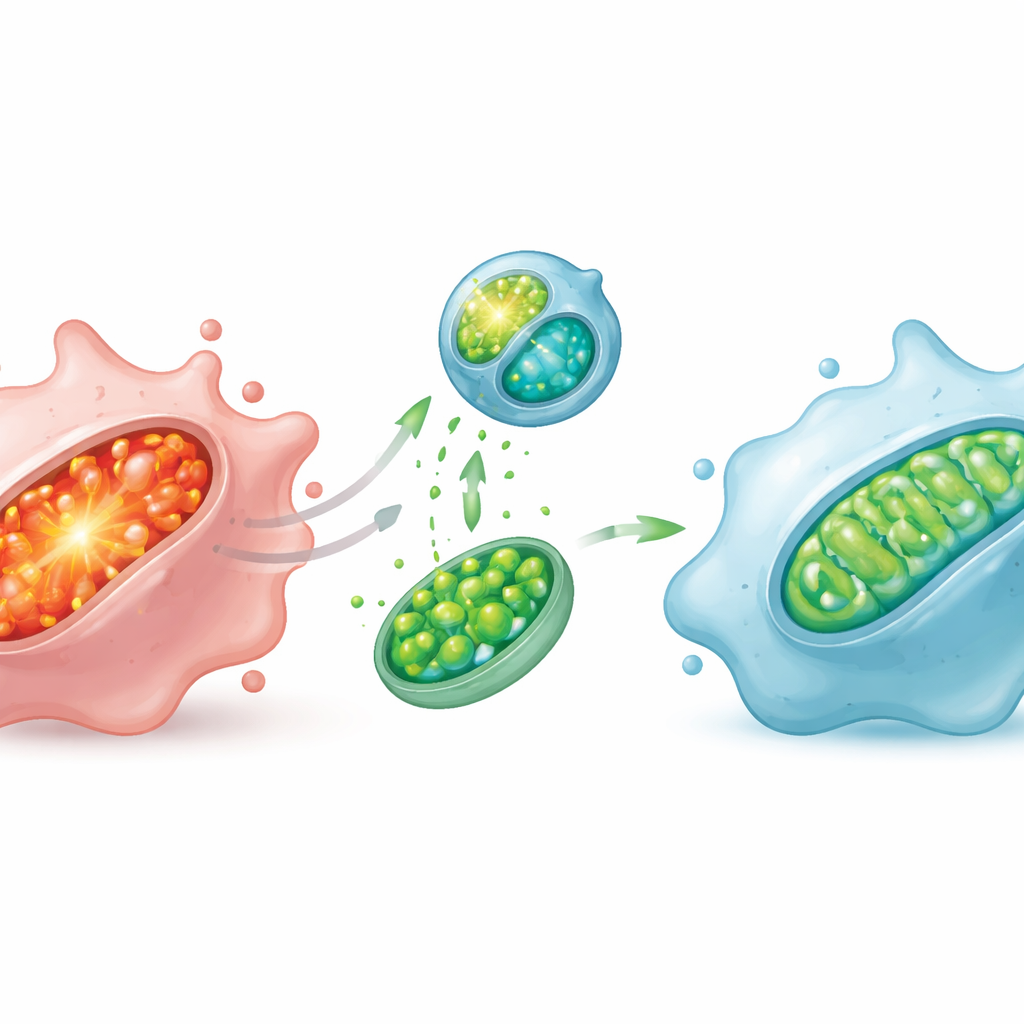
Aiutare le ferite a chiudersi negli animali diabetici
Quando i ricercatori hanno iniettato le vescicole ibride sotto la pelle intorno a ferite a tutto spessore in topi diabetici, le particelle si sono diffuse nel tessuto danneggiato e sono state assorbite principalmente dai macrofagi, compresi i loro mitocondri. Nel corso di alcuni giorni, i livelli di ossidanti mitocondriali sono diminuiti, i segnali infiammatori si sono attenuati e i macrofagi orientati alla riparazione sono diventati più numerosi. Rispetto a vari trattamenti di controllo — incluso il farmaco libero, vescicole senza il pro‑farmaco e altre particelle a base di membrana — le vescicole ibride hanno prodotto una chiusura delle ferite più rapida, una ricrescita più precoce dello strato esterno della pelle, più nuovi vasi sanguigni e fibre di collagene più dense e meglio organizzate. Le ferite trattate con il nuovo sistema apparivano e funzionavano più come pelle sana e guarita.
Cosa potrebbe significare per le cure future
Lo studio dimostra che non è possibile solo bloccare le specie reattive dell’ossigeno, ma anche sintonizzarle nel posto giusto e al momento giusto combinando targeting bio‑ispirato con chimica on‑demand. Mirando ai mitocondri dei macrofagi e rilasciando antiossidanti solo in condizioni di alto stress, queste vescicole ibride ripristinano l’equilibrio invece di sopprimere semplicemente i segnali. Nei topi diabetici, questo controllo preciso attenua l’infiammazione cronica e rilancia la riparazione normale, indicando una possibile nuova classe di trattamenti per le ferite diabetiche e altre malattie infiammatorie legate allo squilibrio mitocondriale.
Citazione: Fan, L., Zhang, C., Xu, Z. et al. Hybrid macrophage-mitochondria extracellular vesicles for mitochondrial ROS regulation in diabetic wounds. Nat Commun 17, 3285 (2026). https://doi.org/10.1038/s41467-026-69383-3
Parole chiave: guarigione delle ferite diabetiche, mitocondri dei macrofagi, nanovesicole, stress ossidativo, antiossidanti mirati