Clear Sky Science · ru
Гибридные внеклеточные везикулы из макрофагов и митохондрий для регулирования митохондриальных ОВР в диабетических ранах
Почему упорные диабетические раны имеют значение
Для многих людей с диабетом небольшая мозоль или царапина на ступне может перерасти в хроническую рану, которая не заживает и иногда заканчивается инфекцией, госпитализацией или даже ампутацией. Эти трудно‑поддающиеся лечению язвы подпитываются неконтролируемым воспалением в иммунных клетках, находящихся в ране. В этом исследовании учёные создали сверхтаргетированную «нановезикулу» — крошечный клеткоподобный пузырёк, который проникает прямо в энергофонды этих иммунных клеток, успокаивая вредную химию, но не отключая её полностью, что ускоряет заживление у диабетических мышей.
Когда заживление застывает вместо того, чтобы продвигаться
Нормальное заживление ран проходит четкой последовательностью: краткое воспаление, регенерация ткани и длительное ремоделирование. При диабете этот первый этап часто застревает. Макрофаги — иммунные клетки, которые очищают от мусора и координируют ремонт — остаются в агрессивном, воспалительном состоянии вместо того, чтобы переключиться на поддерживающий, восстанавливающий режим. Главный виновник — избыточные реактивные формы кислорода, производимые митохондриями, крошечными электростанциями внутри клеток. Чрезмерное количество этих реакционноспособных видов кислорода повреждает митохондриальную ДНК, липиды и белки, дестабилизируя клетку и мешая макрофагам перейти в профиль, благоприятный для восстановления и антивоспалительный.
Умный антиоксидант, который ждёт проблем
Простое насыщение ран антиоксидантами проблему не решило; это может заглушить как вредные, так и полезные сигналы и при этом не достичь митохондрий вообще. Исследователи вместо этого разработали «пролекарственную» версию природного антиоксиданта кавеиновой кислоты фенетилового эфира. Этот пролекарство химически заперто в стабильной неактивной форме и активируется только при столкновении с высоким уровнем окислителей, как внутри повреждённых митохондрий. Тщательная химическая связка присоединила к антиоксиданту реактивную связь и жировой хвост, сделав молекулу устойчивой в воде, но склонной встраиваться в жирные мембраны. Испытания показали, что пролекарство оставалось целым в мягких условиях, но расщеплялось и высвобождало мощные антиоксиданты при воздействии повышенных уровней окислителей, что точно имитировало происходящее внутри напряжённых митохондрий.
Крошечные гибридные оболочки, нацеленные на энергетические станции иммунитета
Чтобы доставить этот умный груз именно туда, где он нужен, команда создала искусственные внеклеточные везикулы из настоящих биологических мембран. Они выделили и очистили наружные мембраны макрофагов и их митохондрий, а затем слили их в гибридные оболочки. Поскольку эти мембраны несут те же белки, что и исходные клетки и органеллы, получившиеся везикулы могут распознавать макрофаги и затем их митохондрии, словно соответствие ключа и замка. Эксперименты показали, что при контакте с макрофагами загруженные лекарством гибридные везикулы захватывались через естественные пути поглощения и затем сливались с митохондриальными мембранами. Внутри среда с высоким содержанием окислителей разрезала химический замок у пролекарства, высвобождая активный антиоксидант точно в том месте, где возникал избыток повреждений. 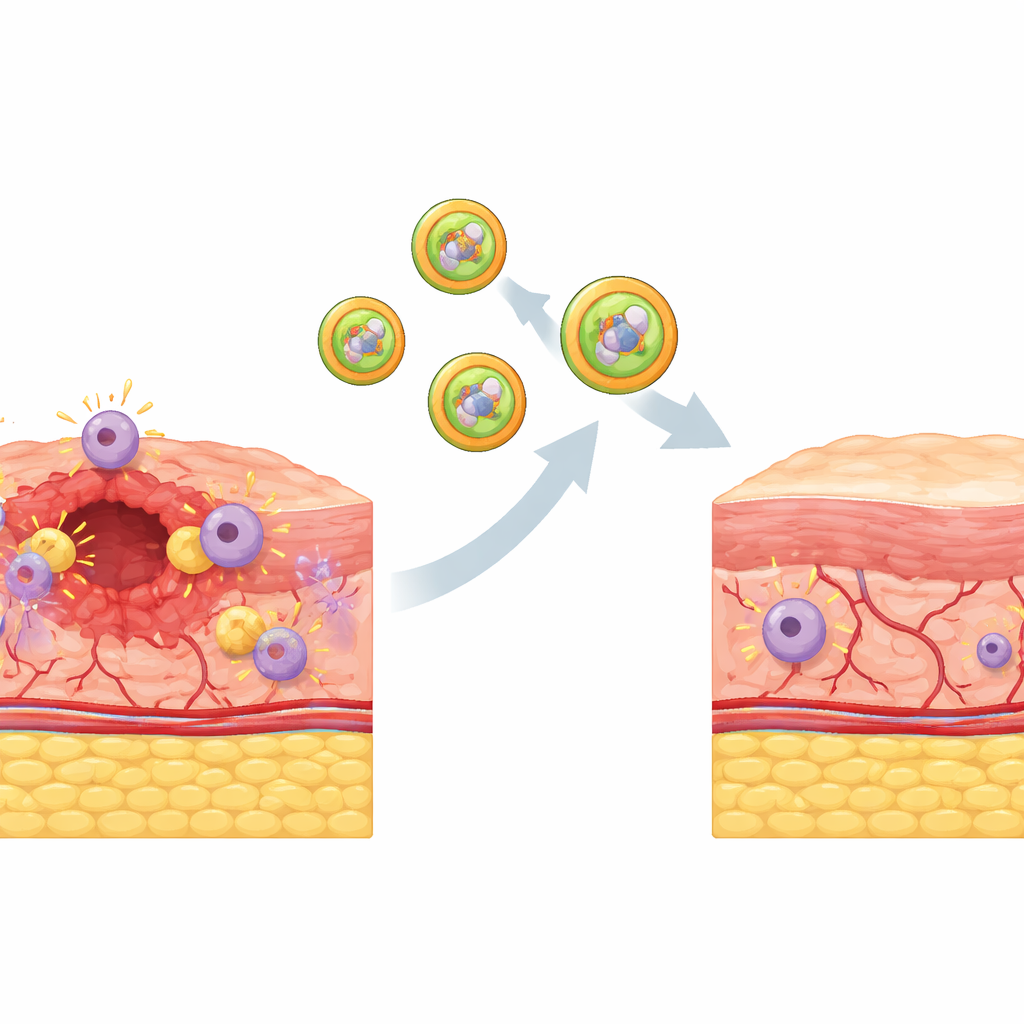
Перепрограммирование иммунных клеток и восстановление повреждённой ткани
В культурах клеток эта таргетированная система резко снизила вредные митохондриальные окислители, ограничила повреждение липидов внутри митохондрий, восстановила электрохимический потенциал, необходимый для выработки энергии, и улучшила синтез АТФ. Электронная микроскопия показала, что распухшие, деформированные митохондрии вернулись к стройным, хорошо организованным структурам после лечения. Эти внутренние починки сильно повлияли на поведение клеток: макрофаги сместились прочь от воспалительного профиля, уменьшив экспрессию генов и маркеров, связанных с атакой, и усилив те, которые связаны с успокаивающим, тканеразвиющим состоянием. 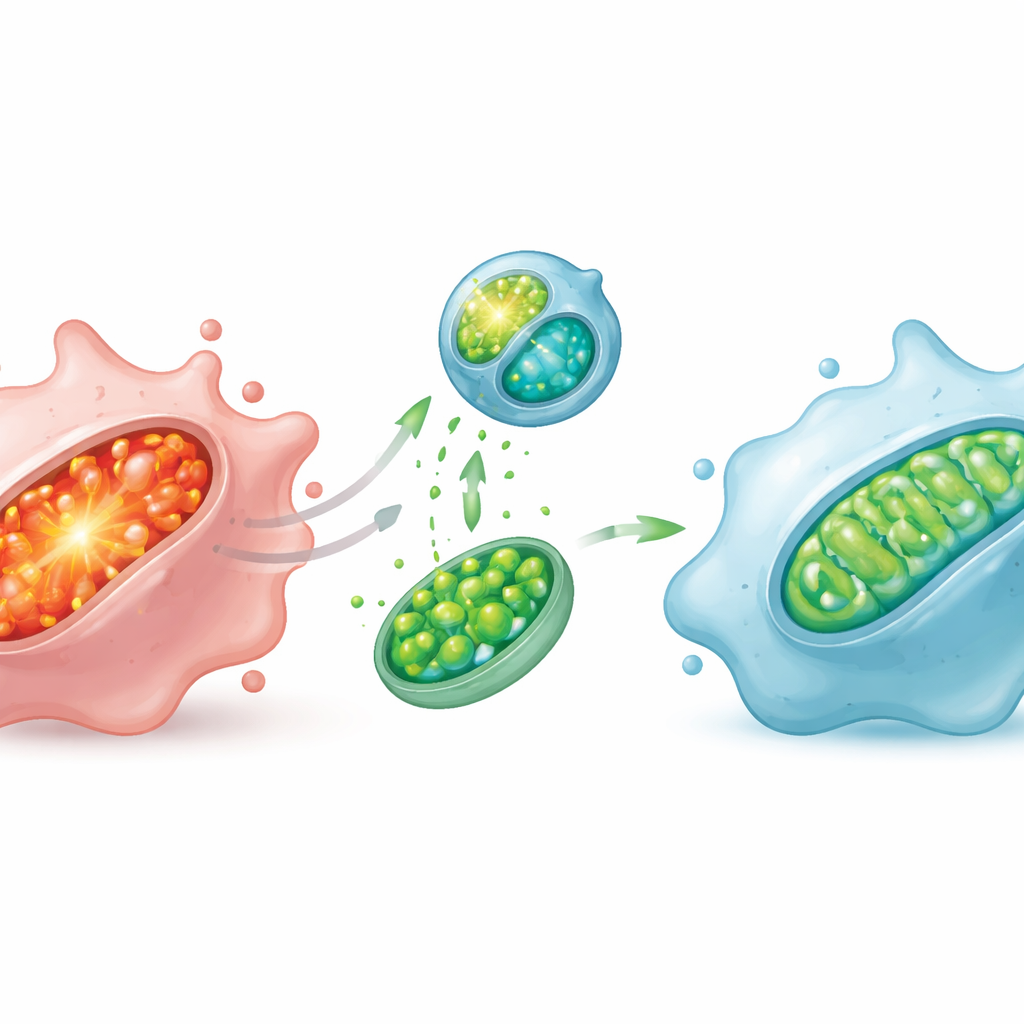
Помощь в закрытии ран у диабетических животных
Когда исследователи вводили гибридные везикулы под кожу вокруг полнослойных ран у диабетических мышей, частицы распространялись по повреждённой ткани и в основном захватывались макрофагами, включая их митохондрии. В течение нескольких дней уровни митохондриальных окислителей снизились, воспалительные сигналы ослабли, и профиль макрофагов сместился в сторону клеток, ориентированных на восстановление. По сравнению с несколькими контрольными вариантами — включая свободный препарат, везикулы без пролекарства и другие частицы на основе мембран — гибридные везикулы обеспечивали более быстрое закрытие ран, более раннюю регенерацию наружного слоя кожи, больше новых кровеносных сосудов и более плотные, лучше организованные коллагеновые волокна. Лечения новыми везикулами сделали раны внешне и функционально более похожими на зажившую здоровую кожу.
Что это может означать для будущей помощи
Исследование показывает, что можно не просто блокировать реактивные формы кислорода, а настраивать их в нужном месте и в нужное время, сочетая бионически вдохновленную нацеленность с химией по требованию. Направляя действие на митохондрии макрофагов и высвобождая антиоксиданты только при условиях высокого стресса, эти гибридные везикулы восстанавливают баланс, а не просто подавляют сигналы. У диабетических мышей такой точный контроль смягчил хроническое воспаление и запустил нормальный ремонт тканей, указывая на новый класс методов лечения диабетических ран и других воспалительных заболеваний, связанных с митохондриальным дисбалансом.
Цитирование: Fan, L., Zhang, C., Xu, Z. et al. Hybrid macrophage-mitochondria extracellular vesicles for mitochondrial ROS regulation in diabetic wounds. Nat Commun 17, 3285 (2026). https://doi.org/10.1038/s41467-026-69383-3
Ключевые слова: заживление диабетических ран, митохондрии макрофагов, нановезикулы, окислительный стресс, таргетные антиоксиданты