Clear Sky Science · ar
الحويصلات خارج الخلوية الهجينة من البلاعم والميتوكندريا لتنظيم ROS الميتوكندري في جروح السكري
لماذا تهم الجروح المزمنة لدى مرضى السكري
بالنسبة لكثير من المصابين بالسكري، يمكن أن يتحول بثرة صغيرة أو خدش في القدم إلى جرح مزمن يرفض الشفاء، وقد ينتهي أحيانًا بعدوى أو دخول المستشفى أو حتى البتر. هذه القروح الصعبة العلاج يغذيها الالتهاب المفرط داخل خلايا المناعة الموجودة في الجرح. في هذه الدراسة، بنى العلماء "نانوحويصلة" مستهدفة للغاية — فقاعة شبيهة بالخلية — تدخل مباشرة مصانع الطاقة داخل خلايا المناعة هذه لتهدئة الكيمياء الضارة دون إيقافها تمامًا، مما يسرع الشفاء في فئران مصابة بالسكري.
عندما يتعثر الشفاء بدلًا من التقدّم
يمر الشفاء الطبيعي للجروح بتسلسل منظم: التهاب قصير، ونمو نسيجي، وإعادة تشكيل طويلة الأجل. في حالة السكري، غالبًا ما يتوقف هذا الطور الأول. تظل البلاعم — خلايا المناعة التي تنظف الحطام وتنسق الإصلاح — عالقة في حالة عدائية مدفوعة بالالتهاب بدلًا من الانتقال إلى وضع إعادة البناء والتغذية. سبب رئيسي هو إنتاج كمية مفرطة من أنواع الأكسجين التفاعلية بواسطة الميتوكندريا، وهي مصانع الطاقة الصغيرة داخل الخلايا. يؤدي فرط هذه الأكسجين التفاعلي إلى إتلاف DNA الميتوكندريا والدهون والبروتينات، مما يزعزع الخلية ويمنع البلاعم من التحول إلى حالة مضادة للالتهاب ومساعدة على الإصلاح.
مضاد أكسدة ذكي ينتظر ظهور المشكلة
التعامل ببساطة عبر إغراق الجروح بمضادات الأكسدة لم يحل المشكلة؛ إذ يمكن أن يضعف كلًا من الإشارات الضارة والمفيدة ويفشل في الوصول إلى الميتوكندريا تمامًا. لذلك صمم الباحثون نسخة "برودواء" من مضاد أكسدة طبيعي يسمى أسيتات فينيل إستر حمض القهوة (caffeic acid phenethyl ester). هذا البرودواء مقفل كيميائيًا في شكل مستقر وغير نشط يصبح نشطًا فقط عند مواجهة مستويات عالية من المؤكسدات، مثل تلك الموجودة داخل الميتوكندريا التالفة. ربطت الكيمياء المتأنية المضاد الأكسدة برابطة تفاعلية وذيل دهني، مما جعل الجزيء مستقرًا في الماء لكنه ميال للاندماج في الأغشية الدهنية. أظهرت الاختبارات أن هذا البرودواء يبقى سليمًا في ظروف معتدلة لكنه يتحلل ويطلق مضادات أكسدة قوية عند التعرض لمستويات مؤكسدة أعلى، مما يحاكي بدقة ما يحدث داخل الميتوكندريا المتوترة.
قشور هجينة صغيرة تتوجه إلى مصانع طاقة المناعة
لتسليم هذه الحمولة الذكية إلى المكان المنشود بالضبط، بنى الفريق حويصلات خارج خلوية اصطناعية من أغشية حيوية حقيقية. استخلصوا ونقّوا الأغشية الخارجية من البلاعم ومن ميتوكندرياتها، ثم دمجوها لتشكيل قشور هجينة. وبما أن هذه الأغشية تحمل نفس البروتينات الموجودة في الخلايا والعضيات الأصلية، يمكن للحويصلات الناتجة التعرف على البلاعم ثم على ميتوكندرياها، تمامًا مثل مفتاح يتطابق مع قفل. أظهرت التجارب أنه عندما تلامست هذه الحويصلات المحمّلة بالدواء مع البلاعم، تم بلعها عبر طرق الامتزاز الطبيعية ثم اندمجت مع أغشية الميتوكندريا. في الداخل، أدى الوسط المؤكسد العالي إلى قطع القفل الكيميائي على البرودواء، وإطلاق المضاد الأكسدة النشط بالضبط حيث نشأ الضرر الزائد. 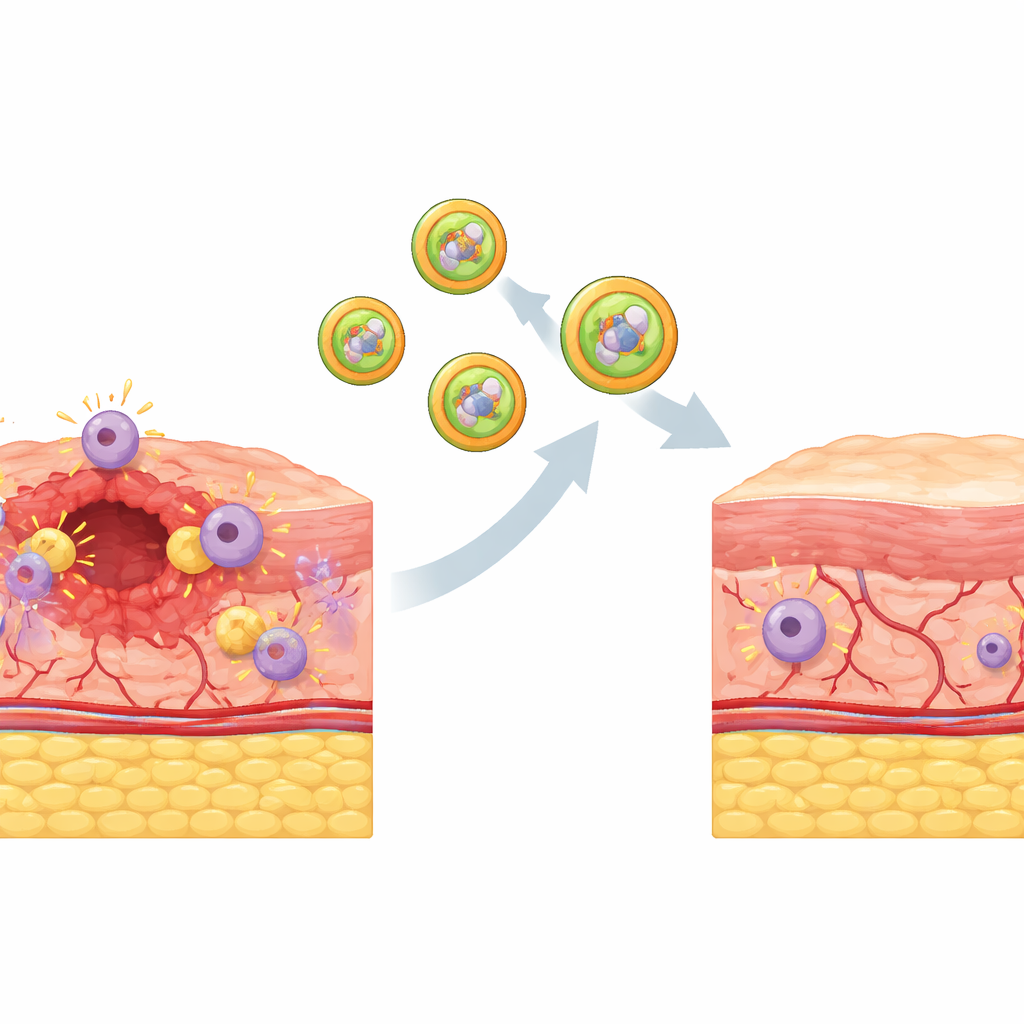
إعادة برمجة خلايا المناعة وإنقاذ النسيج التالف
في مستزرعات الخلايا، قلل هذا النظام المستهدف بشكل حاد من المؤكسدات الميتوكندريّة الضارة، وقيّد تلف الدهون داخل الميتوكندريا، واستعاد الجهد الكهربائي الذي تحتاجه لصنع الطاقة، وحسّن إنتاج ATP. كشفت المجهرية الإلكترونية أن الميتوكندريا المنتفخة والمشوهة عادت لتصبح هياكل نحيلة ومنظمة جيدًا بعد العلاج. كان لهذه الإصلاحات الداخلية آثار كبيرة على سلوك الخلايا: تحولت البلاعم بعيدًا عن الملف الالتهابي، وخفّضت التعبير عن الجينات والسمات المرتبطة بوضع الهجوم وزادت تلك المرتبطة بوضع مهدئ ومساعد على إصلاح النسيج. 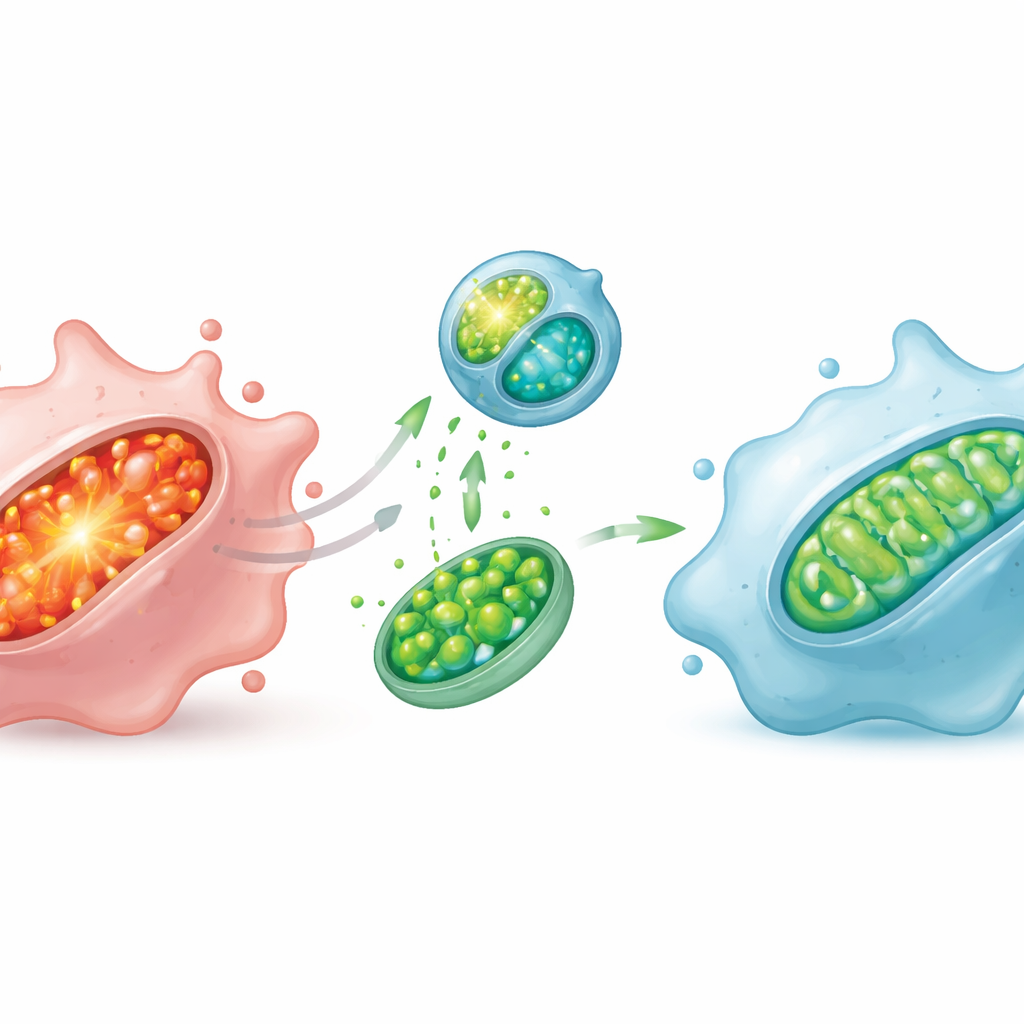
مساعدة الجروح على الانغلاق في الحيوانات المصابة بالسكري
عندما حقن الباحثون الحويصلات الهجينة تحت الجلد حول جروح كاملة السمك في فئران مصابة بالسكري، انتشرت الجسيمات عبر النسيج التالف وتمت بلعها في المقام الأول بواسطة البلاعم، بما في ذلك ميتوكندرياها. على مدى أيام، انخفضت مستويات المؤكسدات الميتوكندريّة، تراجعت الإشارات الالتهابية، وأصبح البلاعم الموجهة نحو الإصلاح أكثر شيوعًا. مقارنة بعدة علاجات ضابطة — بما في ذلك الدواء الحر، والحويصلات دون البرودواء، وجسيمات قائمة على أغشية أخرى — أدت الحويصلات الهجينة إلى إغلاق أسرع للجروح، ونمو مبكر للطبقة الخارجية للجلد، ومزيد من الأوعية الدموية الجديدة، وألياف كولاجين أكثر كثافة وتنظيمًا. بدت الجروح المعالجة بالنظام الجديد وعملت بشكل أقرب إلى الجلد المتعافى والصحي.
ما الذي قد يعنيه هذا للرعاية المستقبلية
تُظهر الدراسة أنه من الممكن ألا تكتفي بحجب أنواع الأكسجين التفاعلية فحسب، بل ضبطها في المكان والزمان المناسبين عبر الجمع بين استهداف مستوحى من الطبيعة وكيمياء مطلوبة عند الطلب. من خلال التركيز على ميتوكندريا البلاعم وإطلاق مضادات الأكسدة فقط في ظل ظروف الإجهاد العالي، تعيد هذه الحويصلات الهجينة التوازن بدلًا من قمع الإشارات فحسب. في فئران السكري، يخفف هذا التحكم الدقيق من الالتهاب المزمن ويعيد بدء الإصلاح الطبيعي، مما يشير إلى فئة جديدة من العلاجات لجروح السكري وأمراض التهابية أخرى مرتبطة بخلل في الميتوكندريا.
الاستشهاد: Fan, L., Zhang, C., Xu, Z. et al. Hybrid macrophage-mitochondria extracellular vesicles for mitochondrial ROS regulation in diabetic wounds. Nat Commun 17, 3285 (2026). https://doi.org/10.1038/s41467-026-69383-3
الكلمات المفتاحية: التئام جروح السكري, ميتوكندريا البلاعم, نانوحويصلات, الإجهاد التأكسدي, مضادات الأكسدة المستهدفة