Clear Sky Science · zh
NEO-STIM 推进个体化新抗原特异性输注性 T 细胞治疗
将免疫系统变成定制的抗癌药物
肿瘤常通过伪装成正常组织来逃避免疫防御。该研究描述了一种方法,将患者自身的免疫细胞转变为一种定制的活体药物,能够靶向该患者肿瘤中的独特突变。对于关注癌症治疗进展的读者而言,这显示出研究者如何从一刀切的疗法迈向高度定制的细胞治疗,并且所需样本来自简单的抽血而非手术切除。
为何针对肿瘤“错字”很重要
每种癌症都携带可能改变肿瘤细胞内蛋白的基因“错字”。这些改变蛋白的片段称为新抗原,能在细胞表面出现并将肿瘤标识为外来物。它们是理想的靶点,因为通常仅出现在肿瘤中而在健康组织中缺失,这意味着针对新抗原的免疫细胞理论上应能避免损伤正常器官。现有的肿瘤浸润淋巴细胞(TIL)疗法通过扩增自然渗入肿瘤的 T 细胞,已经让部分患者获益。但 TIL 疗法需要从手术获得较大肿瘤样本,仅覆盖所有潜在新抗原靶点的一小部分,而且常倚赖那些已在肿瘤恶劣微环境中被耗竭的 T 细胞。
从抽血到个体化 T 细胞制剂
为克服这些障碍,作者开发了 NEO-STIM,一种分步的体外方法,能够完全从外周血构建个体化的 T 细胞治疗产品。他们不以肿瘤组织为起点,而是从静脉采集的白细胞(白细胞分离术,一种“免疫细胞收集”)开始。首先去除已知会抑制免疫反应的细胞类型,然后利用循环中的树突状细胞——免疫系统中高效的侦察细胞——向 T 细胞呈递精心设计的新抗原肽。在受控的生长信号组合下,这些相遇能启动从未接触过肿瘤的“初始”T 细胞并扩增那些已对肿瘤有记忆的罕见细胞。两轮交错刺激约四周后,可产生数十亿对新抗原有反应的 T 细胞,随后冷冻保存作为药物制剂。
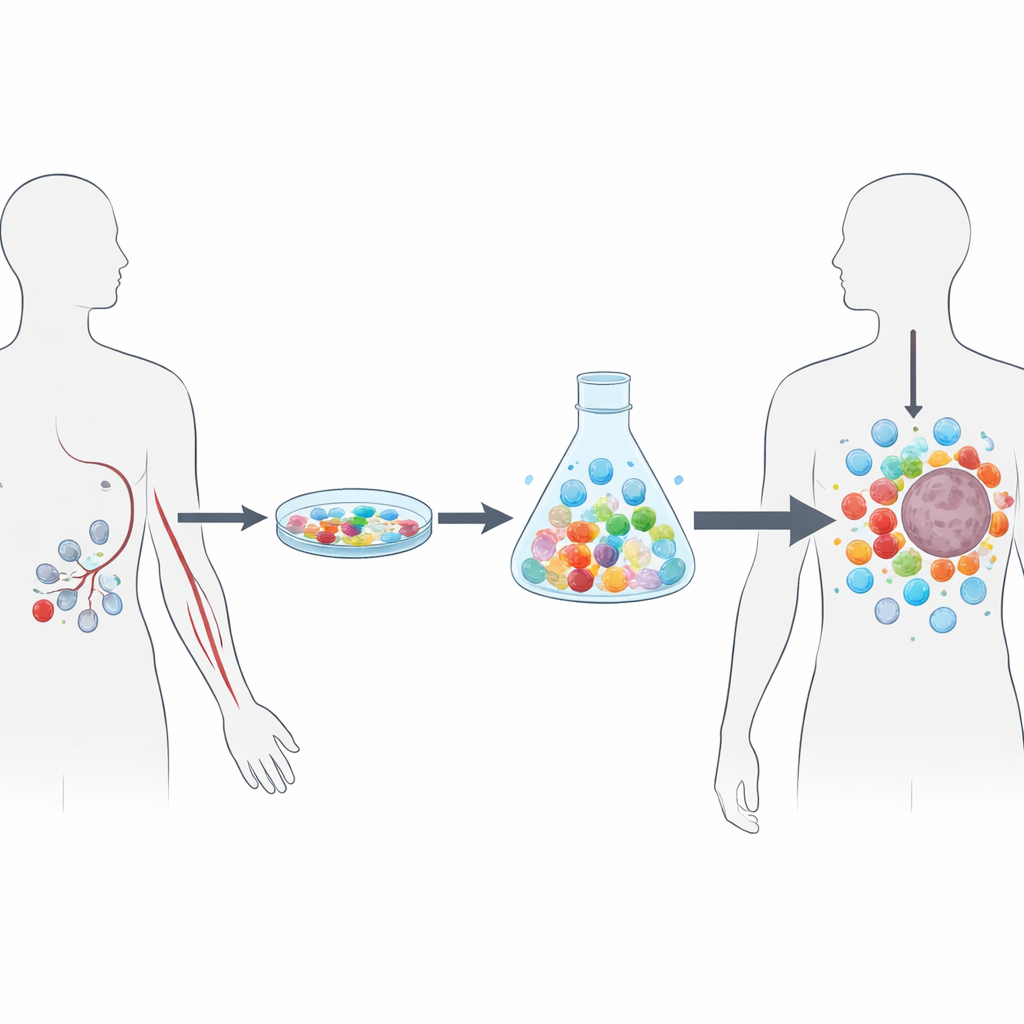
构建多样且功能性的 T 细胞军队
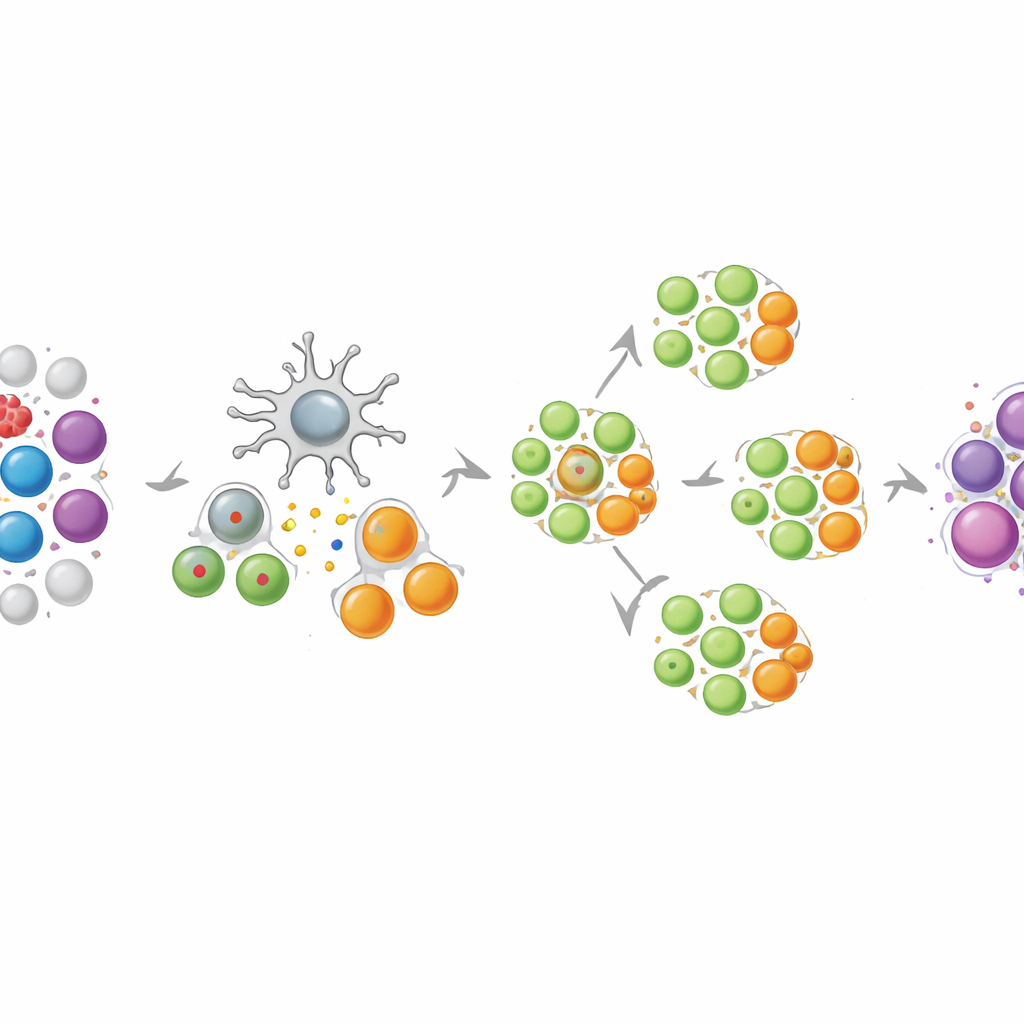
在来自健康志愿者及黑色素瘤或卵巢癌患者的血样中,团队展示了 NEO-STIM 能稳定产生广泛的 T 细胞反应混合物。最终制剂包含多种 CD8 T 细胞(可直接杀伤癌细胞)和 CD4 T 细胞(协调并维持免疫反应)。许多反应为“新生”的,意味着在培养前无法检测到,因而是在体外新激发的。当研究者用用于训练的相同新抗原片段刺激这些细胞时,观察到强烈的“多功能”行为:单个细胞常同时释放多种防御分子并显示出主动攻击的标志。重要的是,大多数反应对靶点的突变形式高度选择性,明显偏好突变而忽视或远不及对正常形式的反应,从而降低对健康组织的附带损伤风险。
将细胞放到肿瘤面前考验
实验不仅限于识别孤立肽段。研究者改造了肿瘤细胞系,使其自然加工并展示相同的新抗原,然后与 NEO-STIM 衍生的 T 细胞共培养。在大多数情况下,T 细胞不仅发生脱颗粒——表明释放毒性分子——还触发了肿瘤细胞内的早期死亡信号,显示出真实的杀伤活性。对于部分患者,团队还获得了其实际肿瘤中的活细胞。NEO-STIM 产生的新抗原特异性 T 细胞能够识别并对这些自体肿瘤材料作出反应,即便未外加额外肽段,表明它们能感知与体内相当的生理水平靶点。
在患者体内追踪这些细胞
该方法已进入晚期黑色素瘤患者的一项首例人体临床试验。通过测序 T 细胞受体——每个克隆独特的分子“身份证”——研究者在输注后将实验室中诱导出的单个新抗原特异性系谱追踪到血液和肿瘤中。新诱导和既有的克隆在数周后均可检测到。在肿瘤内部,这些细胞带有激活、细胞毒性和部分耗竭的特征谱系,符合它们正在积极与癌细胞接触的状态。在早期临床观察中,大多数患者达到了疾病稳定,多名患者出现了可测量的肿瘤缩小,这支持了该策略的潜力,后续更大规模研究仍在进行中。
这对未来癌症护理意味着什么
通俗地说,NEO-STIM 是一种将一管血转化为识别每位患者独特肿瘤突变的个体化抗癌细胞军队的制造处方。该流程可重复地产出大量活跃、聚焦于突变的 T 细胞,这些细胞能够识别并攻击肿瘤物质,早期临床经验表明该方法可行且耐受良好。尽管关于这些细胞在体内持久性如何以及如何与其他治疗最佳联合等问题仍待解决,这项工作勾勒出了一条从肿瘤基因分析到定制细胞疗法的可扩展路径,使癌症治疗更接近高度个体化、以突变为导向的免疫疗法。
引用: Lenkala, D., Kohler, J., McCarthy, B. et al. NEO-STIM advances personalized neoantigen-specific adoptive T cell therapy. Nat Commun 17, 3683 (2026). https://doi.org/10.1038/s41467-026-68680-1
关键词: 癌症免疫治疗, 新抗原 T 细胞, 个体化医学, 输注性细胞治疗, 黑色素瘤