Clear Sky Science · de
NEO-STIM fördert personalisierte, neoantigenspezifische adoptive T‑Zelltherapie
Das Immunsystem in ein maßgeschneidertes Krebsmedikament verwandeln
Krebs entzieht sich oft unseren Abwehrkräften, indem er sich als normales Gewebe tarnt. Diese Studie beschreibt einen Weg, die eigenen Immunzellen eines Patienten in ein maßgefertigtes lebendes Medikament zu verwandeln, das gezielt die einzigartigen Mutationen des Tumors erkennt. Für Leser, die den Fortschritt in der Krebstherapie verfolgen, zeigt sie, wie Forscher von Einheitslösungen zu hochgradig zugeschnittenen Zelltherapien übergehen, die aus einer einfachen Blutentnahme statt aus einer Operation entstehen.
Warum das Anvisieren von Tumor‑„Tippfehlern“ wichtig ist
Jeder Krebs trägt genetische „Tippfehler“, die Proteine in Tumorzellen verändern können. Fragmente dieser veränderten Proteine, sogenannte Neoantigene, können an der Zelloberfläche erscheinen und den Tumor als fremd markieren. Sie sind attraktive Ziele, weil sie dem Tumor eigen sind und in gesundem Gewebe meist fehlen — das bedeutet, dass Immunzellen, die auf Neoantigene abzielen, prinzipiell gesunde Organe schonen sollten. Bestehende Therapien mit tumorinfiltrierenden Lymphozyten (TIL) helfen bereits einigen Patienten, indem T‑Zellen vermehrt werden, die natürlicherweise in Tumoren vorkommen. Aber TIL‑Therapien verlangen eine erhebliche Tumorprobe aus der Chirurgie, erfassen nur einen kleinen Bruchteil möglicher Neoantigen‑Ziele und beruhen oft auf T‑Zellen, die durch das feindliche Tumorumfeld bereits erschöpft sind.
Von der Blutentnahme zum personalisierten T‑Zellpräparat
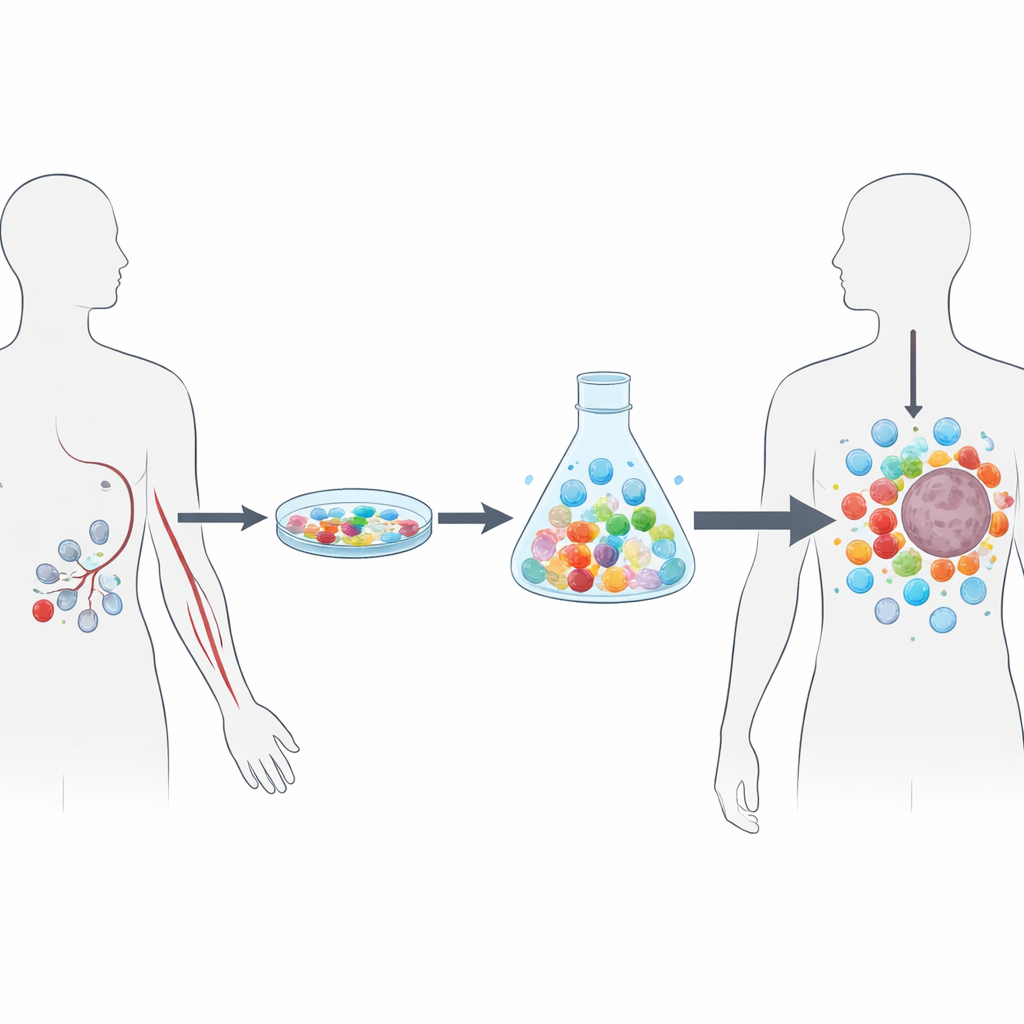
Um diese Hürden zu überwinden, entwickelten die Autoren NEO‑STIM, ein schrittweises Laborverfahren, das eine personalisierte T‑Zellbehandlung vollständig aus peripherem Blut erzeugt. Anstatt mit Tumorgewebe zu beginnen, starten sie mit weißen Blutkörperchen, die per Leukapherese — einer Art „Immunzellernte“ aus einer Vene — gewonnen werden. Zuerst entfernen sie Zelltypen, die bekanntermaßen Immunreaktionen dämpfen, und nutzen dann natürlich zirkulierende dendritische Zellen — hocheffiziente Wächter des Immunsystems — um sorgfältig gestaltete Neoantigen‑Peptide den T‑Zellen zu präsentieren. Unter einer kontrollierten Mischung von Wachstums‑ und Differenzierungssignalen primen diese Begegnungen naïve T‑Zellen, die den Tumor noch nie gesehen haben, und verstärken seltene Gedächtniszellen, die bereits auf den Krebs abgestimmt sind. Zwei gestaffelte Stimulationsrunden über etwa vier Wochen führen zu Milliarden neoantigenreaktiver T‑Zellen, die als Arzneimittelprodukt eingefroren werden können.
Eine vielfältige, funktionsfähige T‑Zellarmee aufbauen
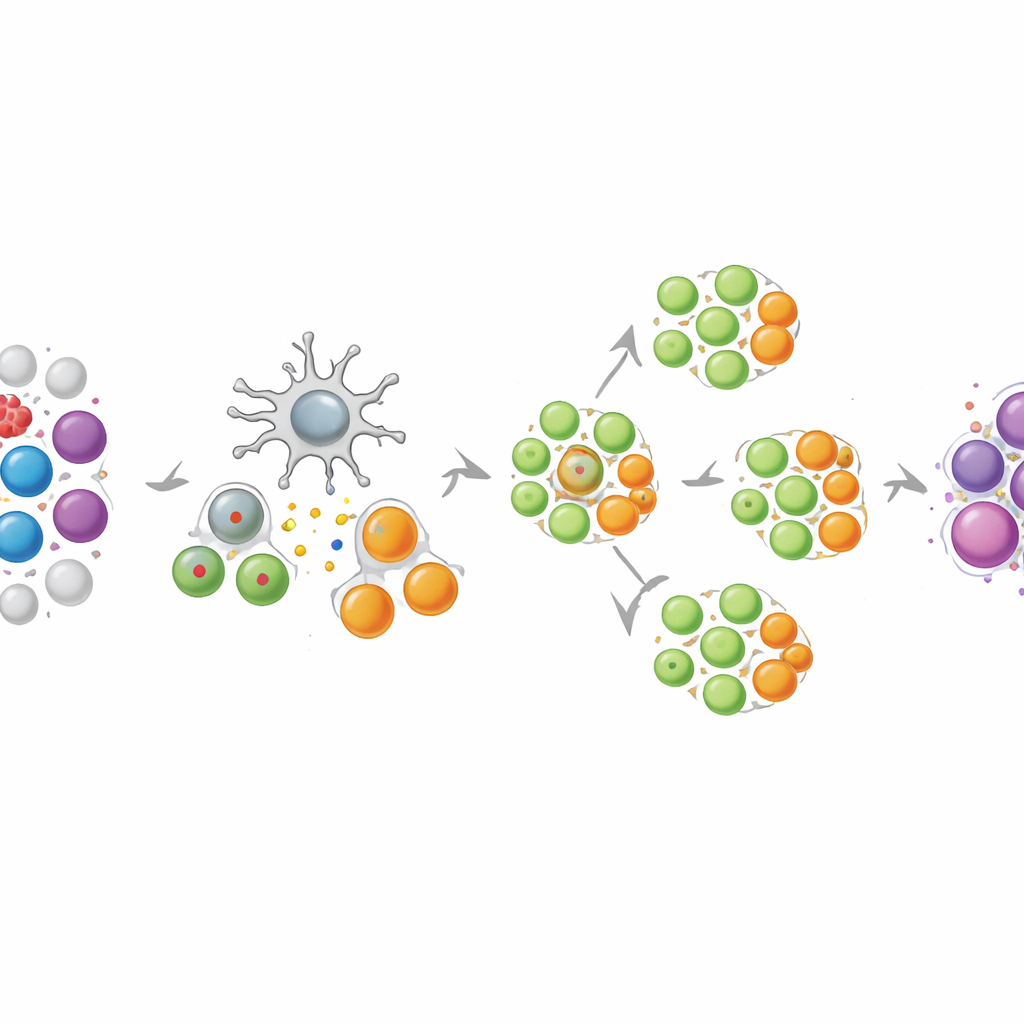
Anhand von Blutproben gesunder Freiwilliger sowie von Patienten mit Melanom oder Ovarialkarzinom zeigte das Team, dass NEO‑STIM konsistent ein breites Spektrum an T‑Zellantworten erzeugt. Die Endprodukte enthielten mehrere CD8‑T‑Zellen, die Tumorzellen direkt abtöten können, und CD4‑T‑Zellen, die Immunangriffe koordinieren und aufrechterhalten. Viele dieser Reaktionen waren „de novo“, also vor der Kultur nicht nachweisbar und erst im Reagenzglas entstanden. Wenn die Forschenden diese Zellen mit genau den Neoantigenfragmenten testeten, die zur Schulung verwendet wurden, zeigten sie starke „polyfunktionale“ Eigenschaften: Einzelzellen setzten oft mehrere Abwehrmoleküle gleichzeitig frei und zeigten Marker aktiver Angriffsfunktion. Wichtig war, dass die meisten Antworten hochselektiv für die mutierte Form jedes Ziels waren und die normale Version ignorierten oder deutlich zugunsten der Mutante bewerteten, wodurch das Risiko von Kollateralschäden am gesunden Gewebe verringert wird.
Die Zellen im Kampf gegen Tumore prüfen
Die Labortests gingen über die Erkennung isolierter Fragmente hinaus. Die Wissenschaftler konstruierten Tumorzelllinien so, dass sie die gleichen Neoantigene natürlich verarbeiten und präsentieren, und kultivierten sie gemeinsam mit NEO‑STIM‑abgeleiteten T‑Zellen. In den meisten Fällen degranulierten die T‑Zellen nicht nur — ein Zeichen der Freisetzung toxischer Moleküle —, sondern lösten auch frühe Todessignale in den Tumorzellen aus, was auf echte Abtötungsaktivität hindeutet. Für eine Untergruppe von Patienten gewann das Team lebensfähige Zellen aus ihren tatsächlichen Tumoren. Neoantigenspezifische T‑Zellen, die durch NEO‑STIM erzeugt wurden, erkannten und reagierten auf dieses autologe Tumormaterial, selbst ohne zusätzliche Peptide, was zeigt, dass sie physiologische Zielmengen so wahrnehmen können wie im Körper.
Die Zellen im Patienten verfolgen
Der Ansatz ist bereits in eine First‑in‑Human‑Studie bei Menschen mit fortgeschrittenem Melanom eingetreten. Durch das Sequenzieren der T‑Zell‑Rezeptoren — der einzigartigen molekularen „ID‑Tags“ jedes Klons — verfolgten die Forschenden einzelne neoantigenspezifische Linien vom Reagenzglas in die Blutbahn und die Tumoren nach der Infusion. Sowohl neu induzierte als auch vorbestehende Klone waren noch Wochen später nachweisbar. Innerhalb der Tumoren trugen diese Zellen Signaturen von Aktivierung, Zytotoxizität und partieller Erschöpfung, was auf eine aktive Auseinandersetzung mit Krebszellen hindeutet. Klinisch zeigten in der frühen Studie die meisten Patienten eine Krankheitsstabilisierung, und mehrere wiesen messbare Tumorschrumpfungen auf, was das Potenzial dieser Strategie stützt, während größere Studien folgen.
Was das für die künftige Krebsversorgung bedeutet
Anschaulich ist NEO‑STIM eine Herstellungsanleitung, um aus einer Blutprobe eine personalisierte Armee von krebsjagenden Zellen zu machen, die die einzigartigen Tumormutationen jedes Patienten erkennen. Der Prozess erzeugt zuverlässig große Mengen aktiver, mutationsfokussierter T‑Zellen, die Tumormaterial erkennen und angreifen können, und erste klinische Erfahrungen deuten darauf hin, dass er durchführbar und verträglich ist. Zwar bleiben Fragen dazu, wie lange diese Zellen persistieren und wie man sie am besten mit anderen Therapien kombiniert, doch diese Arbeit skizziert einen skalierbaren Weg von der genetischen Analyse eines Tumors zu einer maßgeschneiderten Zelltherapie und rückt die Krebsbehandlung näher an eine hochgradig individualisierte, mutationsgerichtete Immuntherapie.
Zitation: Lenkala, D., Kohler, J., McCarthy, B. et al. NEO-STIM advances personalized neoantigen-specific adoptive T cell therapy. Nat Commun 17, 3683 (2026). https://doi.org/10.1038/s41467-026-68680-1
Schlüsselwörter: Krebsimmuntherapie, Neoantigen‑T‑Zellen, Personalisierte Medizin, adoptive Zelltherapie, Melanom