Clear Sky Science · ja
NEO-STIMは個別化されたネオアンチゲン特異的採取T細胞療法を前進させる
免疫系を患者専用のがん薬に変える
がんはしばしば正常組織に擬態して免疫の監視をすり抜けます。本研究は、患者自身の免疫細胞を個別に設計された生きた薬剤に変え、その人の腫瘍に特有の変異を標的にする方法を示しています。がん治療の進展を追う読者にとって、これは一律の治療法を超えて、手術ではなく簡単な採血から作製される高度に個別化された細胞療法へ研究が向かっていることを示します。
腫瘍の「タイプミス」を狙う意義
すべてのがんはタンパク質を変える遺伝的な「タイプミス」を抱えています。これら変化したタンパク質の断片、ネオアンチゲンは細胞表面に現れて腫瘍を異物として示すことがあります。ネオアンチゲンは腫瘍固有で健常組織にほとんど存在しないため魅力的な標的です。つまり、ネオアンチゲンを狙う免疫細胞は原則として正常な臓器を避けられるはずです。既存の腫瘍浸潤リンパ球(TIL)療法は、腫瘍に自然に浸潤するT細胞を増幅して一部の患者に利益をもたらしますが、TIL療法は手術で得た大きな腫瘍サンプルを必要とし、利用可能なすべてのネオアンチゲン標的のごく一部しか捉えられず、しかも腫瘍内という過酷な環境で既に消耗したT細胞に依存することが多いという課題があります。
採血から個別化T細胞製品へ
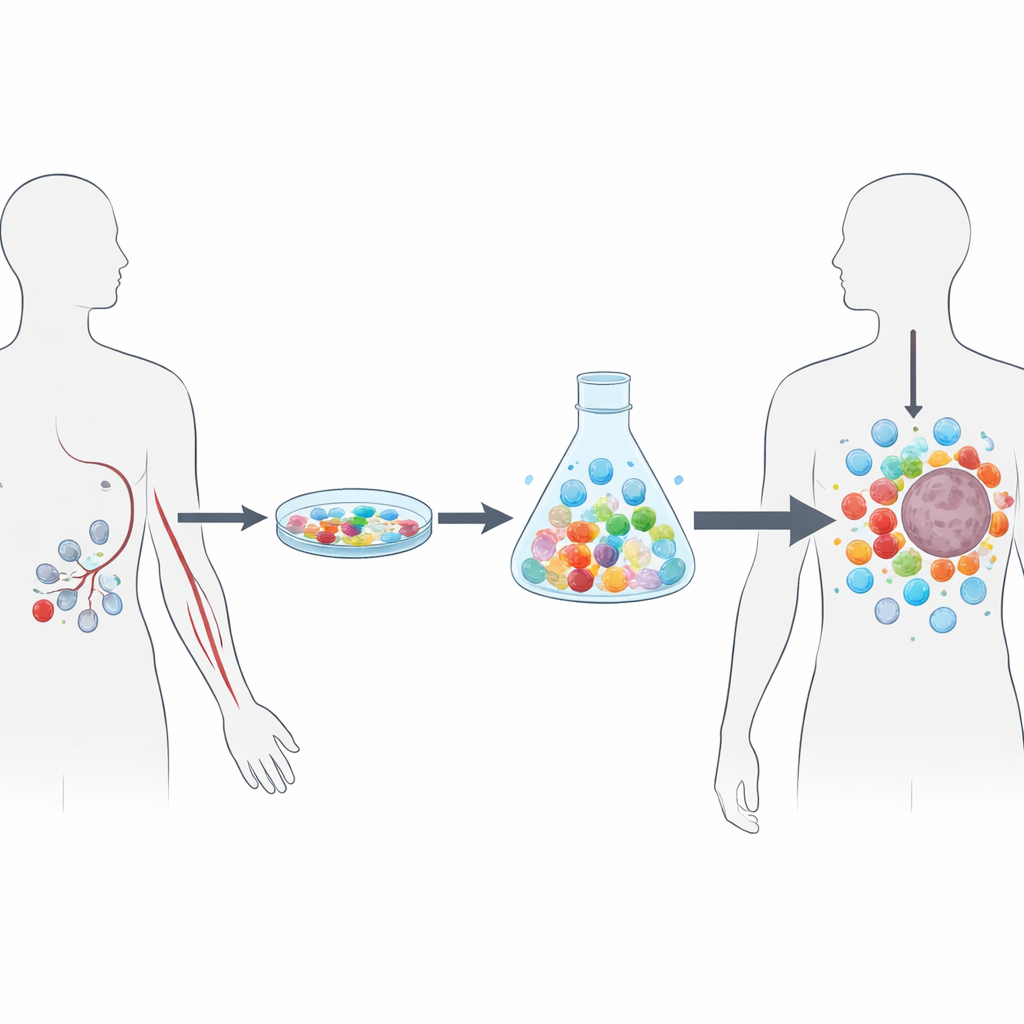
これらの障壁を克服するために、著者らはNEO-STIMという段階的なラボ手法を開発し、末梢血のみから個別化T細胞治療を構築します。腫瘍組織から始める代わりに、静脈からの白血球採取(白血球除去療法とも言える「免疫細胞の収穫」)で得た血液を出発点とします。まず免疫応答を抑えることで知られる細胞種を除去し、次に自然に循環する樹状細胞――免疫系の高効率なセンサー――に精巧に設計したネオアンチゲンペプチドを提示させます。制御された増殖シグナルの混合条件下で、これらの遭遇が腫瘍を一度も見たことのない“ナイーブ”なT細胞を初回活性化するとともに、既にがんに合わせて調整された稀なメモリー細胞を増幅します。約4週間のうちに2回の段階的刺激を行うことで、薬剤として凍結保存できる数十億規模のネオアンチゲン反応性T細胞が得られます。
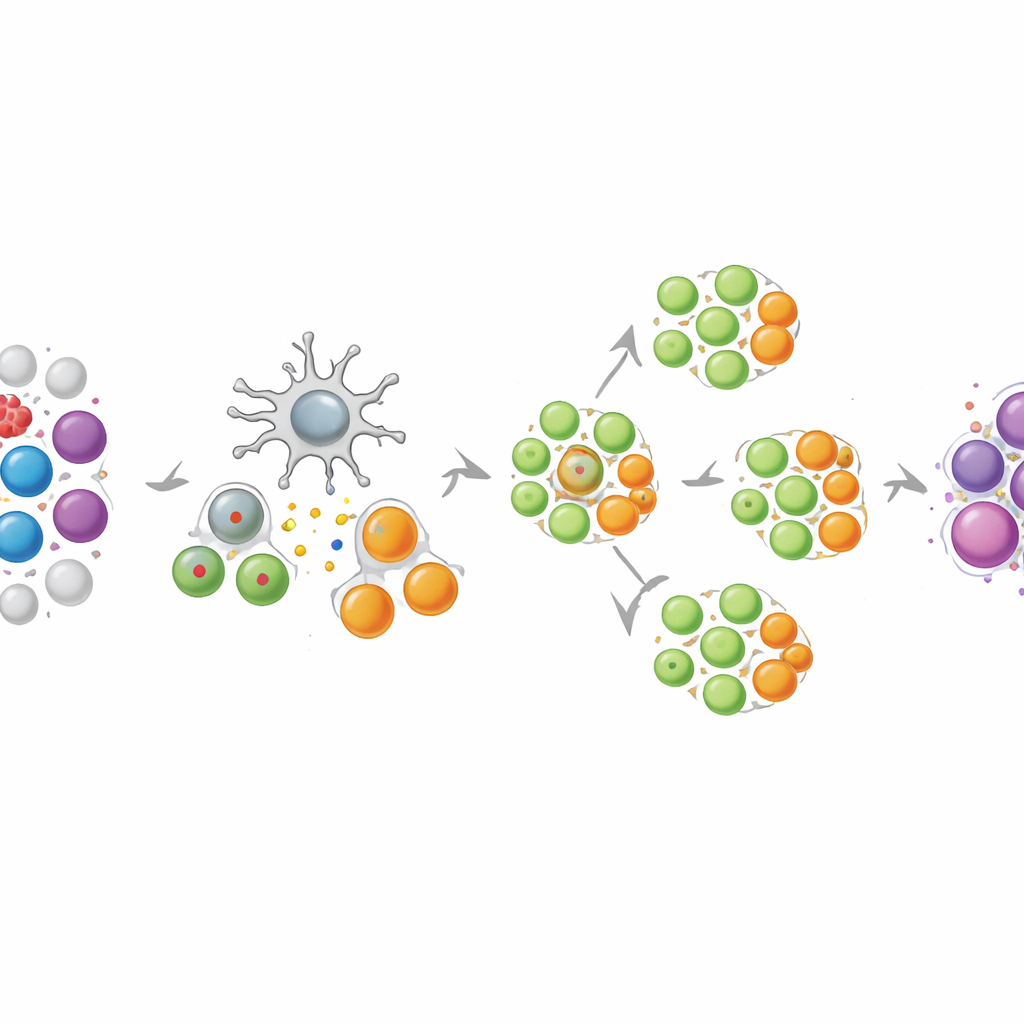
多様で機能的なT細胞の軍団を作る
健常ボランティアと黒色腫や卵巣がん患者からの血液を用い、NEO-STIMが一貫して広範なT細胞応答の混合を生み出すことを示しました。最終製品には、がん細胞を直接殺せるCD8 T細胞や、免疫攻撃を調整・維持するCD4 T細胞が複数含まれていました。多くの応答は“de novo”で、培養前には検出されず、培養で新たに誘導されたものでした。研究者が訓練に使ったネオアンチゲン断片でこれらの細胞を刺激すると、単一細胞が複数の防御分子を同時に放出し活性攻撃のマーカーを示すなど強い“多機能”な挙動が観察されました。重要な点として、多くの応答は各ターゲットの変異型に対して高い選択性を持ち、正常型を無視するか変異型を強く好むため、健常組織への副作用リスクが低く抑えられます。
腫瘍に対する細胞の効力を検証する
ラボでの試験は単なる断片の認識にとどまりません。研究者らは同じネオアンチゲンを自然に処理・提示するように改変した腫瘍細胞株を作製し、それらをNEO-STIM由来のT細胞と共培養しました。多くの場合、T細胞は顆粒を放出する(毒性分子を分泌する兆候)だけでなく、腫瘍細胞内で早期の死のシグナルを誘導し、実際の殺傷活性を示しました。患者の一部からは実際の腫瘍組織由来の生細胞も取得しており、NEO-STIMで作られたネオアンチゲン特異的T細胞は外部から追加ペプチドを加えなくてもその同種腫瘍材料を認識・反応しました。これはこれらの細胞が体内での生理的な標的水準を感知できることを示しています。
患者内でのT細胞の追跡
このアプローチは既に進行した黒色腫患者を対象とした初回のヒト試験に入っています。クローンごとの独自の分子的“IDタグ”であるT細胞受容体を配列決定することで、研究者らは培養皿から静脈注入後の血中および腫瘍内へと移行した個々のネオアンチゲン特異的系統を追跡しました。新たに誘導されたクローンも既存のクローンも数週間後に検出されました。腫瘍内では、これらの細胞は活性化、細胞傷害性、部分的な疲弊の署名を示しており、がん細胞への能動的な関与と一致します。臨床的には、初期試験で多くの患者が病勢安定を達成し、複数例で明確な腫瘍縮小が確認され、この戦略の可能性を支持しています。より大規模な研究が進行中です。
将来のがん医療への意味
日常語で言えば、NEO-STIMは1本の血液を患者固有の腫瘍変異を認識する“がん狩りの軍隊”に変える製造レシピです。このプロセスは大量の活性化された変異特異的T細胞を安定的に生産し、腫瘍材料を認識・攻撃できることを示し、初期の臨床経験は実行可能で許容されうることを示唆しています。これらの細胞がどれくらい長く持続するか、また他の治療とどう組み合わせるのが最適かといった課題は残りますが、本研究は腫瘍の遺伝子解析から個別の細胞療法を作るスケーラブルな道筋を示し、変異指向の高度に個別化された免疫療法にがん医療を近づけます。
引用: Lenkala, D., Kohler, J., McCarthy, B. et al. NEO-STIM advances personalized neoantigen-specific adoptive T cell therapy. Nat Commun 17, 3683 (2026). https://doi.org/10.1038/s41467-026-68680-1
キーワード: がん免疫療法, ネオアンチゲンT細胞, 個別化医療, 採取細胞療法, 黒色腫