Clear Sky Science · zh
锌蓄积诱导的整合应激反应触发β细胞身份丧失
这项研究为何对糖尿病患者重要
2型糖尿病常被描述为机体“耗尽”了胰岛素产生细胞,但许多这些细胞并非单纯死亡——它们改变了自身的身份。本研究揭示了导致这种身份危机的一个意外元凶:胰腺产胰岛素细胞内过量的锌。通过追踪人类与小鼠细胞以及干细胞衍生迷你胰岛中的变化,作者描绘了锌超载如何使这些细胞承受压力并被推动转变为错误的细胞类型,以及这一过程如何可能被减缓甚至逆转。
当胰岛素细胞忘记了自己的职责
在健康人中,胰腺岛包含不同的激素分泌细胞,按微妙平衡排列,产胰岛素的β细胞占主导地位。在2型糖尿病中,临床观察到β细胞减少而产生升高血糖激素的α细胞增多。研究团队深入分析了来自人类胰腺的大型单细胞数据集,发现从典型β细胞向类α细胞的平滑“轨迹”,其中包括携带两者特征的混合细胞。来自有无糖尿病人群的组织样本以及糖尿病小鼠模型证实,在高血糖条件下,更多β细胞失去其原有身份并开始在形态和功能上表现得像α细胞,而不是简单消失。
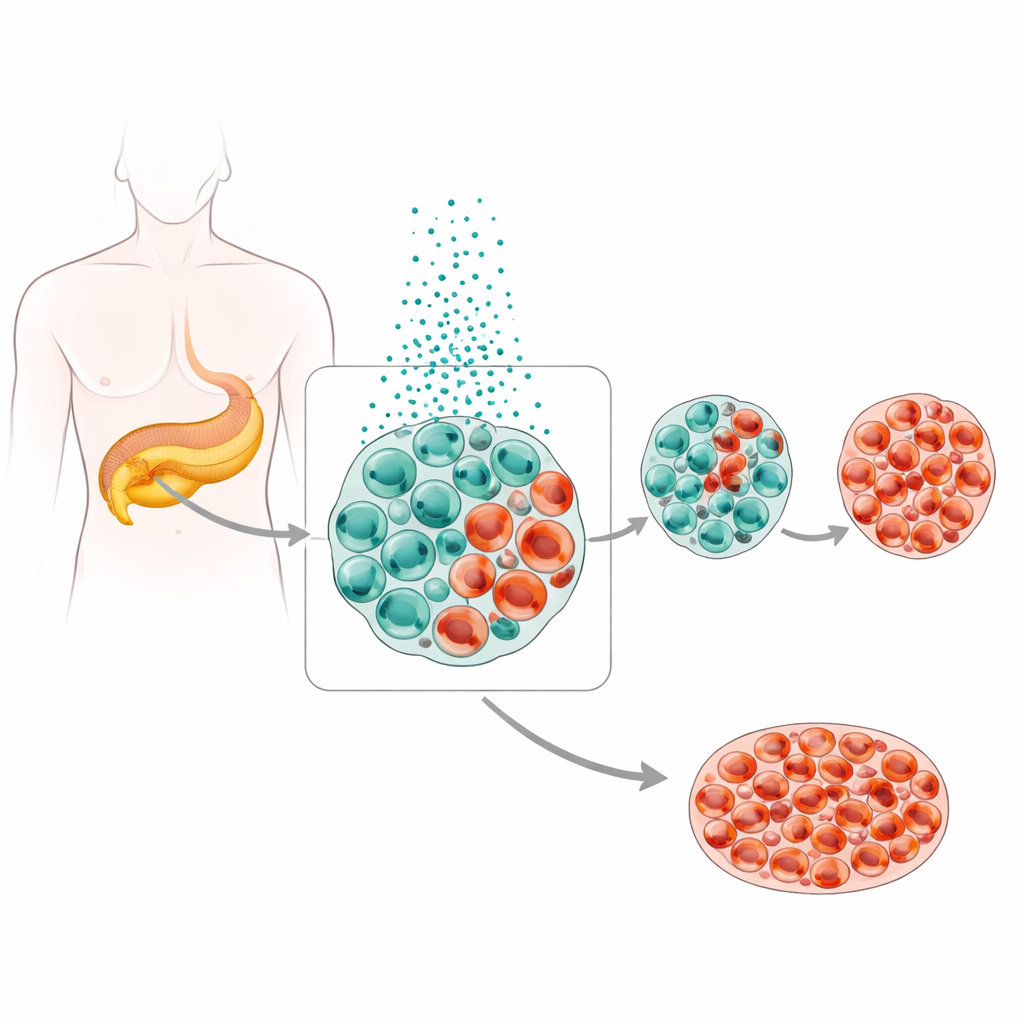
一枚双面金属
锌对β细胞至关重要,因为它有助于将胰岛素包装以便储存与释放。但这些细胞本就携带远高于大多数其他组织的锌水平,研究显示进一步推高锌含量会变得危险。一个特定的转运蛋白ZnT8通常将锌转运到胰岛素颗粒中。在来自2型糖尿病患者的胰岛和糖尿病小鼠中,ZnT8水平明显升高,细胞内锌含量测量显示出清晰的蓄积。当研究者强制使人类胰岛表达更多ZnT8,或在培养中加入额外锌或含锌化合物时,β细胞数量减少,而α细胞和混合胰岛素–胰高血糖素细胞增多,这在体外培养和活体小鼠中均可观察到。相反,通过基因手段降低ZnT8则能使锌水平维持较低并更好地保留β细胞身份。
细胞内的应激:分子拐点
为理解过量锌如何改变细胞命运,团队转向干细胞衍生的胰岛,这是一个可精细操控的人类模型。在长期高葡萄糖条件下,这些实验室培养的β细胞逐渐累计锌并开始向类α特征转变。单细胞基因谱分析显示,随着锌升高,β细胞开启了一套称为整合应激反应的细胞警报系统。该通路降低总体蛋白合成,但强烈上调一个名为ATF4的因子。研究者表明,ATF4可以直接结合α细胞主控基因ARX的调控区并促其激活。当增加ATF4或锌时,ARX在β细胞中出现,细胞向α型身份转换;而当用小分子抑制剂阻断该应激通路时,这种转换在很大程度上被阻止。
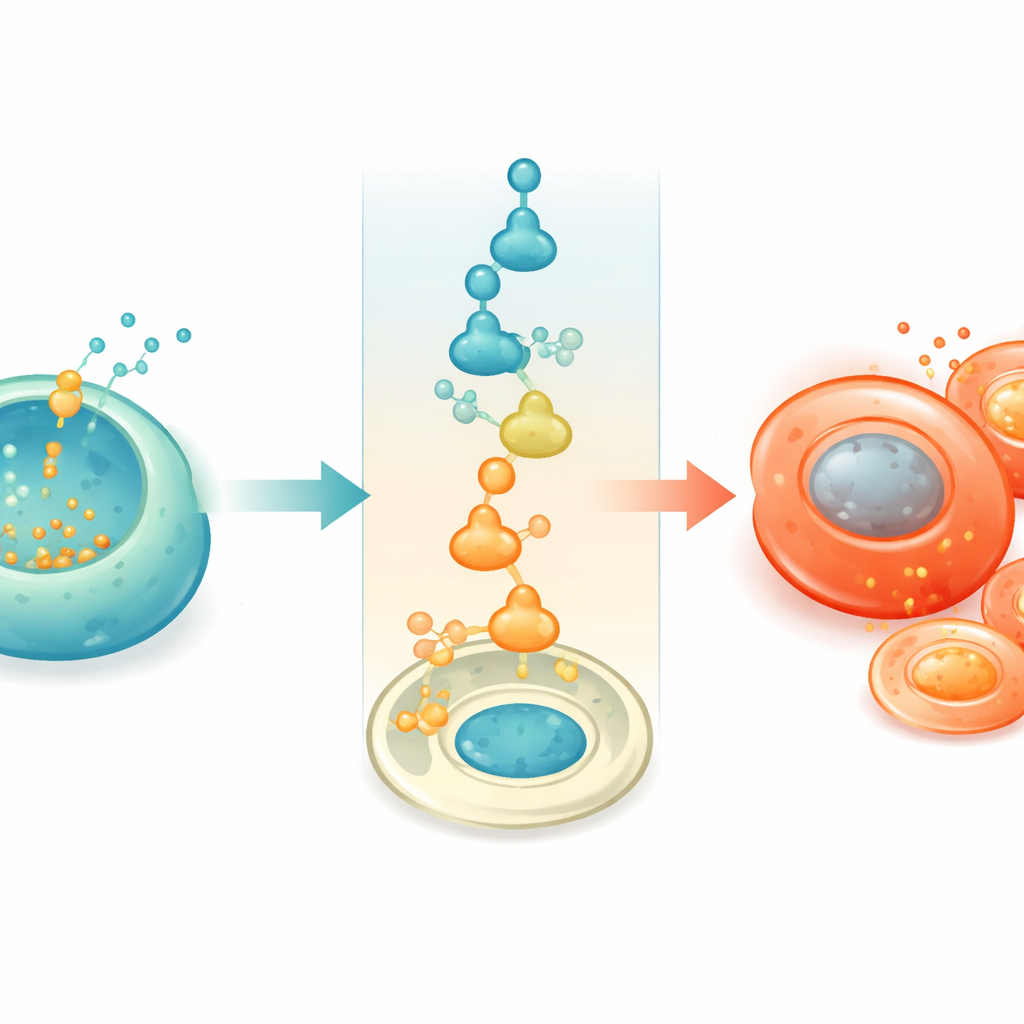
在糖尿病体内保护替代细胞
当人类胰岛或纯干细胞衍生的β细胞移植到糖尿病小鼠体内时,也出现了同样的锌驱动身份丧失。在高糖环境中,移植的β细胞蓄积锌、丧失其标志性特征并产生更多类胰高血糖素细胞,从而削弱了血糖控制。干预锌—应激轴能改变这一结局。给予小鼠应激反应抑制剂可保留更多β样细胞并改善胰岛素分泌和糖耐量。同样,使用缺乏ZnT8的工程化β细胞,或用低剂量药物anisomycin选择性降低ZnT8及锌蓄积,也有助于维持β细胞身份并使移植细胞更有效地降低血糖,在所研究的动物中未见明显毒性。
这对未来糖尿病治疗意味着什么
这项工作描绘出一幅清晰图景:在2型糖尿病中,慢性高血糖促使β细胞囤积锌,进而触发细胞内应激系统,启动α细胞的基因程序。许多β细胞并非死亡,而是本质上被重新编程为错误的激素分泌类型,从而破坏了机体对葡萄糖的控制。通过针对锌的处理或下游的应激反应,或许可以让β细胞继续“按剧本”运作,无论是在患者自身的胰腺中,还是在用于治疗的移植或干细胞衍生细胞中。尽管在这些策略进入临床之前仍需大量工作,但该研究为保护产胰岛素细胞提供了具体的分子路线图。
引用: Ma, Q., Xu, W., Wang, X. et al. Zinc accumulation-induced integrated stress response triggers β-cell identity loss. Cell Res 36, 359–376 (2026). https://doi.org/10.1038/s41422-026-01222-y
关键词: 2型糖尿病, β细胞身份, 锌蓄积, 胰腺岛, 干细胞来源的胰岛