Clear Sky Science · de
Zinkakkumulation-induzierte integrierte Stressantwort löst den Identitätsverlust von β‑Zellen aus
Warum diese Forschung für Menschen mit Diabetes wichtig ist
Typ‑2‑Diabetes wird oft so erklärt, dass dem Körper die insulinproduzierenden Zellen „ausgehen“, aber viele dieser Zellen sterben nicht einfach — sie verändern ihre Identität. Diese Studie enthüllt einen überraschenden Übeltäter in dieser Identitätskrise: zu viel Zink in den insulinproduzierenden Zellen der Bauchspeicheldrüse. Anhand von Untersuchungen an menschlichen und Maus‑Zellen sowie an aus Stammzellen gezüchteten Mini‑Inseln zeichnen die Autoren nach, wie Zinküberladung diese Zellen belastet, sie in falsche Zelltypen drängt und wie dieser Prozess verlangsamt oder sogar umgekehrt werden könnte.
Wenn Insulinzellen ihren Job vergessen
Bei gesunden Menschen enthalten die Pankreasinseln verschiedenartige Hormon produzierende Zellen in einem feinen Gleichgewicht, wobei die insulinproduzierenden Beta‑Zellen die Hauptrolle spielen. Bei Typ‑2‑Diabetes haben Ärztinnen und Ärzte weniger Beta‑Zellen und mehr Alpha‑Zellen beobachtet, die Glukagon produzieren — ein Hormon, das den Blutzucker erhöht. Das Team untersuchte umfangreiche Einzelzell‑Datensätze aus menschlichen Pankreasproben und fand eine fließende „Trajectory“ von typischen Beta‑Zellen hin zu alpha‑ähnlichen Zellen, einschließlich hybrider Zellen mit Merkmalen beider Typen. Gewebeproben von Menschen mit und ohne Diabetes sowie diabetische Mausmodelle bestätigten, dass bei hohem Blutzucker mehr Beta‑Zellen ihre ursprüngliche Identität verlieren und anfangen, wie Alpha‑Zellen auszusehen und zu funktionieren, anstatt einfach zu verschwinden.
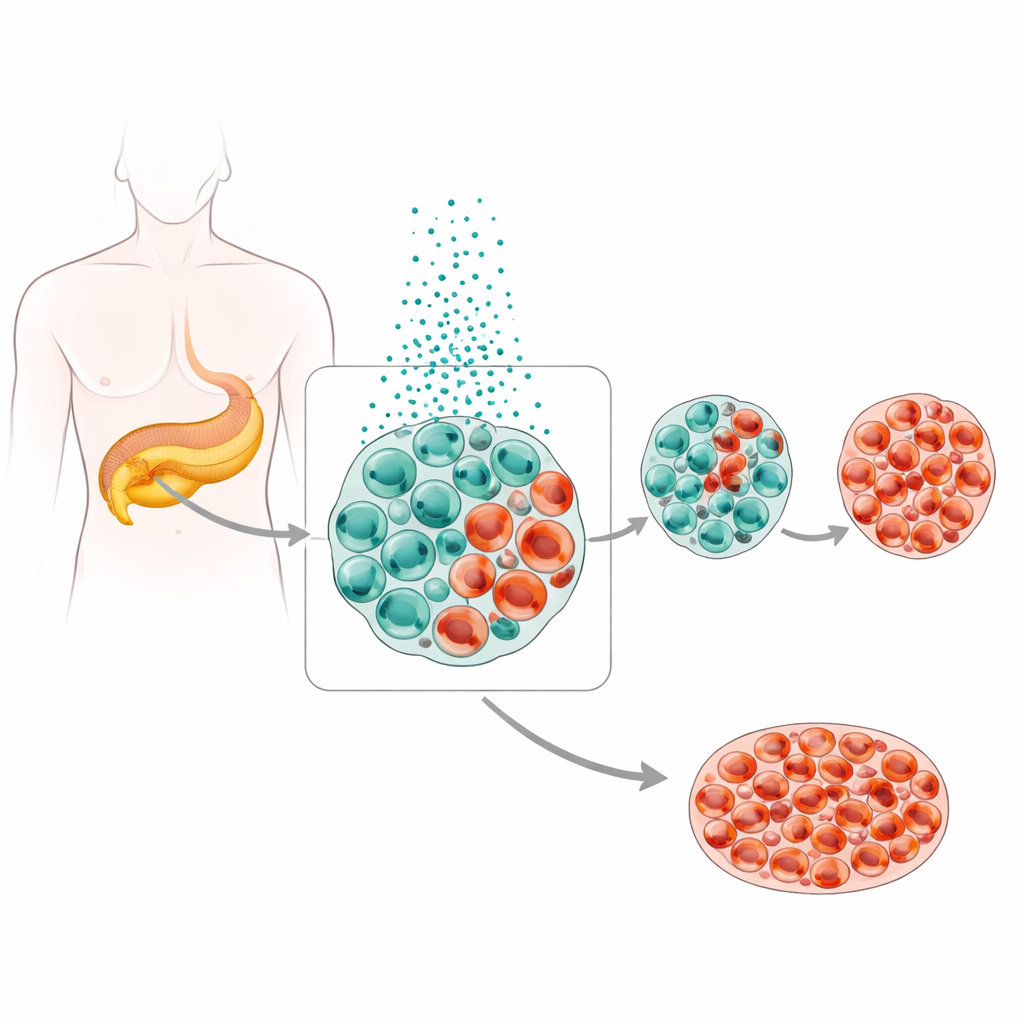
Ein Metall mit zwei Gesichtern
Zink ist für Beta‑Zellen essentiell, weil es hilft, Insulin für Speicherung und Freisetzung zu verpacken. Diese Zellen führen jedoch ohnehin Zink in Konzentrationen, die deutlich über denen der meisten anderen Gewebe liegen, und die Studie zeigt, dass eine weitere Erhöhung gefährlich wird. Ein spezifisches Transportprotein, ZnT8, befördert normalerweise Zink in die Insulinspeichergranula. In Inseln von Menschen mit Typ‑2‑Diabetes und in diabetischen Mäusen waren die ZnT8‑Spiegel deutlich erhöht, und Messungen zeigten eine klare Zinkakkumulation in den Zellen. Wenn die Forschenden menschliche Inseln dazu brachten, mehr ZnT8 zu produzieren, oder sie in zusätzliches Zink bzw. eine Zink‑tragende Verbindung tauchten, nahm die Anzahl der Beta‑Zellen ab, während Alpha‑Zellen und gemischte Insulin‑Glukagon‑Zellen zunahmen — sowohl in Kultur als auch in lebenden Mäusen. Genetische Eingriffe, die ZnT8 reduzierten, hielten dagegen die Zinkspiegel niedriger und bewahrten die Beta‑Zell‑Identität besser.
Stress im Inneren der Zelle: ein molekularer Kipppunkt
Um zu verstehen, wie überschüssiges Zink das Zellschicksal verändert, nutzte das Team aus Stammzellen gewonnene Inseln als manipulierbares menschliches Modell. Unter anhaltend hohem Glukosespiegel bauten diese im Labor gezüchteten Beta‑Zellen allmählich Zink auf und begannen, alpha‑ähnliche Merkmale zu entwickeln. Einzelzell‑Genexpressionsanalysen zeigten, dass mit steigendem Zink die Beta‑Zellen ein zelluläres Alarmsystem aktivierten, die sogenannte integrierte Stressantwort. Dieser Weg senkt die allgemeine Proteinproduktion, steigert jedoch stark einen Faktor namens ATF4. Die Forschenden zeigten, dass ATF4 direkt an die Kontrollregion von ARX binden kann — einem Schalter, der normalerweise Alpha‑Zellen definiert — und dessen Aktivität erhöht. Wenn ATF4 oder Zink verstärkt wurden, trat ARX in Beta‑Zellen auf und die Zellen konvertierten in Richtung einer Alpha‑Identität; wenn der Stressweg mit einem kleinen Molekülhemmer blockiert wurde, wurde diese Umwandlung weitgehend verhindert.
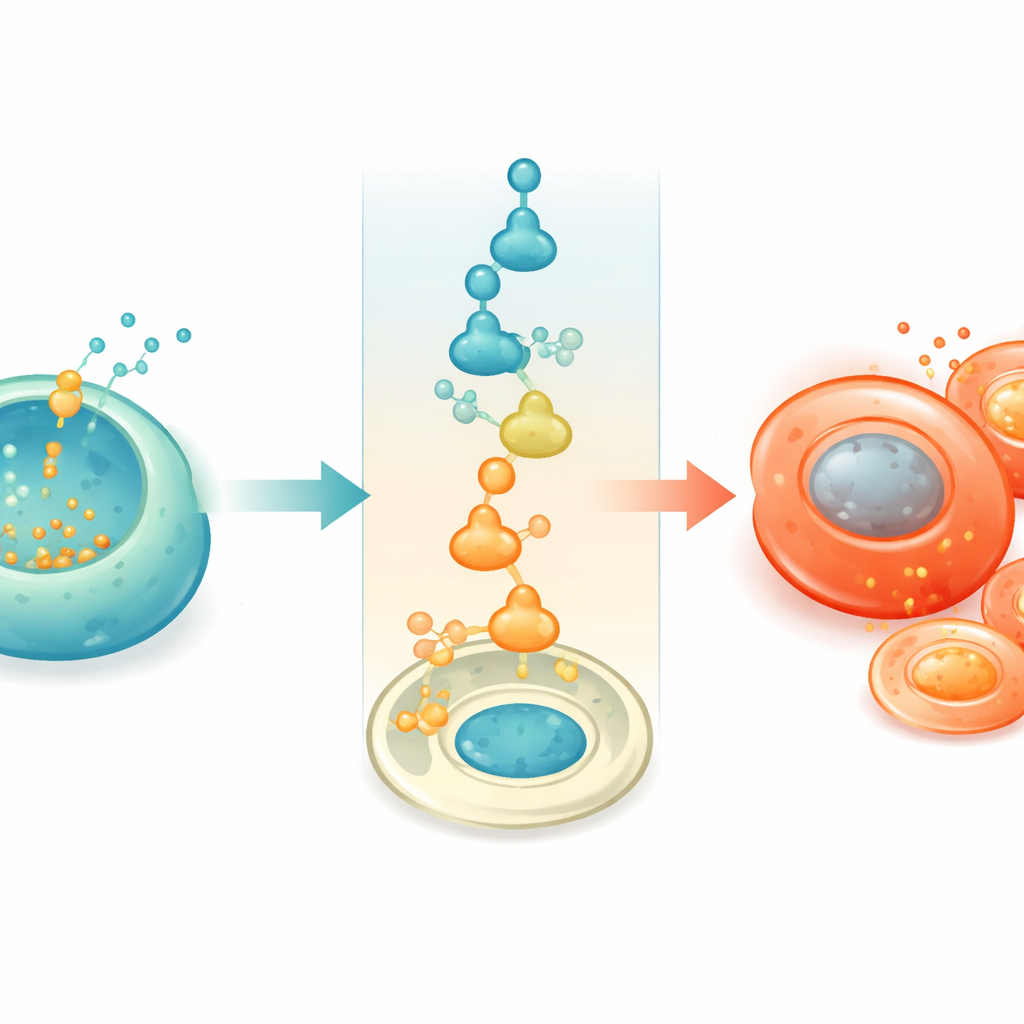
Schutz von Ersatzzellen im diabetischen Körper
Der gleiche zinkgetriebene Identitätsverlust trat auf, wenn menschliche Inseln oder reine, aus Stammzellen hergestellte Beta‑Zellen in diabetische Mäuse transplantiert wurden. In der zuckerreichen Umgebung akkumulierten die transplantierten Beta‑Zellen Zink, verloren ihre charakteristischen Merkmale und produzierten mehr glukagonähnliche Zellen, was die Blutzuckerregulation verschlechterte. Das Eingreifen in die Zink‑Stress‑Achse veränderte dieses Ergebnis. Die Gabe eines Inhibitors der Stressantwort bewahrte mehr beta‑ähnliche Zellen und verbesserte Insulinausschüttung und Glukosetoleranz. Ebenso halfen Beta‑Zellen, denen ZnT8 fehlte, oder die Behandlung mit einer niedrigen Dosis des Wirkstoffs Anisomycin, die selektiv ZnT8 und Zinkansammlungen verringerte, die Beta‑Zell‑Identität zu erhalten und transplantierte Zellen wirksamer beim Senken des Blutzuckers zu machen — ohne offensichtliche Toxizität in den untersuchten Tieren.
Was das für zukünftige Diabetes‑Therapien bedeutet
Diese Arbeit zeichnet ein klares Bild: Beim Typ‑2‑Diabetes regt chronisch hoher Blutzucker Beta‑Zellen dazu an, Zink zu horten, wodurch ein internes Stresssystem aktiviert wird, das ein alpha‑Zell‑Genprogramm einschaltet. Viele Beta‑Zellen werden statt zu sterben im Grunde in den falschen Hormon produzierenden Typ umprogrammiert und schwächen so die Glukosekontrolle des Körpers. Durch das Anvisieren der Zinkverarbeitung oder der nachgeschalteten Stressantwort könnte man Beta‑Zellen sowohl im eigenen Pankreas von Patientinnen und Patienten als auch in transplantierten oder aus Stammzellen erzeugten Zellen für Therapien „auf Kurs“ halten. Zwar ist noch viel Arbeit nötig, bevor diese Strategien klinisch anwendbar sind, doch die Studie liefert eine konkrete molekulare Landkarte zum Schutz der insulinproduzierenden Zellen.
Zitation: Ma, Q., Xu, W., Wang, X. et al. Zinc accumulation-induced integrated stress response triggers β-cell identity loss. Cell Res 36, 359–376 (2026). https://doi.org/10.1038/s41422-026-01222-y
Schlüsselwörter: Typ‑2‑Diabetes, Beta‑Zell‑Identität, Zinkakkumulation, Pankreasinseln, Stammzell‑Inseln