Clear Sky Science · pl
Nadmierne gromadzenie cynku wywołuje zintegrowaną odpowiedź na stres i prowadzi do utraty tożsamości komórek β
Dlaczego to badanie ma znaczenie dla osób z cukrzycą
Cukrzycę typu 2 często tłumaczy się jako „wyczerpanie” komórek produkujących insulinę, ale wiele z tych komórek nie ginie po prostu — zmienia swoją tożsamość. To badanie ujawnia zaskakującego winowajcę tego kryzysu tożsamości: nadmiar cynku we wnętrzu komórek produkujących insulinę w trzustce. Śledząc, co dzieje się zarówno w komórkach ludzkich, jak i mysich oraz w mini‑wyspach pochodzących z komórek macierzystych, autorzy opisują, jak przeciążenie cynkiem stresuje te komórki i popycha je do przyjęcia niewłaściwego typu komórkowego oraz jak ten proces można spowolnić lub nawet odwrócić.
Kiedy komórki produkujące insulinę zapominają swojej roli
U zdrowych osób wyspy trzustkowe zawierają różne komórki wydzielające hormony ułożone w delikatnej równowadze, z komórkami beta produkującymi insulinę jako kluczowymi wykonawcami. W cukrzycy typu 2 lekarze obserwują mniej komórek beta i więcej komórek alfa, które wytwarzają glukagon — hormon podnoszący poziom cukru we krwi. Zespół przeanalizował obszerne zestawy danych z pojedynczych komórek z ludzkich trzustek i znalazł płynną „trajektorię” od typowych komórek beta w kierunku komórek przypominających alfa, włącznie z komórkami hybrydowymi łączącymi cechy obu. Próbki tkankowe od osób z cukrzycą i bez niej oraz modele mysie potwierdziły, że przy wysokim stężeniu glukozy coraz więcej komórek beta traci swoją pierwotną tożsamość i zaczyna przypominać komórki alfa zamiast po prostu zanikać.
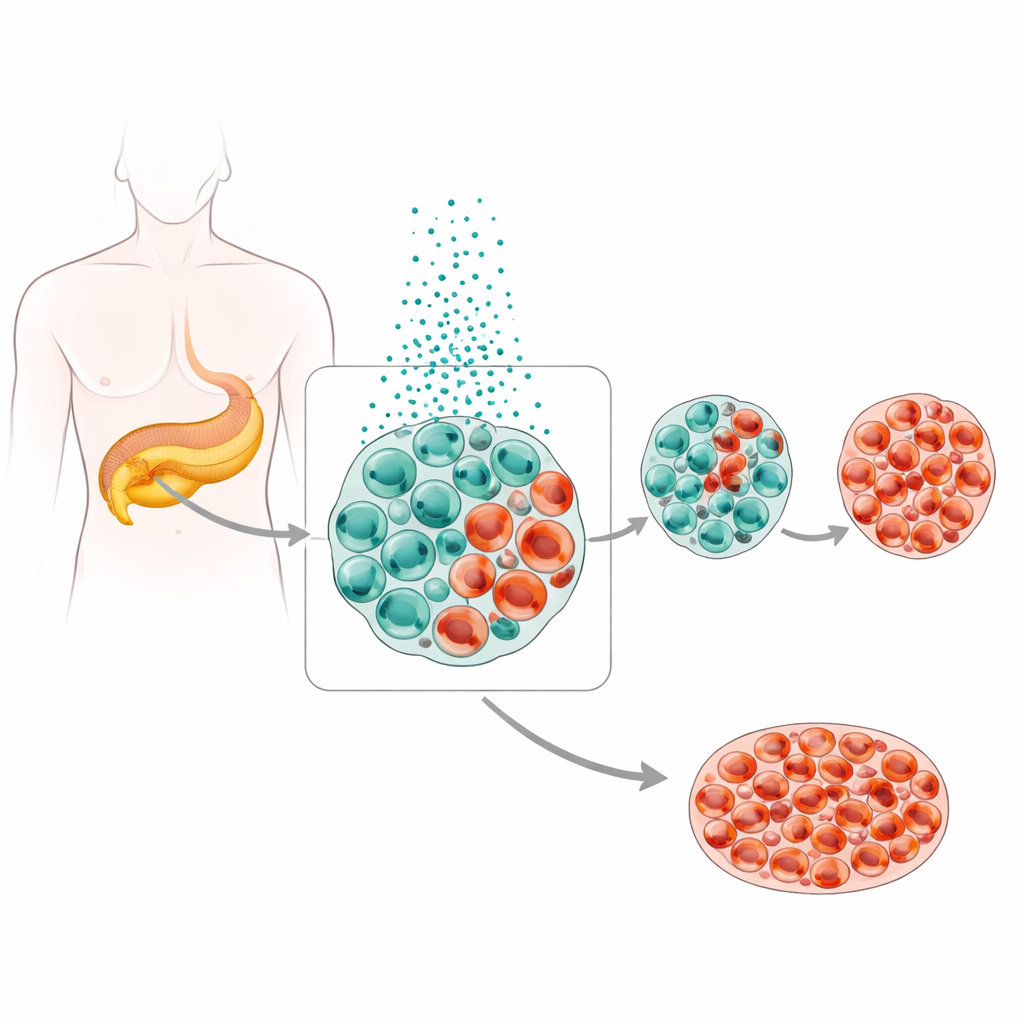
Metal o dwoistej naturze
Cynk jest niezbędny dla komórek beta, ponieważ pomaga pakować insulinę do ziarnistości do magazynowania i uwalniania. Jednak te komórki zawierają już poziomy cynku znacznie wyższe niż większość tkanek, a badanie pokazuje, że dalsze zwiększenie staje się szkodliwe. Specyficzny białkowy transporter, ZnT8, normalnie przenosi cynk do ziarenek insuliny. W wyspach od osób z cukrzycą typu 2 i w wyspach mysich z cukrzycą poziomy ZnT8 były wyraźnie podwyższone, a pomiary cynku wewnątrzkomórkowego wykazały jego akumulację. Gdy badacze zmusili ludzkie wyspy do produkcji większej ilości ZnT8 lub eksponowali je na dodatkowy cynk bądź związek przenoszący cynk, liczba komórek beta malała, podczas gdy komórek alfa i mieszanych komórek insulinowo‑glukagonowych przybywało — zarówno w hodowlach, jak i u żywych myszy. Sztuczki genetyczne zmniejszające ZnT8 przeciwnie utrzymywały niższe poziomy cynku i lepiej chroniły tożsamość komórek beta.
Stres wewnątrz komórki: molekularny punkt przechyłowy
Aby zrozumieć, jak nadmiar cynku zmienia losy komórkowe, zespół sięgnął po wyspy pochodzące z komórek macierzystych — model ludzki, którym mogli manipulować szczegółowo. Przy długotrwałym wysokim stężeniu glukozy te laboracyjne komórki beta stopniowo gromadziły cynk i zaczynały przechodzić w kierunku cech przypominających komórki alfa. Profilowanie genów pojedynczych komórek ujawniło, że wraz ze wzrostem cynku komórki beta uruchamiały wewnątrzkomórkowy alarm zwany zintegrowaną odpowiedzią na stres. Ta ścieżka zmniejsza ogólną produkcję białek, ale silnie zwiększa czynnik zwany ATF4. Badacze pokazali, że ATF4 może bezpośrednio wiązać się z regionem kontrolnym ARX — głównym przełącznikiem definiującym komórki alfa — i go włączać. Gdy ATF4 lub cynk były podwyższone, ARX pojawiał się w komórkach beta i komórki przekształcały się w kierunku tożsamości alfa; gdy ścieżkę stresową zablokowano małocząsteczkowym inhibitorem, ta konwersja była w dużej mierze powstrzymywana.
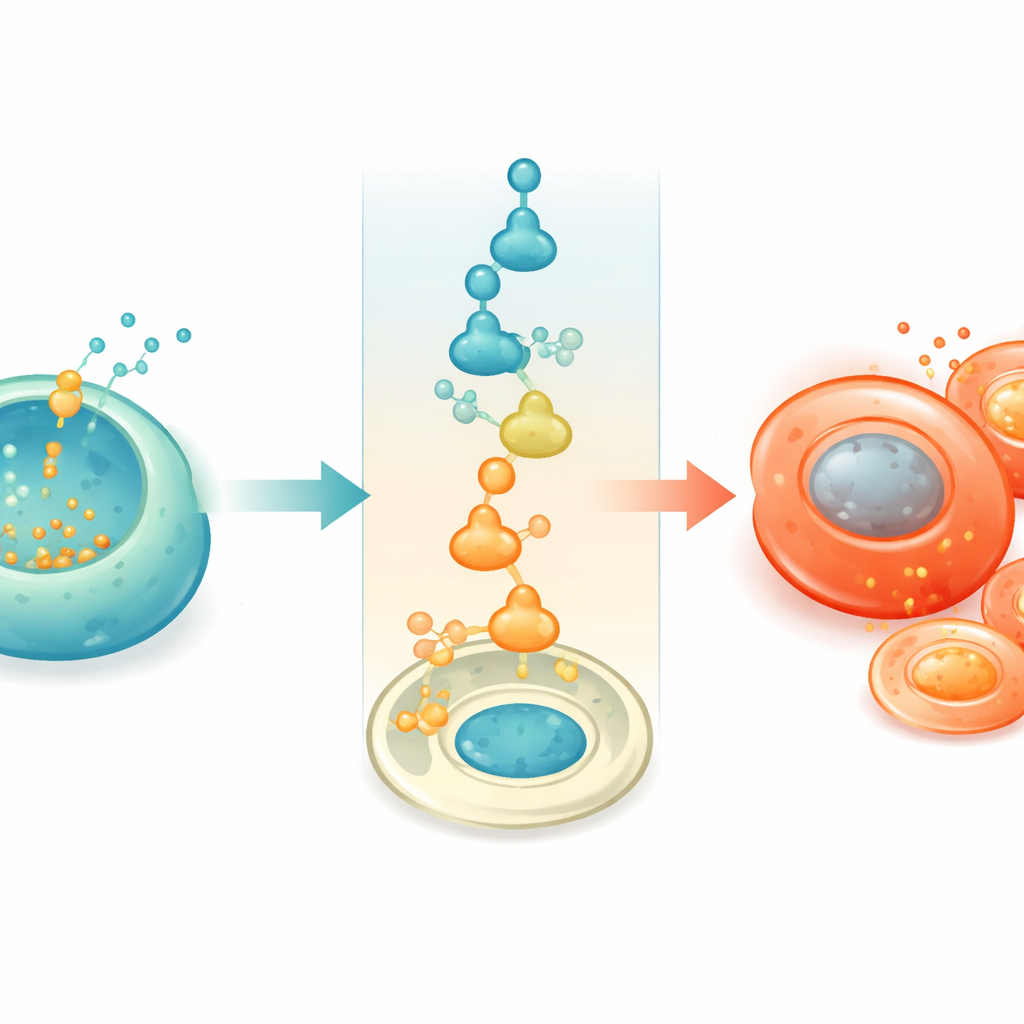
Ochrona komórek zastępczych w cukrzycowym organizmie
Ta sama zależna od cynku utrata tożsamości występowała, gdy ludzkie wyspy lub czyste komórki beta pochodzące z komórek macierzystych były przeszczepiane do myszy z cukrzycą. W środowisku o wysokim poziomie cukru przeszczepione komórki beta gromadziły cynk, traciły swoje charakterystyczne cechy i generowały więcej komórek podobnych do alfa, co osłabiało kontrolę glikemii. Zakłócenie osi cynk–stres zmieniało ten rezultat. Podawanie myszy inhibitora odpowiedzi na stres chroniło więcej komórek o fenotypie beta i poprawiało wydzielanie insuliny oraz tolerancję glukozy. Podobnie użycie komórek beta zaprojektowanych tak, by nie miały ZnT8, albo leczenie komórek niską dawką anisomycyny, która selektywnie obniżała ZnT8 i nagromadzenie cynku, pomagało utrzymać tożsamość komórek beta i sprawiało, że przeszczepione komórki skuteczniej obniżały poziom cukru, bez oczywistej toksyczności u badanych zwierząt.
Co to oznacza dla przyszłych terapii cukrzycy
Praca ta kreśli jasny obraz: w cukrzycy typu 2 przewlekle wysoki poziom cukru pobudza komórki beta do gromadzenia cynku, co włącza wewnętrzny system stresowy aktywujący program genowy komórek alfa. Zamiast umierać, wiele komórek beta jest w istocie przeprogramowywanych na niewłaściwy typ wydzielający hormon, co podważa zdolność organizmu do kontroli glukozy. Poprzez celowanie w gospodarkę cynkiem lub w następczą odpowiedź na stres można potencjalnie utrzymać komórki beta „przy skrypcie”, zarówno w trzustce pacjenta, jak i w komórkach przeszczepianych czy pochodzących z komórek macierzystych używanych w terapii. Choć przed wprowadzeniem tych strategii do kliniki potrzeba jeszcze wielu badań, badanie oferuje konkretną molekularną mapę drogową do ochrony komórek produkujących insulinę.
Cytowanie: Ma, Q., Xu, W., Wang, X. et al. Zinc accumulation-induced integrated stress response triggers β-cell identity loss. Cell Res 36, 359–376 (2026). https://doi.org/10.1038/s41422-026-01222-y
Słowa kluczowe: cukrzyca typu 2, tożsamość komórek beta, nagromadzenie cynku, wyspy trzustkowe, wyspy pochodzące z komórek macierzystych