Clear Sky Science · nl
Door zinkstapeling geïnduceerde geïntegreerde stressrespons veroorzaakt verlies van β-celidentiteit
Waarom dit onderzoek belangrijk is voor mensen met diabetes
Type 2 diabetes wordt vaak uitgelegd als het lichaam dat "insulineproducerende cellen raakt kwijt", maar veel van deze cellen sterven niet zomaar — ze veranderen van identiteit. Deze studie onthult een verrassende schuldige in die identiteitscrisis: te veel zink binnen in de insulineproducerende cellen van de alvleesklier. Door te volgen wat er gebeurt in zowel menselijke als muizencellen, en in stamcel-afgeleide mini-eilandjes, beschrijven de auteurs hoe zinkoverdaad deze cellen onder stress zet en ze dwingt het verkeerde celtype te worden, en hoe dat proces mogelijk vertraagd of zelfs omgekeerd kan worden.
Wanneer insulinecellen hun taak vergeten
Bij gezonde mensen bevatten pancreas-eilandjes verschillende hormoonproducerende cellen in een delicate balans, waarbij insulineproducerende bèta-cellen de hoofdrol spelen. Bij type 2 diabetes merken artsen minder bèta-cellen en meer alfa-cellen, die glucagon maken, een hormoon dat de bloedglucose verhoogt. Het team onderzocht grote enkelceldatasets uit menselijke pancreas en vond een geleidelijke "traject" van typische bèta-cellen richting alfa-achtige cellen, inclusief hybride cellen die kenmerken van beide dragen. Weefselmonsters van mensen met en zonder diabetes, samen met diabetische muismodellen, bevestigden dat bij hoge bloedglucose meer bèta-cellen hun oorspronkelijke identiteit verliezen en eerder gaan lijken en functioneren als alfa-cellen in plaats van simpelweg te verdwijnen.
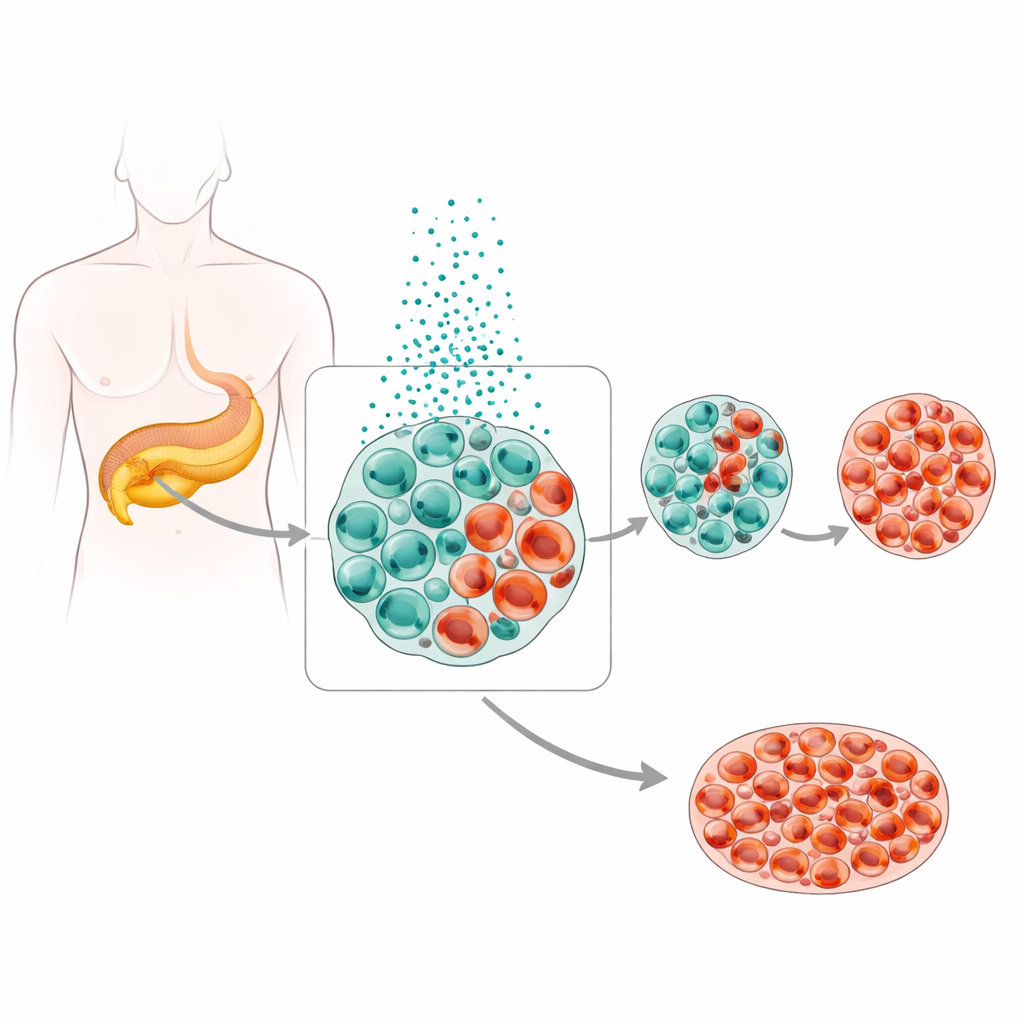
Een metaal met twee gezichten
Zink is essentieel voor bèta-cellen omdat het helpt insuline in te pakken voor opslag en vrijgave. Maar deze cellen bevatten van zichzelf al veel hogere zinkniveaus dan de meeste andere weefsels, en de studie toont aan dat het nog verder opvoeren van zink gevaarlijk wordt. Een specifiek transportereiwit, ZnT8, verplaatst normaal zink in insulinegranules. In eilandjes van mensen met type 2 diabetes en in diabetische muizen waren ZnT8-niveaus duidelijk hoger, en metingen van zink binnenin de cellen toonden duidelijke ophoping. Toen de onderzoekers menselijke eilandjes dwongen meer ZnT8 te maken, of ze in extra zink of een zinkdragende verbinding plaatsten, namen het aantal bèta-cellen af terwijl alfa-cellen en gemengde insuline–glucagoncellen toenamen, zowel in kweek als in levende muizen. Genetische ingrepen die ZnT8 juist verlaagden hielden daarentegen de zinkniveaus lager en bewaarden beter de bèta-celidentiteit.
Stress binnen de cel: een moleculair kantelpunt
Om te begrijpen hoe overtollig zink de celfate verandert, wendde het team zich tot stamcel-afgeleide eilandjes, een humaan model dat ze gedetailleerd konden manipuleren. Bij langdurig hoge glucose bouwden deze in het lab gekweekte bèta-cellen geleidelijk zink op en begonnen ze in de richting van alfa-achtige kenmerken te verschuiven. Enkelceld-genprofilering toonde aan dat, naarmate zink toenam, bèta-cellen een cellulair alarmsysteem inschakelden dat de geïntegreerde stressrespons wordt genoemd. Deze route vermindert de algemene eiwitsynthese maar verhoogt sterk een factor genaamd ATF4. De onderzoekers lieten zien dat ATF4 zich direct kan binden aan het regelgebied van ARX, een meesterregelaar die normaal alfa-cellen definieert, en het kan activeren. Wanneer ATF4 of zink verhoogd werden, verscheen ARX in bèta-cellen en converteerden de cellen naar een alfa-identiteit; wanneer de stressroute werd geblokkeerd met een kleine molecuulremmer, werd deze conversie grotendeels voorkomen.
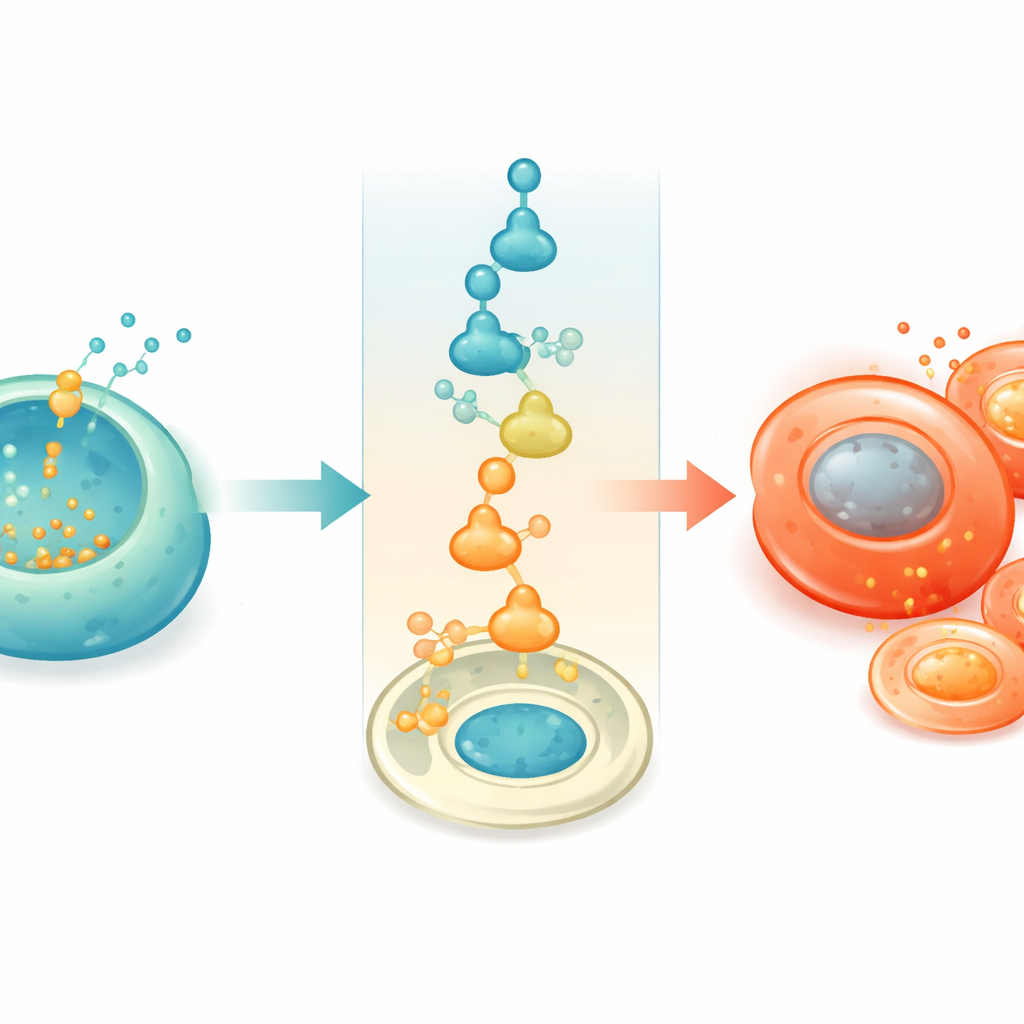
Vervangende cellen beschermen in een diabetisch lichaam
Dezelfde door zink gedreven identiteitsverlies trad op wanneer menselijke eilandjes of zuivere stamcel-afgeleide bèta-cellen werden getransplanteerd in diabetische muizen. In de hoge-suikervoorziening hoopten getransplanteerde bèta-cellen zink op, verloren hun kenmerkende eigenschappen en produceerden meer glucagonachtige cellen, wat de glucoseregeling verzwakte. Interferentie met de zink–stress-as veranderde dit resultaat. Toediening van een remmer van de stressrespons aan muizen behield meer bèta-achtige cellen en verbeterde insulineafgifte en glucosetolerantie. Evenzo hielpen bèta-cellen die genetisch zo waren aangepast dat ze ZnT8 misten, of behandeling van cellen met een lage dosis van het middel anisomycine die selectief ZnT8 en zinkophoping verminderde, om de bèta-celidentiteit te behouden en maakten getransplanteerde cellen effectiever in het verlagen van bloedglucose, allemaal zonder duidelijke toxiciteit in de bestudeerde dieren.
Wat dit betekent voor toekomstige diabetesbehandelingen
Dit werk schetst een helder beeld: bij type 2 diabetes stimuleert chronisch hoge bloedglucose bèta-cellen om zink te hamsteren, wat een intern stresssysteem activeert dat een alfacel-genprogramma inschakelt. In plaats van te sterven, worden veel bèta-cellen in wezen omgeprogrammeerd tot het verkeerde hormoonproducerende type, wat het vermogen van het lichaam om glucose te regelen ondermijnt. Door zinkhandeling of de daarachter liggende stressrespons te richten, zou het mogelijk kunnen zijn bèta-cellen "op script" te houden, zowel in iemands eigen pancreas als in getransplanteerde of stamcel-afgeleide cellen die voor therapie worden gebruikt. Hoewel er nog veel werk nodig is voordat deze strategieën de kliniek bereiken, biedt de studie een concreet moleculair stappenplan om de cellen die insuline maken te beschermen.
Bronvermelding: Ma, Q., Xu, W., Wang, X. et al. Zinc accumulation-induced integrated stress response triggers β-cell identity loss. Cell Res 36, 359–376 (2026). https://doi.org/10.1038/s41422-026-01222-y
Trefwoorden: type 2 diabetes, beta-celidentiteit, zinkstapeling, pancreatische eilandjes, stamcel-eilandjes