Clear Sky Science · zh
MEKK3 连接肠-脑通讯与脑海绵状血管畸形的发病机制
为何肠道可能与脑出血有关
脑海绵状血管畸形是大脑中由脆弱血管簇构成的病灶,可能渗漏或出血,引发癫痫、头痛和中风。本文综述探讨了一个令人意外的线索:肠道中的微小微生物及其释放的化学信号,可能影响这些异常血管是否形成或加重。作者沿着从肠道细菌到血液再到大脑的链条阐述,指出血管细胞内的一个信号枢纽 MEKK3,可能是将肠道扰动转化为危险脑病变的关键中继点。
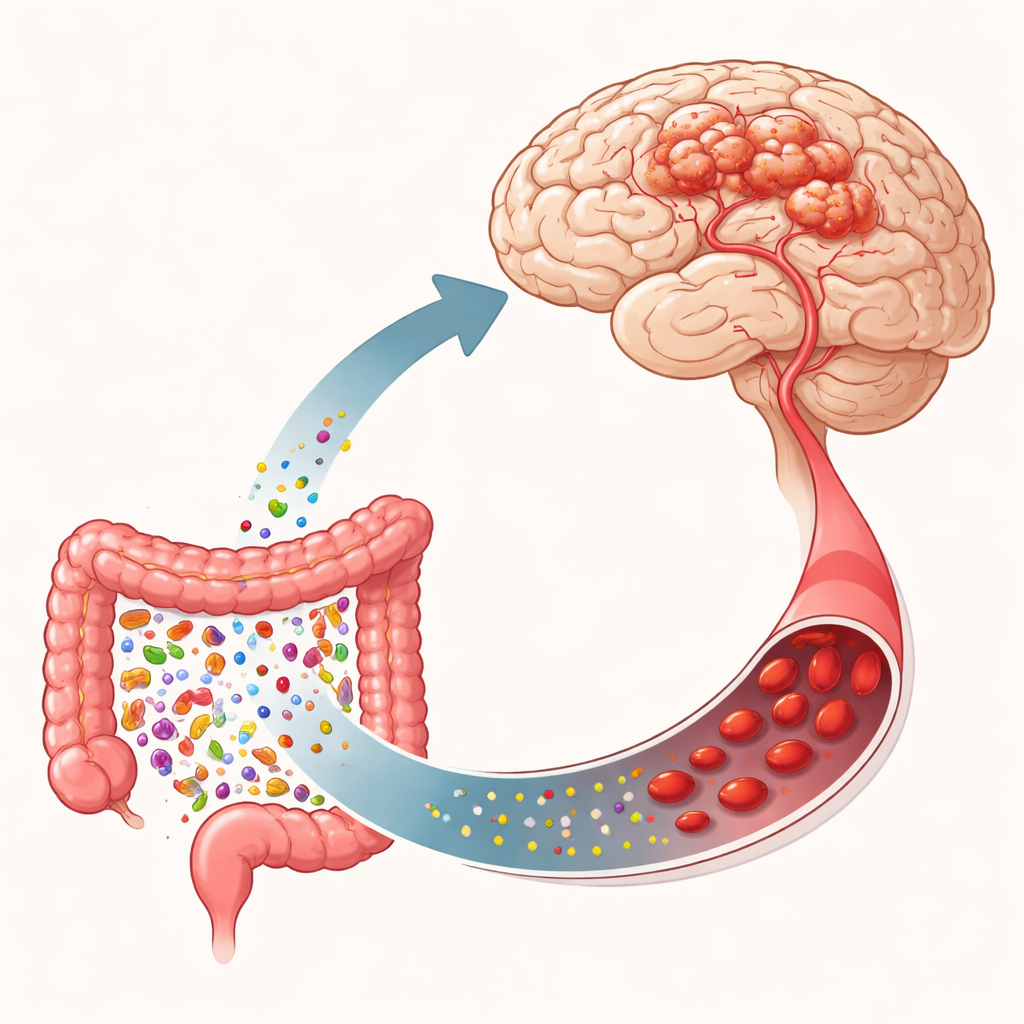
藏在脑血管中的薄弱环节
脑海绵状血管畸形(CCM)影响大约数百人中的一人,尽管许多人并不知情。这些畸形由薄壁、囊状的血管构成,可能破裂。一部分病例是偶发的,表现为单发病灶,而另一部分则有家族遗传性且多发。遗传性病例通常源自三个基因(通常称为 CCM1、CCM2 和 CCM3)中某一基因的破坏性变异,这些基因有助于维持血管内皮的紧密性和稳定性。当这些基因失效时,血管细胞间的连接变松,血管异常扩张,可能形成海绵状的纠结。生长通路中的额外突变,例如 PIK3CA,能够驱动这些脆弱细胞增殖和重塑,使病灶变大并更具侵袭性。
名为 MEKK3 的细胞“交换台”
本故事的核心是 MEKK3,一种存在于血管细胞内、如同交换台般整合多种输入信号的蛋白。遗传学研究显示,MEKK3 基因(MAP3K3)中特定变异足以在动物模型中触发海绵状畸形,从而界定了患者的一个独特亚群。MEKK3 的活性控制着其它因子 KLF2 和 KLF4,后者进而影响细胞黏附的紧密程度、增殖水平以及血管壁的通透性。当 MEKK3 过度活跃时,内皮细胞之间的连接变弱,通常将血液与脑组织隔开的屏障变得多孔,畸形更容易增大和出血。MEKK3 并非孤立工作;它与 VEGF、PI3K 等生长信号以及对血流机械力和炎症反应的通路相互交叉。
肠道如何与大脑对话
肠-脑轴是连接肠道与神经系统的通讯网络,通过神经、免疫细胞、激素和微生物化学物质相互作用。本文综述强调了其中的一条通路:肠道微生物产物进入血液循环并影响脑血管的过程。当肠道菌群失衡时,某些细菌会释放脂多糖(LPS)——它们外膜的成分——进入血液循环。LPS 可松动肠道屏障,进一步增加自身进入血液的机会。一旦到达脑血管,LPS 会激活内皮细胞表面的感受器 TLR4,进而触发 MEKK3 及其下游炎性级联反应。其结果是血管更多渗漏、免疫细胞被招募,以及 CCM 病灶的进展。其他来源于肠道的分子,如短链脂肪酸、三甲胺氧化物(TMAO)和吲哚相关化合物,依其平衡状况可支持屏障健康或助长炎症。
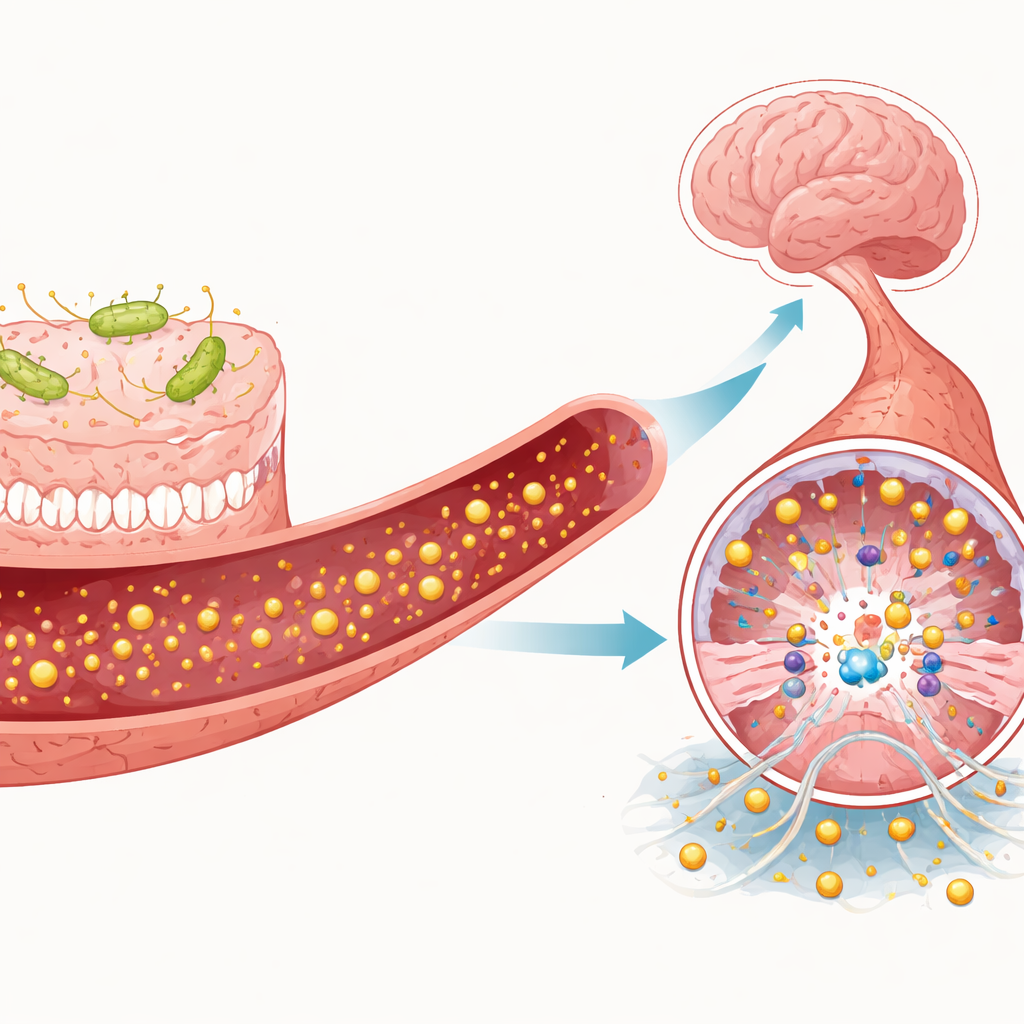
微生物与免疫细胞的有益与有害信号
文章详述了单个肠道代谢产物和免疫细胞如何将 MEKK3 信号推向损伤或保护方向。由微生物分解膳食纤维产生的短链脂肪酸(如丁酸)似乎能增强血脑屏障,并可能间接抑制 TLR4 和 MEKK3 活性。相反,TMAO 和某些吲哚衍生物(如吲哚硫酸盐)会促进炎症、氧化应激并增强 TLR4 信号,从而可能加剧 MEKK3 的激活。免疫细胞也参与其中。中性粒细胞可释放粘稠的细胞外网,进一步刺激血管细胞上的 TLR4;促炎性巨噬细胞和 T 辅助细胞增强与 MEKK3 相关的通路,而抗炎细胞则可能抑制这些通路。综合来看,这些信号形成了一场动态的拉锯战,决定大脑血管是保持稳定还是恶化为海绵状病灶。
通往更温和治疗的新途径
目前对脑海绵状血管畸形的治疗选择有限,常依赖于手术或对高风险病灶的精准放疗。作者认为,了解肠道微生物及其产物如何影响以 MEKK3 为中心的信号网络,开辟了新的、侵入性更小的可能性。原则上,未来的疗法可以将以微生物组为导向的策略——如饮食调整、益生菌或靶向减少有害代谢产物——与抑制脑血管中 TLR4 或 MEKK3 活性的药物相结合。对非专业读者而言,结论是:肠道问题能对大脑血管健康产生深远影响,而像 MEKK3 这样的单一细胞“枢纽”可能是减弱这种有害对话、预防危险性脑出血的关键。
引用: Cheng, P., Han, H., Huang, Y. et al. MEKK3 bridges gut-brain communication and cerebral cavernous malformation pathogenesis. Cell Death Discov. 12, 197 (2026). https://doi.org/10.1038/s41420-026-03062-6
关键词: 脑海绵状血管畸形, 肠-脑轴, MEKK3 信号传导, 肠道菌群代谢产物, 神经血管炎症