Clear Sky Science · de
MEKK3 vermittelt die Kommunikation zwischen Darm und Gehirn und die Pathogenese zerebraler kavernöser Malformationen
Warum der Darm für Hirnblutungen wichtig sein könnte
Zerebrale kavernöse Malformationen sind Ansammlungen fragiler Blutgefäße im Gehirn, die undicht werden oder bluten können und Krampfanfälle, Kopfschmerzen und Schlaganfälle verursachen. Dieser Übersichtsartikel beleuchtet eine überraschende Wendung: winzige Mikroben in unserem Darm und die chemischen Signale, die sie freisetzen, könnten beeinflussen, ob sich diese abnormalen Gefäße bilden oder verschlimmern. Indem die Autoren der Kette von Darmbakterien über das Blut bis zum Gehirn folgen, heben sie einen Signalknoten namens MEKK3 in den Gefäßzellen als wichtigen Relay-Punkt hervor, der Darmstörungen in gefährliche Hirnherde übersetzen könnte.
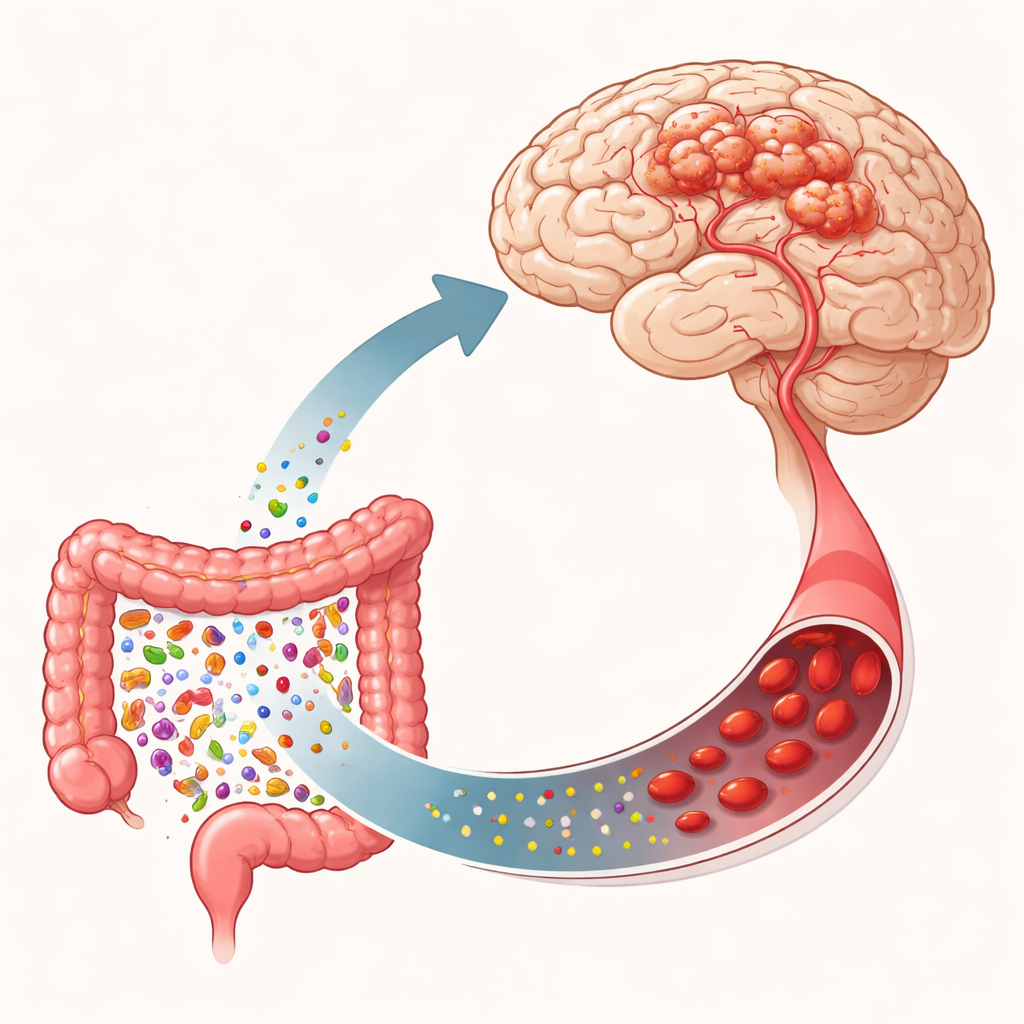
Versteckte Schwachstellen in Gehirngefäßen
Zerebrale kavernöse Malformationen (CCM) betreffen etwa eine von einigen Hundert Personen, viele wissen jedoch nie, dass sie sie haben. Diese Malformationen bestehen aus dünnwandigen, ballonartigen Gefäßen, die einreißen können. Manche Fälle sind sporadisch und treten als einzelne Läsionen auf, andere treten familiär auf und umfassen mehrere Läsionen. Erbliche Formen beruhen meist auf schädigenden Veränderungen in einem von drei Genen (häufig CCM1, CCM2 und CCM3 genannt), die dazu beitragen, die Auskleidung der Blutgefäße dicht und stabil zu halten. Versagen diese Gene, lockern sich die Verbindungen zwischen Gefäßzellen, die Gefäße weiten sich abnormal und es können kavernartige Verwicklungen entstehen. Zusätzliche Mutationen in Wachstumswegen, wie etwa PIK3CA, können diese fragilen Zellen zur Vermehrung und Umgestaltung antreiben, wodurch Läsionen größer und aggressiver werden.
Ein zelluläres Schaltzentrum namens MEKK3
Im Zentrum dieser Geschichte steht MEKK3, ein Protein in Gefäßzellen, das wie ein Schaltzentrum für viele eintreffende Signale wirkt. Genetische Studien zeigen, dass spezifische Veränderungen im MEKK3-Gen (MAP3K3) ausreichen, um in Tiermodellen kavernöse Malformationen auszulösen und eine eigene Patientengruppe zu definieren. Die MEKK3-Aktivität steuert andere Faktoren, KLF2 und KLF4, die wiederum beeinflussen, wie eng Zellen aneinander haften, wie stark sie proliferieren und wie durchlässig die Gefäßwand wird. Bei überaktiver MEKK3 lockern sich die Verbindungen zwischen Endothelzellen, die Barriere, die normalerweise Blut vom Hirngewebe trennt, wird porös, und Malformationen wachsen und bluten eher. MEKK3 agiert nicht isoliert; es kreuzt sich mit Wachstumssignalen wie VEGF und PI3K sowie mit Wegen, die auf physikalischen Blutfluss und Entzündung reagieren.
Wie der Darm mit dem Gehirn spricht
Die Darm–Hirn-Achse ist das Kommunikationsnetzwerk, das den Darm mit dem Nervensystem über Nerven, Immunzellen, Hormone und mikrobielle Chemikalien verbindet. Diese Übersichtsarbeit betont insbesondere einen Weg: das Eindringen mikrobieller Produkte aus dem Darm in den Blutkreislauf und von dort in die Blutgefäße des Gehirns. Wenn die Darmgemeinschaft aus dem Gleichgewicht gerät, setzen bestimmte Bakterien Lipopolysaccharid (LPS) frei, einen Bestandteil ihrer äußeren Membran, der in die Zirkulation gelangt. LPS kann die Darmbarriere lockern und so seinen eigenen Übergang ins Blut weiter erhöhen. Einmal in den Hirngefäßen, aktiviert LPS einen Oberflächensensor namens TLR4 auf Endothelzellen, der dann MEKK3 und nachgeschaltete entzündliche Kaskaden auslöst. Das Ergebnis sind verstärkte Gefäßundichtigkeit, Anlockung von Immunzellen und Fortschreiten von CCM-Läsionen. Andere darmabgeleitete Moleküle, wie kurzkettige Fettsäuren, Trimethylamin-N-oxid (TMAO) und Indol-assoziierte Verbindungen, können je nach ihrem Gleichgewicht entweder die Barrieregesundheit unterstützen oder Entzündungen fördern.
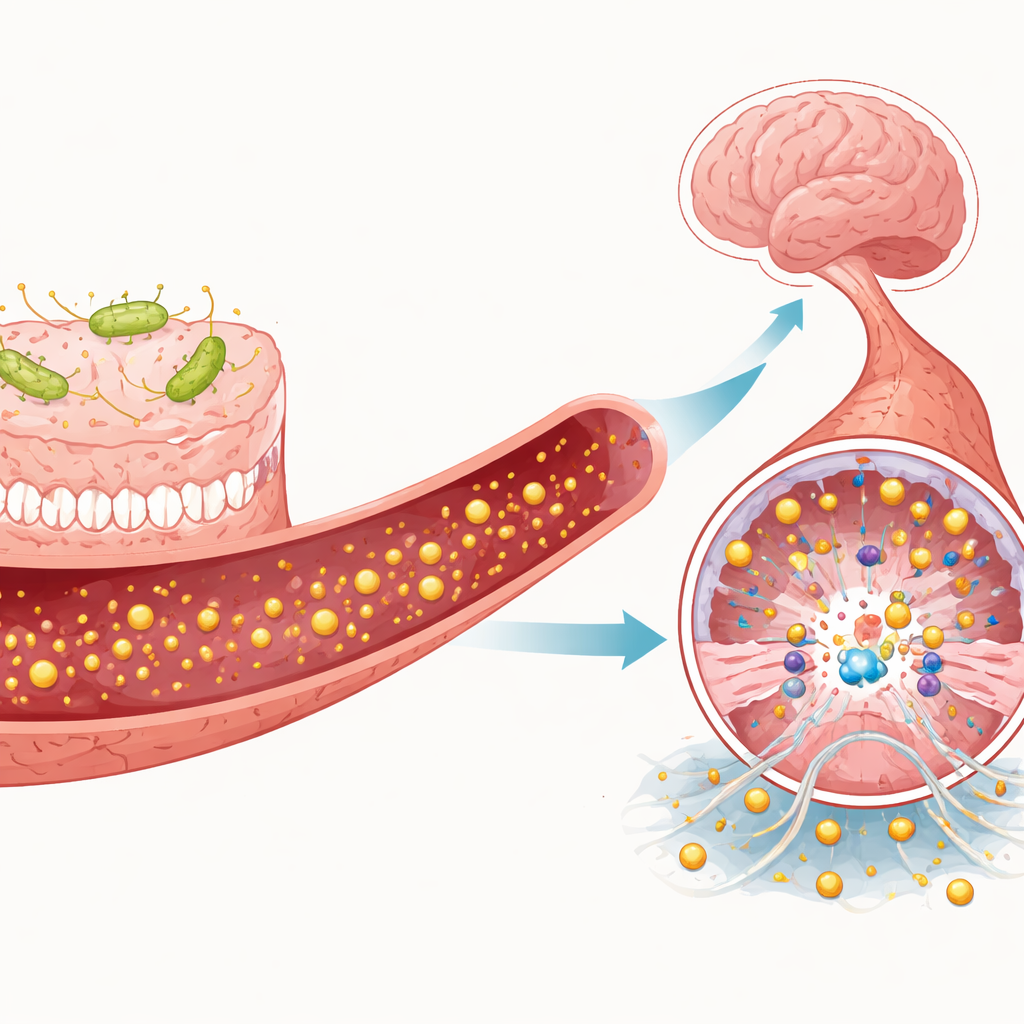
Hilfreiche und schädliche Signale von Mikroben und Immunzellen
Der Artikel beschreibt, wie einzelne Darmmetaboliten und Immunzellen die MEKK3-Signalgebung in Richtung Schaden oder Schutz kippen können. Kurzkettige Fettsäuren wie Butyrat, die entstehen, wenn Mikroben Ballaststoffe verstoffwechseln, scheinen die Blut–Hirn-Schranke zu stärken und können indirekt TLR4- und MEKK3-Aktivität dämpfen. Im Gegensatz dazu fördern TMAO und bestimmte Indol-Derivate, etwa Indoxylsulfat, Entzündung, oxidativen Stress und stärkere TLR4-Signale, was die MEKK3-Aktivierung verstärken kann. Auch Immunzellen spielen eine Rolle: Neutrophile können klebrige extrazelluläre Netzwerke freisetzen, die TLR4 auf Gefäßzellen weiter stimulieren, während proinflammatorische Makrophagen und T-Helferzellen MEKK3-verknüpfte Wege verstärken; antiinflammatorische Gegenstücke können sie hemmen. Gemeinsam erzeugen diese Signale ein dynamisches Tauziehen darüber, ob Hirngefäße stabil bleiben oder zu kavernösen Läsionen degenerieren.
Neue Wege zu schonenderen Behandlungen
Die aktuellen Behandlungsmöglichkeiten für zerebrale kavernöse Malformationen sind begrenzt und stützen sich oft auf Operationen oder präzise Strahlentherapie bei hochriskanten Läsionen. Die Autoren argumentieren, dass das Verständnis, wie Darmmikroben und ihre Produkte in MEKK3-zentrierte Signalwege einfließen, neue, weniger invasive Optionen eröffnet. Grundsätzlich könnten künftige Therapien mikrobiomorientierte Strategien—wie Ernährung, Probiotika oder gezielte Reduktion schädlicher Metaboliten—mit Medikamenten kombinieren, die TLR4- oder MEKK3-Aktivität in Hirngefäßen dämpfen. Für Laien lautet die Kernbotschaft, dass Störungen im Darm weitreichende Auswirkungen auf die Gesundheit der Hirngefäße haben können und dass ein einzelner zellulärer „Knotenpunkt“ wie MEKK3 der Schlüssel sein könnte, um dieses schädliche Gespräch zu entschärfen und gefährliche Hirnblutungen zu verhindern.
Zitation: Cheng, P., Han, H., Huang, Y. et al. MEKK3 bridges gut-brain communication and cerebral cavernous malformation pathogenesis. Cell Death Discov. 12, 197 (2026). https://doi.org/10.1038/s41420-026-03062-6
Schlüsselwörter: zerebrale kavernöse Malformation, Darm-Hirn-Achse, MEKK3-Signalübertragung, Stoffwechselprodukte der Darmmikrobiota, neurovaskuläre Entzündung